Презентация на тему: Оксиды. Состав. Классификация. Номенклатура. Свойства. Получение. Применение



Создать условия для изучения классификации неорганических веществ и самостоятельному применению знаний в сходной и новой ситуациях. Создать условия для изучения классификации неорганических веществ и самостоятельному применению знаний в сходной и новой ситуациях.

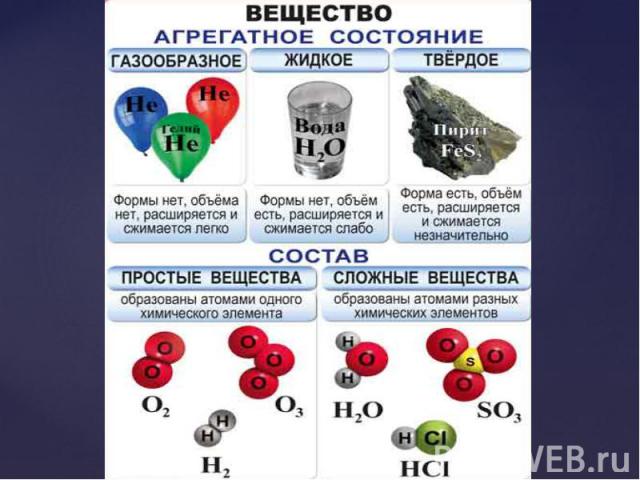
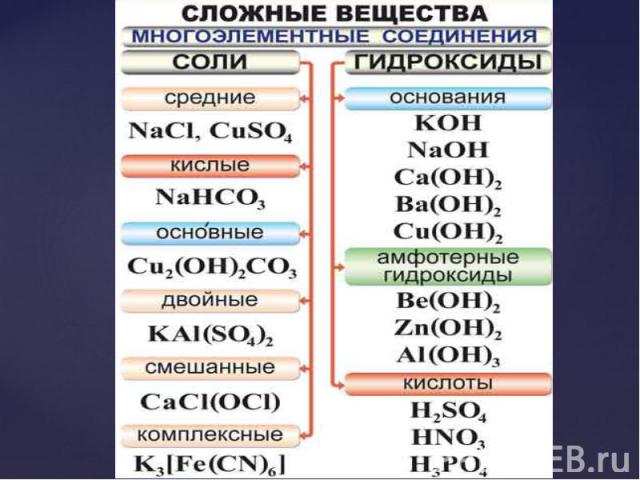
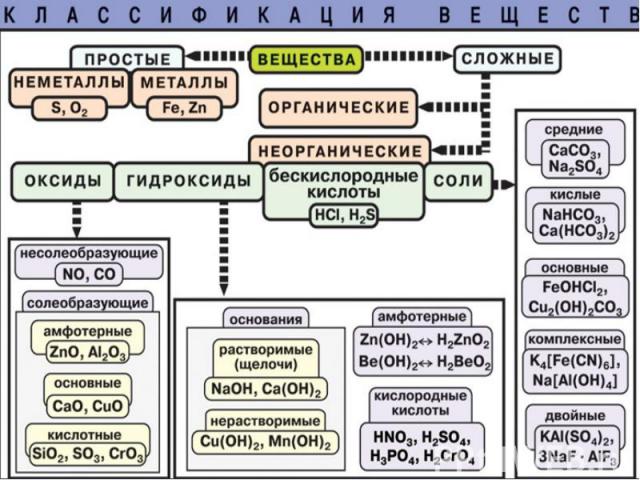
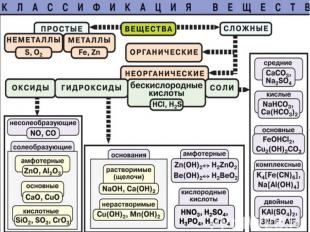
Простые и сложные вещества; Простые и сложные вещества; Классификация и номенклатура; Оксиды; Основания; Кислоты; Соли.







Оксиды; Оксиды; Состав; Классификация; Номенклатура; Свойства; Получение; Применение.

(окисел, окись) — бинарное соединение химического элемента с кислородом в степени окисления −2, в котором сам кислород связан только с менее электроотрицательным элементом. (окисел, окись) — бинарное соединение химического элемента с кислородом в степени окисления −2, в котором сам кислород связан только с менее электроотрицательным элементом.


1. Солеобразующие: 1. Солеобразующие: Основной оксид (МеО - Wме – I, II) Амфотерный оксид (МеО - Wме – III – исключение оксид бериллия, оксид цинка, оксид марганца (IV)) Кислотный оксид (МеО, неМеО – W ≥ IV) 2. Несолеобразующие (безразличные): неМеО - WнеМе ≤ IV

Оксид серы (IV); Оксид серы (IV); Оксид калия; Оксид алюминия; Оксид железа (II); Оксид железа (III); Оксид марганца (VII); Оксид серебра.

Оксид серы (IV) – SO2 - кислотный ; Оксид серы (IV) – SO2 - кислотный ; Оксид калия – K2O - основной; Оксид алюминия – Al2O3 - амфотерный; Оксид железа (II) – FeO - основной; Оксид железа (III) – Fe2O3 - амфотерный; Оксид марганца (VII) – Mn2O7 - кислотный; Оксид серебра – Ag2O - основной.



1. ... + H2O → МеОН (р) 1. ... + H2O → МеОН (р) 2. ... + HR → MeR + H2O 3. ... + кислотный оксид → MeR

... + H2O → HR (р) ... + H2O → HR (р) ... + MeOH(р) → MeR + H2O ... + основной оксид → MeR

... + HR (р) → MeR + H2O ... + HR (р) → MeR + H2O ... + MeOH(р) → MeR + H2O

1. Рассмотреть химические свойства: 1. Рассмотреть химические свойства: 1 ряд – оксид лития; 2 ряд – оксид азота (IV); 3 ряд – оксид цинка. 2. Составьте рассказ о происхождении данных оксидов. 3. Осуществите превращение: литий → оксид лития → гидроксид лития → ортофосфат лития


Непосредственное соединение простого вещества с кислородом; Непосредственное соединение простого вещества с кислородом; Горение сложных веществ; Разложение при нагревании кислородных соединений: карбонатов, нитратов, нерастворимых оснований.

1. Непосредственное соединение простого вещества с кислородом (демонстрационый эксперимент): 1. Непосредственное соединение простого вещества с кислородом (демонстрационый эксперимент):




1. Сложные вещества делят на …; 1. Сложные вещества делят на …; 2. Основной оксид - …; 3. Кислотный оксид - …; 4. Основания – это сложные вещества, состоящие из …; 5. Кислоты – это сложные вещества, состоящие из …; 6. Соли – это сложные вещества, состоящие из …

1. Оксиды – сложные вещества, состоящие из двух элементов, один из которых кислород; 1. Оксиды – сложные вещества, состоящие из двух элементов, один из которых кислород; 2. Неметаллы обладают металлическим блеском; 3. Оксид серы (IV) – кислотный оксид; 4. Оксид натрия – кислотный оксид; 5. Реакция обмена – реакция между основанием и кислотой.

1. Оксиды – сложные вещества, состоящие из двух элементов, один из которых кислород; 1. Оксиды – сложные вещества, состоящие из двух элементов, один из которых кислород; 2. Неметаллы обладают металлическим блеском; 3. Оксид серы (IV) – кислотный оксид; 4. Оксид натрия – кислотный оксид; 5. Реакция обмена – реакция между основанием и кислотой.

1. Литий, вода, натрий, алюминий; 1. Литий, вода, натрий, алюминий; 2. Фосфор, сера, кремний, железо; 3. Оксид бария, оксид фосфора (V), оксид азота (IV), оксид серы (IV); 4. Серная кислота, сернистая кислота, фосфорная кислота, угольная кислота; 5. Гидроксид калия, гидроксид кальция, гидроксид лития, гидроксид натрия.

1. Fe(OH)2; Cu(OH)2; NaOH; Zn(OH)2; 2. Na2O; BeO; CaO; CuO; 3. H2SO4; HClO4; H2S; H2CO3; 4. Na2SO4; KCl; HF; KNO3.

HCl, K2O, NaOH, K2CO3, Ca(OH)2, HNO3, Zn(OH)2, SO2, Fe(OH)2, H2SO4, Fe2O3, MgSO4. HCl, K2O, NaOH, K2CO3, Ca(OH)2, HNO3, Zn(OH)2, SO2, Fe(OH)2, H2SO4, Fe2O3, MgSO4.

1. Бромид железа (III); 1. Бромид железа (III); 2. Сульфат марганца (II); 3. Гидросульфид натрия; 4. Дихромовая кислота; 5. Нитрат меди (II); 6. Азотистая кислота; 7. Иодид бария; 8. Дигидрофосфат железа (III); 9. Гидрокарбонат кальция; 10. Сульфат натрия.

- Знаю – - Знаю – - Узнал – - Хочу узнать –


1. Я познаю мир: Детская энциклопедия: Химия/ Авт.-сост. Л. А. Савина; Худож. А. В. Карадашук, О. М. Войтенко. – М.: ООО «Издательство АСТ-ЛТД», 1998. – 448 с. 1. Я познаю мир: Детская энциклопедия: Химия/ Авт.-сост. Л. А. Савина; Худож. А. В. Карадашук, О. М. Войтенко. – М.: ООО «Издательство АСТ-ЛТД», 1998. – 448 с. 2. Кузнецова Н. Е., Титова И. М., Гара Н. Н., Жегин А. Ю. Химия. Учебник для учащихся 8 класса общеобразовательных учреждений. – М.: «Вентана-Граф», 1997. – 336 с. 3. Рудзитис Г. Е. Химия: неорган. химия: учеб. для 8 кл. общеобразоват. учреждений/ Г. Е. Рудзитис, Ф. Г. Фельдман. – 12-е изд. испр. – М.: Просвещение, 2008. – 176 с. 4. Полный комплект цветных таблиц по неорганической химии. Весь курс средней школы 100 таблиц формата А1. Авторы: Назарова Т.С., Куприянова Н.С., Кожевников Д.Н., Назарова А.Г. 5. Лидин Р. А. Задачи, вопросы и упражнения по химии: 8 – 11 кл.: Пособие для учащихся общеобразоват. учреждений/ Р. А. Лидин, Л. Ю. Аликберова. – М.: просвещение, 2002. – 189 с. http://www.ekko.com.ua/img/gor1.jpg http://atf-bntu.narod.ru/articles/generator.html