Презентация на тему: металл, «капнувший с неба»


Шестерых я слуг имел, И все от них о мире знал: Вот как всех я их зову: Кто? Что? Как? Где? Когда? и Почему? Редьярд Киплинг «Слоненок»

… …

В таблице Д.И. Менделеева трудно найти какой-либо иной элемент, с которым так неразрывно связывалась бы жизнь всего человечества. Нет в таблице другого такого элемента, при участии которого проливалось бы столько крови, терялось бы столько жизней, происходило бы столько несчастий. В таблице Д.И. Менделеева трудно найти какой-либо иной элемент, с которым так неразрывно связывалась бы жизнь всего человечества. Нет в таблице другого такого элемента, при участии которого проливалось бы столько крови, терялось бы столько жизней, происходило бы столько несчастий.

Но железо – не только борьба, война, разрушения. Железо – металл созидания, железо – основа всей металлургии, машиностроения, транспорта, грандиозных инженерных сооружений от башни Эйфеля до железнодорожных мостов. Но железо – не только борьба, война, разрушения. Железо – металл созидания, железо – основа всей металлургии, машиностроения, транспорта, грандиозных инженерных сооружений от башни Эйфеля до железнодорожных мостов.

Всё, всё – начиная от швейной иглы и кончая паутиной железных дорог, авианосцами, огнедышащими домнами, где рождается само железо – состоит из железа. Всё, всё – начиная от швейной иглы и кончая паутиной железных дорог, авианосцами, огнедышащими домнами, где рождается само железо – состоит из железа.


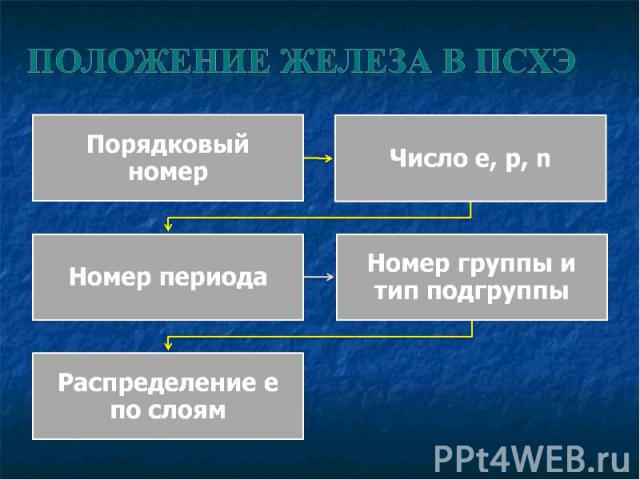
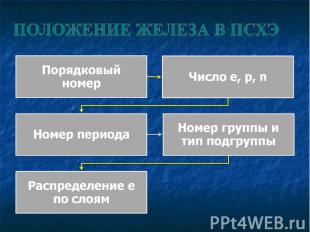
Охарактеризовать элемент железо, исходя из его положения в таблице Менделеева Охарактеризовать элемент железо, исходя из его положения в таблице Менделеева Узнать, где находится железо в природе Рассмотреть физические свойства железа Изучить химические свойства железа Рассмотреть применение и значение железа

Выполнить задания своей группы Выполнить задания своей группы Составить конспект по теме «Железо» Ответить на вопросы теста Оценить свою работу на уроке по 5-ти бальной системе

1 группа 1. Характеристика элемента железо 1 группа 1. Характеристика элемента железо 2. Нахождение элемента железо в природе 2 группа 1. Физические свойства вещества железо 2. Применение железа 3 группа 1. Химические свойства железа 2. Значение железа в развитии человеческой цивилизации

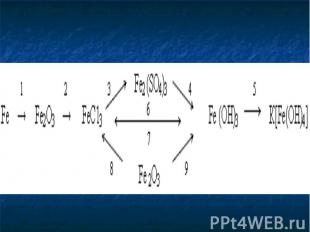
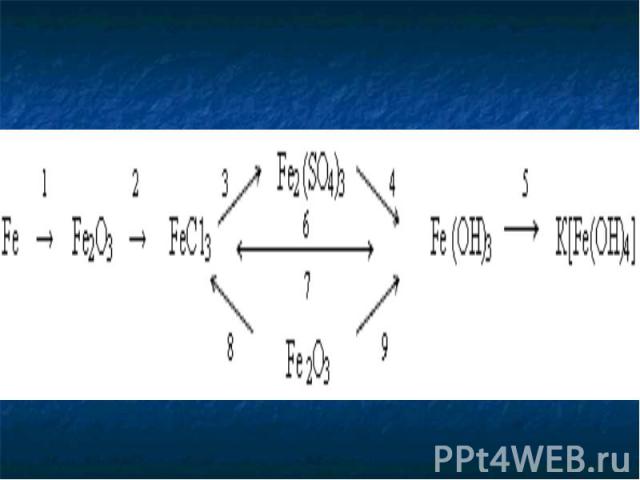
2. Расставьте степени окисления элементов: 2. Расставьте степени окисления элементов: FeCl2, Fe2O3, FeCl3, FeS, FeO
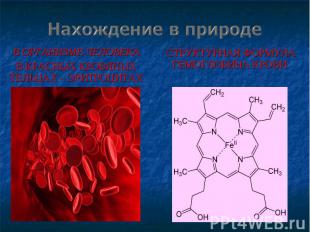
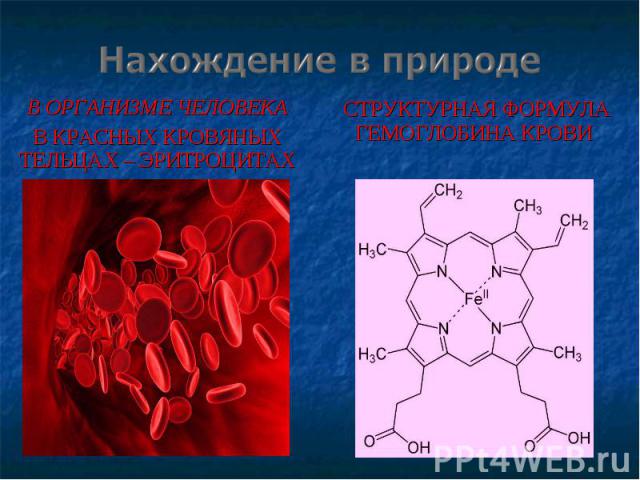
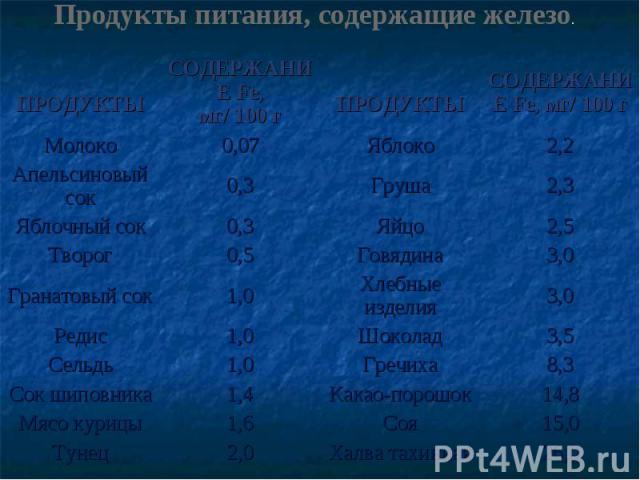
В ОРГАНИЗМЕ ЧЕЛОВЕКА В ОРГАНИЗМЕ ЧЕЛОВЕКА В КРАСНЫХ КРОВЯНЫХ ТЕЛЬЦАХ – ЭРИТРОЦИТАХ

Железо влияет на процесс фотосинтеза Железо влияет на процесс фотосинтеза






или кровавик или кровавик У магов он служит для вычерчивания на полу магического круга и тайных знаков.






1. Как называется болезнь, когда не хватает организму железа? 1. Как называется болезнь, когда не хватает организму железа? ЖЕЛЕЗОДЕФИЦИТНАЯ АНЕМИЯ. 2. Встречается ли железо в виде самородков? ДА 3. Может ли железо падать с неба? МЕТЕОРИТЫ 4. Красные клетки крови, содержащие железо? ЭРИТРОЦИТЫ 5. Как свидетельствует в «Одиссее» Гомер, победителя игр, устроенных Ахиллесом, награждали кусками двух металлов ЗОЛОТА и ЖЕЛЕЗА. 6. Какие степени окисления присущи железу? +2,+3 7.Самые распространенные сплавы железа? ЧУГУН И СТАЛЬ.

§14, с. 68 З. 5 §14, с. 68 З. 5 Задание по желанию Составить мини-сочинение, рекламный ролик, рекламный проспект, кроссворд, тест (15 вопросов) о железе



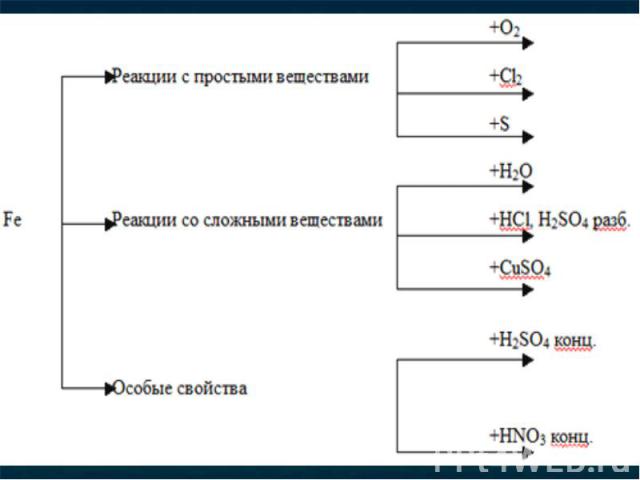
1. У этого металла последние электроны заполняют не внешний, а предвнешний энергетический уровень. 1. У этого металла последние электроны заполняют не внешний, а предвнешний энергетический уровень. 2. На внешнем энергетическом уровне этого металла 2е. 3. Для этого металла характерна постоянная степень окисления. 4. Это один из самых легких и мягких металлов. 5. Этот металл проявляет восстановительные свойства в реакциях. 6. Этот металл не взаимодействует с растворами солей. 7. При взаимодействии с серой этот металл приобретает степень окисления +2. 8. Этот металл вытесняет водород из соляной и разбавленной серной кислоты.

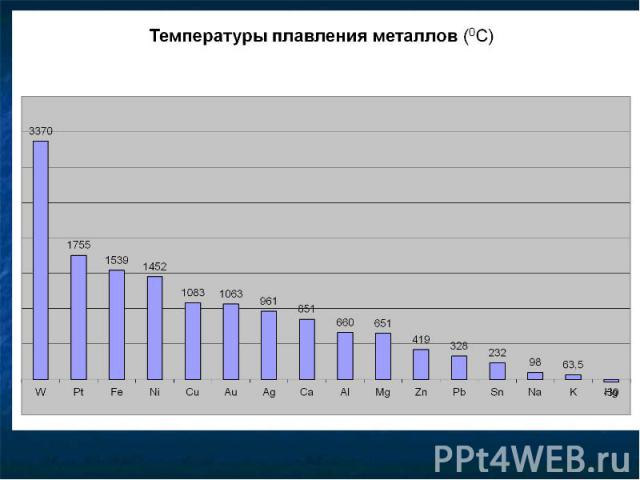
9. Этот металл образует металлическую кристаллическую решетку и металлическую связь. 9. Этот металл образует металлическую кристаллическую решетку и металлическую связь. 10. На внешнем энергетическом уровне у атома этого металла 3 электрона. 11. Для этого металла характерна переменная степень окисления. 12. Этот металл обладает сильными магнитными свойствами. 13. Этот металл при взаимодействии с кислородом образует смесь оксидов МеО и Ме2О3 14. При взаимодействии с хлором этот металл приобретает степень окисления +3 15. Этот металл не взаимодействует с концентрированной серной и азотной кислотами при нормальных условиях. 16. Это серебристо-серый металл, ковкий и пластичный, с температурой плавления 15390С.