Презентация на тему: Процессы в растворах электролитическая диссоциация


Электролиты Электролиты - вещества, растворы и расплавы которых не проводят электрический ток.

вещества, которые содержат ковалентные неполярные или малополярные связи. Эти связи не распадаются на ионы. вещества, которые содержат ковалентные неполярные или малополярные связи. Эти связи не распадаются на ионы. газы, твердые вещества (неметаллы), органические соединения (сахароза, бензин, спирт).

Вещества, которые содержат ионные и ковалентные полярные связи. Эти связи легко распадаются на ионы. Вещества, которые содержат ионные и ковалентные полярные связи. Эти связи легко распадаются на ионы. Неорганические кислоты, основания, соли.



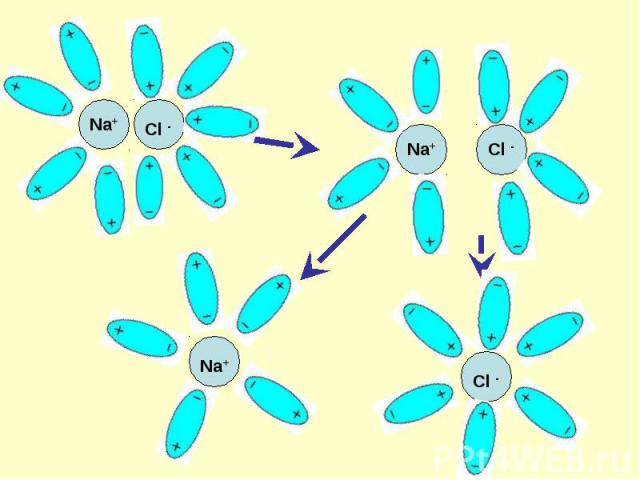
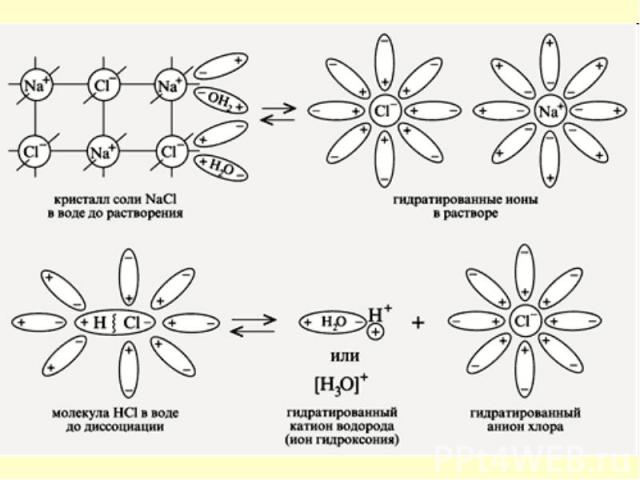
Ориентация диполей воды вокруг кристаллов соли. Ориентация диполей воды вокруг кристаллов соли. Образование между молекулами воды и ионами кристаллов слабых связей. Разрушение кристаллической решетки и образование гидратированных ионов.
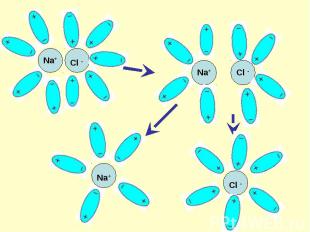

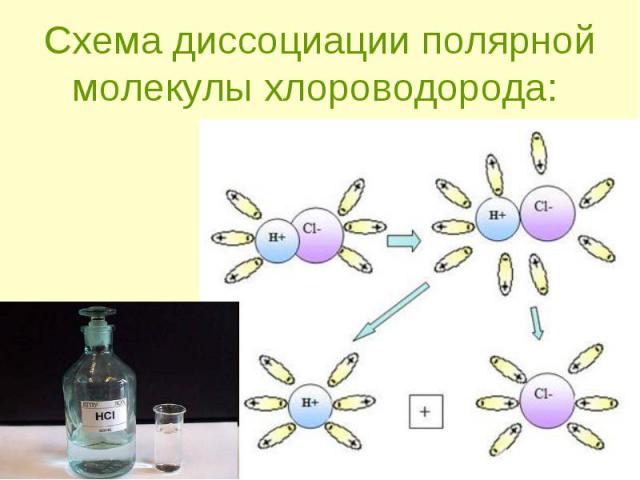
ориентация диполей воды вокруг полярной молекулы. ориентация диполей воды вокруг полярной молекулы. еще большая поляризация полярной молекулы и превращение полярной связи ее в ионную. образование свободных гидратирован-ных ионов.
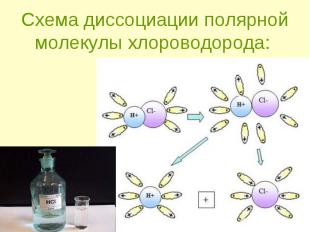

Сильные Сильные - при растворении в воде практически полностью распадаются на ионы.

вещества с ионными или сильно полярными связями. вещества с ионными или сильно полярными связями. все хорошо растворимые соли, сильные кислоты (HCl, HBr, HI, HClO4, H2SO4,HNO3) и сильные основания: LiOH, NaOH, KOH, RbOH, CsOH, Вa(OH)2, Sr(OH)2, Сa(OH)2.

вещества с неполярными и малополярными связями: вещества с неполярными и малополярными связями: 1) почти все органические кислоты (CH3COOH, C2H5COOH и др.); 2) некоторые неорганические кислоты (H2CO3, H2S и др.); 3) почти все малорастворимые в воде соли, основания и гидроксид аммония (Ca3(PO4)2; Ca(OH)2; Al(OH)3; NH4OH);

Степень диссоциации (α) - отношение числа распавшихся на ионы молекул (n) к общему числу растворенных молекул (N): Степень диссоциации (α) - отношение числа распавшихся на ионы молекул (n) к общему числу растворенных молекул (N):

CaCl2 = Ca2+ + 2Cl- CaCl2 = Ca2+ + 2Cl- KAl(SO4)2 = K+ + Al3+ + 2SO42- HNO3 = H+ + NO3- Ba(OH)2 = Ba2+ + 2OH-

осуществляется ступенчато. На каждой ступени отщепляется один ион водорода. осуществляется ступенчато. На каждой ступени отщепляется один ион водорода. H Cl = H+ + Cl - - H2SO4 = H+ + HSO4- (I ступень) HSO4- = H+ + SO42- (II ступень) Кислоты - при диссоциации образуют катионы водорода и анионы кислотного остатка.

Ba(OH)2 = Ba2+ + 2OH- Ba(OH)2 = Ba2+ + 2OH- Сa(OH)2 = Сa2+ + 2OH- Основания - при диссоциации образуют катионы металла и анионы - гидроксид-ионы.

Средние соли – соли, состоящие из атомов металла и кислотного остатка, диссоциируют в одну ступень: Средние соли – соли, состоящие из атомов металла и кислотного остатка, диссоциируют в одну ступень: CaCl2 = Ca2+ + 2Cl- KBr = K+ + Br- NaCl = Na+ + Cl-

Кислые соли – соли, в состав молекул которых кроме атомов металла входят атомы водорода, распадаются ступенчато. Сначала отрываются все атомы металла, а затем атомы водорода по- одному. Кислые соли – соли, в состав молекул которых кроме атомов металла входят атомы водорода, распадаются ступенчато. Сначала отрываются все атомы металла, а затем атомы водорода по- одному. KHCO3 = K+ + HCO3− HCO3− = H+ + CO32-

В 1887 году создал теорию ЭД. В 1887 году создал теорию ЭД. В 1903году был удостоен Нобелевской премии "За чрезвычайные заслуги в развитии химии".


Русские химики И.А.Каблуков и В.А.Кистяковский применили к объяснению электролитической диссоциации химическую теорию растворов Д.И.Менделеева и доказали, что при растворении электролита происходит химическое взаимодействие растворенного вещества с водой, которое приводит к образованию гидратов, а затем они диссоциируют на ионы. Русские химики И.А.Каблуков и В.А.Кистяковский применили к объяснению электролитической диссоциации химическую теорию растворов Д.И.Менделеева и доказали, что при растворении электролита происходит химическое взаимодействие растворенного вещества с водой, которое приводит к образованию гидратов, а затем они диссоциируют на ионы.

1. Электролиты в водной среде (и в 1. Электролиты в водной среде (и в расплавленном состоянии) распадаются на положительно заряженные ионы (катионы) и отрицательно заряженные ионы (анионы).
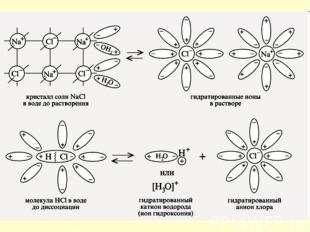

2. Беспорядочное движение ионов в растворе под действием электрического поля становится направленным: положительно заряженные ионы (катионы) движутся к электроду с отрицательным зарядом (катоду), а анионы – к аноду. 2. Беспорядочное движение ионов в растворе под действием электрического поля становится направленным: положительно заряженные ионы (катионы) движутся к электроду с отрицательным зарядом (катоду), а анионы – к аноду.

3. Диссоциация – обратимый процесс: параллельно с распадом молекул на ионы (диссоциацией) протекает процесс соединения ионов (ассоциация). Поэтому в уравнениях электролитической диссоциации вместо знака равенства ставят знак обратимости. NaCl Na+ + Cl- 3. Диссоциация – обратимый процесс: параллельно с распадом молекул на ионы (диссоциацией) протекает процесс соединения ионов (ассоциация). Поэтому в уравнениях электролитической диссоциации вместо знака равенства ставят знак обратимости. NaCl Na+ + Cl-

4. Степень электролитической диссоциации (a) зависит от природы электролита и растворителя, температуры и концентрации. Она показывает отношение числа молекул, распавшихся на ионы (n) к общему числу молекул, введенных в раствор (N). 4. Степень электролитической диссоциации (a) зависит от природы электролита и растворителя, температуры и концентрации. Она показывает отношение числа молекул, распавшихся на ионы (n) к общему числу молекул, введенных в раствор (N).

5. Свойства ионов резко отличаются от 5. Свойства ионов резко отличаются от свойств нейтральных атомов составляющих их элементов. Ионы в водных растворах гидратированы.

http://slovari.yandex.ru/ http://slovari.yandex.ru/ http://www.lyceum8.ru/himiya/4.htm http://900igr.net/fotografii/khimija/Dissotsiatsija/010-Mekhanizm-dissotsiatsii-veschestv.html http://him.1september.ru/2003/34/7.htm http://900igr.net/kartinki/khimija/Povarennaja-sol/059-K-r-i-s-t-a-l-l-y-g-a-l-i-t-a.html