Презентация на тему: Основание

ОСНОВАНИЕ

Какие вещества называются основаниями? Гидроксиды металлов с общей формулой M(OH)n (M – металл, n – его валентность, обычно n < 3) называются основаниями. Основания – это сложные вещества, в которых атомы металлов соединены с одной или несколькими гидроксильными группами. Например, основаниями являются гидроксиды натрия NaOH, магния Mg(OH)2, железа (III) Fe(OH)3.
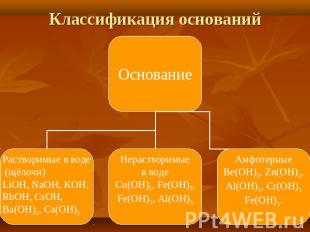
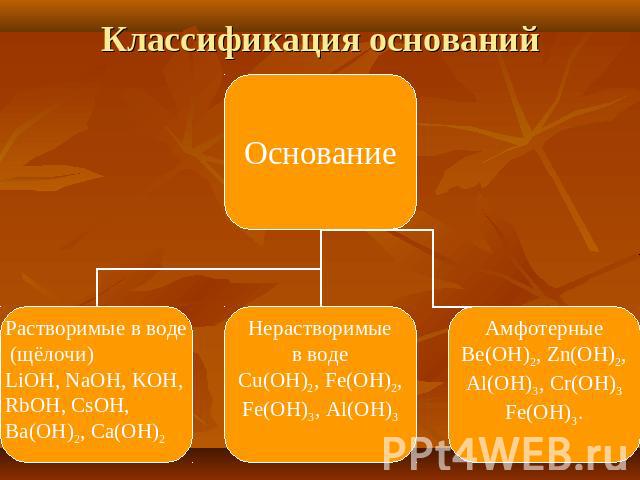
Классификация оснований

Физические свойства Все основания металлов – твердые вещества. Как и соли, они могут быть бесцветными и окрашенными. Основания делятся на растворимые и нерастворимые в воде. Растворимые в воде основания образованы самыми активными металлами, которые реагируют с водой при обычных температурах. Эти металлы находятся в IA группе (щелочные металлы) и во IIA группе (щелочноземельные металлы). Их гидроксиды называются щелочами.

Гидроксид калия (едкое кали)

Гидроксид кальция (гашеная известь)

Гидроксид натрия (натр едкий, каустическая сода )

Получение В лаборатории: Щелочей: 1. Взаимодействием активного металла с водой 2К + 2Н2О → 2КОН + Н2↑ 2. Взаимодействием основных оксидов с водой К2О + Н2О → 2КОН В промышленности: Электролиз солей. Нерастворимые основания получают действием щелочей на соли: CuCl2 + NaOH → Cu(OH)2↓ + 2NaCl

Химические свойства 1. Изменяют окраску индикатора: NaOH + фенолфталеин → малиновая окраска NaOH + лакмус → синяя окраска NaOH + метиловый оранжевый → желтый 2. Взаимодействие с кислотными оксидами: 2NaOH + CO2 = Na2CO3 + H2O 3. Взаимодействие с кислотами: NaOH + HCl → NaCl + H2O Взаимодействуют с растворами солей: FeCl3 + 3NaOH → Fe(OH)3↓ + 3NaCl

Нерастворимые основания: Взаимодействие с кислотами: Cu(OH)2 + 2HCl → CuCl2 + 2H2O При нагревании разлагаются: Cu(OH)2 → CuO + H2O Присутствие щелочей может быть обнаружено и на ощупь, их растворы "мылкие". (Осторожно! Не рекомендуем пробовать – это опасно! Так как они разъедают многие органические вещества).

Применение LiOH – в аккумуляторах. NaOH – для очистки нефти, производства мыла, в текстильной промышленности, для органического синтеза. KOH - в аккумуляторах. Ca(OH)2 – в производстве сахара, соды, в строительстве, применяют для приготовления бордовской смеси – средства для борьбы с болезнями и вредителями растений.

Тест «Пятерочка» 1. Выберите формулы оснований: а) SO3 б) Mg(OH)2 в) H2SO4 г) СаО 2. К каждому из ниже указанных веществ прибавили воду и фенолфталеин. В каких случаях появится малиновое окрашивание? а) BaO б) HNO3 в) CuO г) КОН 3. Какие из указанных гидроксидов не могут быть получены взаимодействием соответствующих оксидов с водой? а) Аl(OH)3 б) Fe(OH)3 в) Са(ОН)2 г) LiOH

4.Окраска индикаторов под действием раствора гидроксида калия меняется следующим образом: а) лакмус краснеет б) лакмус синеет в) Метилоранж краснеет г) Метилоранж желтеет д) фенолфталеин становится малиновым е) Фенолфталеин остается бесцветным 5. Раствор гидроксида калия вступает в химические реакции с веществами, формулы которых а) СО2 б) H2S в) Са(ОН)2 г) Cu д) NaNO3 e) Mg

Ответы 1. б 2. а г 3. а б 4. б г д 5. а б

Домашние задание § 31 Упр. 6,9. Зад. 1,3.

Задача К 16,2 г смеси оксидов натрия и никеля, содержащей 38,3% оксида натрия, прибавили 200 мл воды. Какова массовая доля (%) щелочи в полученном растворе?