Презентация на тему: Оксиды

Тема урока:Оксиды Презентацию разработала Носенко Е.М.учитель химии МОУ СОШ № 9 с. Подлужное Изобильненского района

Цель урока. Обобщить знания о составе оксидов, рассмотреть их классификацию и свойства основных и кислотных оксидов.

ОксидыОксиды — это сложные вещества, в составе которых два Химических элемента и один из них всегда кислород. Оксиды железа входят в состав красного, бурого и магнитного железняка, из которых получают железо и его сплавы — сталь, чугун.Оксид кальция — негашеная известь. Из негашеной извести получают гашеную (известь Са(ОН)2), которую широко применяют в строительстве.Оксид кремния — это кварц, горный хрусталь, песок кварцевый, речной и морской, входит в состав окрашенных в разнообразные цвета минералов и поделочных камней — аметисты, топазы, агаты, опалы, яшмы.Оксид углерода — углекислый газ содержится в выдыхаемом нами воздухе, в выбросах автомобильных двигателей, заводов, ...

Состав и классификация оксидов Кислоты соответствуют Кислотные оксиды Щелочи соответствуют Основные оксиды
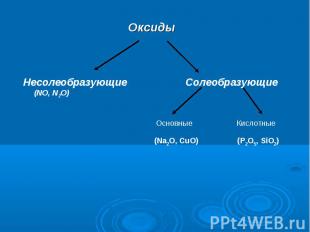
Несолеобразующие Солеобразующие (NO, N2O) (Na2O, CuO) (P2O5, SiO2)

1) получить углекислый газ взаимодействием мрамора и соляной кислоты в пробирке с газоотводной трубкой, а затем пропустить его во вторую пробирку с «известковой водой»2) взаимодействие серной кислоты с оксидом меди (II) при нагревании.

Демонстрационный эксперимент а) P Р2O5 H3PO4 б) Ca CaO Ca(OH)2