Презентация на тему: КОРРОЗИЯ МЕТАЛЛОВ


Коррозия – рыжая крыса, Грызет металлический лом. В Шефнер.

- называют самопроизвольное разрушение металлов и сплавов под влиянием окружающей среды Зачем нам нужно изучать этот процесс? Назовите последствия коррозии.
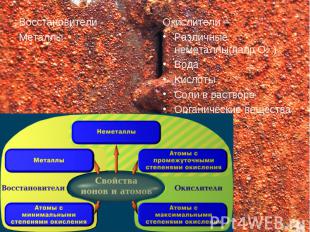
Восстановители - Металлы

Химическая Коррозия Электрохимическая коррозия С 170 -171 учебника

Компоненты окружающей среды окисляют непосредственно металл. Протекающие при химической коррозии окислительно - восстановительные реакции осуществляются путем непосредственного перехода электронов с атомов металлов на частицы окислителя, входящего в состав среды.

Коррозия протекающая в токопроводящей среде. Помимо химической реакции, в системе возникает электрический ток. Процесс электрохимической коррозии происходит при контакте двух металлов Разрушается металл с более сильными восстановительными свойствами (выполняет роль анода)

1 группа – щелочные металлы – наименьшая коррозийная стойкость.(побочная подгруппа – весьма стойкие металлы) 2 группа – главная подгруппа – малоустойчивы, побочная – более устойчивы( в присутствии кислорода образуют прочные пленки оксидов, предохраняющие от дальнейшего разрушения)

3 группа – Алюминий – образуется прочная оксидная пленка ( но она разрушается в растворах кислот и щелочей) В концентрированной азотной и серной кислотах алюминий пассивируется. 3 группа – Алюминий – образуется прочная оксидная пленка ( но она разрушается в растворах кислот и щелочей) В концентрированной азотной и серной кислотах алюминий пассивируется. 4 группа – Олово и свинец – стойкие к коррозии металлы, благодаря прочным оксидным пленкам.

5,6,7,8группы. – металлы побочных подгрупп обладают высокой способностью к пассивации, а следовательно, большой коррозионной стойкостью. 5,6,7,8группы. – металлы побочных подгрупп обладают высокой способностью к пассивации, а следовательно, большой коррозионной стойкостью. Осмий, Иридий, Платина – самые стойкие к коррозии Железо пассивируется концентрированной серной и азотной

Нанесение защитных покрытий. Использование нержавеющих сталей. Введение в рабочую среду ингибиторов коррозии. Удаление веществ, вызывающих коррозию(Деаэрация – удаление растворенного в воде кислорода). Создание контакта с более активным металлом – протектором.