Презентация на тему: Класс альдегидов

Альдегиды 900igr.net

Аль–де–гид Алкоголь дегидрированный Спирт, лишённый водорода: Н O R–C–O–H R–C + H2 H H спирт альдегид t, kat

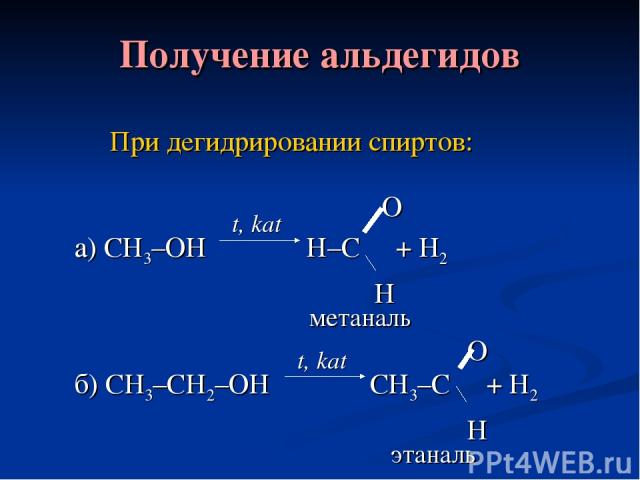
Получение альдегидов При дегидрировании спиртов: О а) СН3–ОН Н–С + Н2 Н метаналь О б) СН3–СН2–ОН СН3–С + Н2 Н этаналь t, kat t, kat
![Альдегиды образуются при окислении первичных спиртов Н О–Н │ │ СН3–С–ОН + [О] → Альдегиды образуются при окислении первичных спиртов Н О–Н │ │ СН3–С–ОН + [О] →](https://fs3.ppt4web.ru/images/132073/183581/310/img3.jpg)
Альдегиды образуются при окислении первичных спиртов Н О–Н │ │ СН3–С–ОН + [О] → СН3–С–ОН → │ │ Н Н О → СН3–С + Н2О Н В общем виде: O R–OH + [О] → R–C + Н2О H

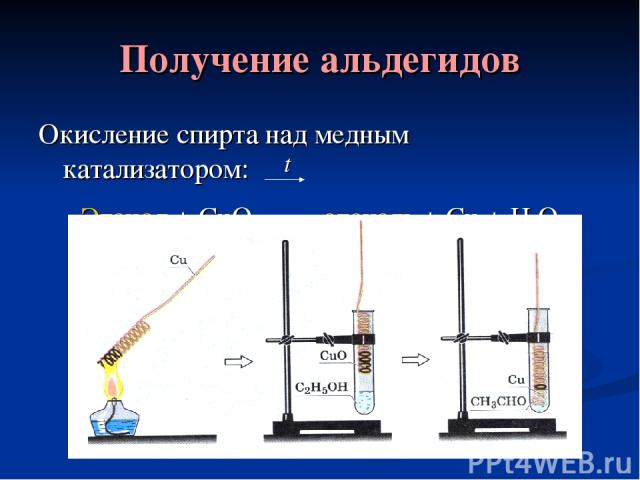
Получение альдегидов Окисление спирта над медным катализатором: Этанол + CuO этаналь + Cu + H2O t
![Получение альдегидов Окисление спирта перманганатом калия: Спирт + [O] → альдеги Получение альдегидов Окисление спирта перманганатом калия: Спирт + [O] → альдеги](https://fs3.ppt4web.ru/images/132073/183581/310/img5.jpg)
Получение альдегидов Окисление спирта перманганатом калия: Спирт + [O] → альдегид + H2O В нашем организме окисление спирта происходит в печени.
![При окислении вторичных спиртов образуются кетоны СН3–СН–СН3 + [O] → CH3–C–CH3 + При окислении вторичных спиртов образуются кетоны СН3–СН–СН3 + [O] → CH3–C–CH3 +](https://fs3.ppt4web.ru/images/132073/183581/310/img6.jpg)
При окислении вторичных спиртов образуются кетоны СН3–СН–СН3 + [O] → CH3–C–CH3 + H2O OH O пропанол-2 пропанон-2 (ацетон) Запомните: альдегиды и кетоны содержат карбонильную группу , поэтому их объединяют в группу карбонильных соединений.

НСОН – метаналь; муравьиный альдегид; формальдегид; водный раствор в воде – формалин. СН3СОН – этаналь; уксусный альдегид; ацетальдегид* *Этаналь может быть получен из ацетилена (реакция Кучерова): O НС≡СН + Н2О CH3 – C H Номенклатура альдегидов HgSO4, H2SO4
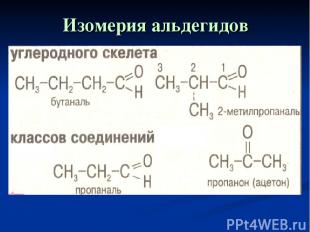
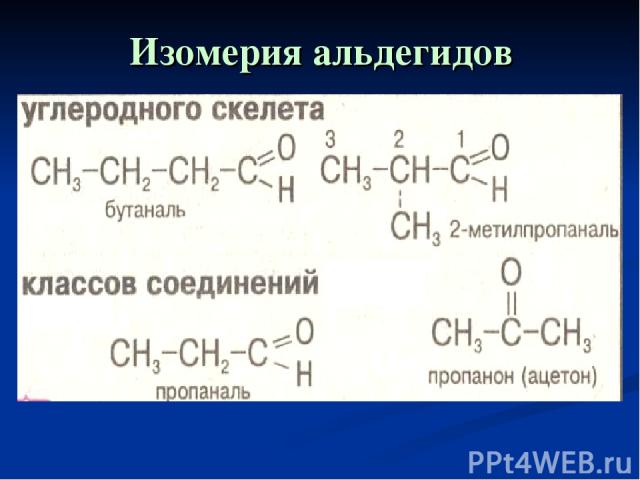
Изомерия альдегидов с кетонами

Физические свойства альдегидов Первый представитель класса – метаналь – при комнатной температуре является газом (с характерным запахом). Низкие температуры кипения альдегидов (по сравнению со спиртами) объясняются ОТСУТСТВИЕМ водородных связей между молекулами альдегидов.

Физические свойства альдегидов Молекула альдегидов содержит полярную альдегидную группу: Благодаря чему первые представители гомологического ряда альдегидов хорошо растворяются в воде.

Химические свойства альдегидов (реакции окисления) Окисление альдегидов аммиачным раствором оксида серебра: Формальдегид + Ag2O муравьиная + 2Ag↓ (аммиач.р-р) кислота Ацетальдегид + Ag2O уксусная + 2Ag↓ (аммиач.р-р) кислота Это реакция «серебряного зеркала» t t

Взаимодействие с гидроксидом меди (II) при нагревании: Метаналь + 2Cu(OH)2 метановая + Сu2O + 2H2O кислота Этаналь + 2Cu(OH)2 этановая + Сu2O + 2H2O кислота Химические свойства альдегидов (реакции окисления) t t

t, kat Химические свойства альдегидов (реакции восстановления) Гидрирование альдегидов с образованием спиртов: Метаналь + Н2 метанол Этаналь + Н2 этанол t, kat
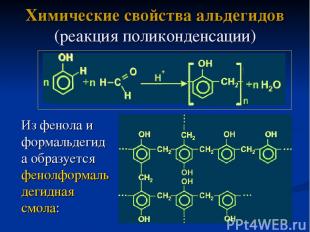
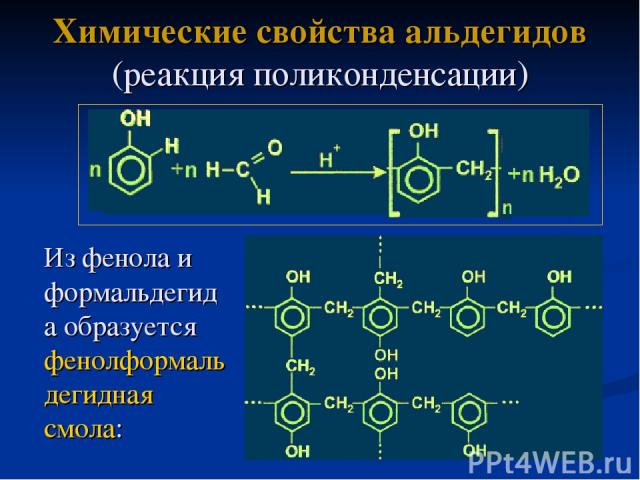
Химические свойства альдегидов (реакция поликонденсации) Из фенола и формальдегида образуется фенолформальдегидная смола:

Применение альдегидов Формальдегид Ацетальдегид

Знаете ли вы, что… Формальдегид содержится в древесном дыме. Он обеспечивает консервирующее действие (за счёт уничтожения бактерий) в ходе копчения пищевых продуктов. Бактерицидное действие формальдегида основано на его взаимодействии с белками, что лишает белки возможности выполнять свои функции. Формальдегид может образоваться в нашем организме из метанола под действием особого фермента, участвующего в химии зрения. Поэтому принятие даже 2 г метанола приводит к слепоте!

Знаете ли вы, что… Ацетальдегид образуется при созревании фруктов и вносит свой вклад в их запах. Ацетальдегид образуется таже дрожжами Sacchromyces cerevisiae. Этим дрожжам позволяют расти на сухом хересе, которому они придают специфический ореховый привкус.

Запомните Для альдегидов (в отличие от спиртов) не характерна изомерия положения функциональной группы. При окислении альдегидов образуются карбоновые кислоты. При восстановлении альдегидов образуются спирты. Качественными реакциями на альдегидную группу являются: а) «реакция серебряного заркала»; б) взаимодействие с гидроксидом меди (II) при нагревании с образованием красного осадка.

Теперь вы знаете Какие вещества относят к альдегидам; Номенклатуру и изомерию альдегидов; Физические и химические свойства альдегидов; Качественные реакции на альдегиды; Получение альдегидов; Применение альдегидов (на примере формальдегида и ацетальдегида).



![Альдегиды образуются при окислении первичных спиртов Н О–Н │ │ СН3–С–ОН + [О] → СН3–С–ОН → │ │ Н Н О → СН3–С + Н2О Н В общем виде: O R–OH + [О] → R–C + Н2О H Альдегиды образуются при окислении первичных спиртов Н О–Н │ │ СН3–С–ОН + [О] → СН3–С–ОН → │ │ Н Н О → СН3–С + Н2О Н В общем виде: O R–OH + [О] → R–C + Н2О H](https://fs3.ppt4web.ru/images/132073/183581/640/img3.jpg)
![Получение альдегидов Окисление спирта перманганатом калия: Спирт + [O] → альдегид + H2O В нашем организме окисление спирта происходит в печени. Получение альдегидов Окисление спирта перманганатом калия: Спирт + [O] → альдегид + H2O В нашем организме окисление спирта происходит в печени.](https://fs3.ppt4web.ru/images/132073/183581/640/img5.jpg)
![При окислении вторичных спиртов образуются кетоны СН3–СН–СН3 + [O] → CH3–C–CH3 + H2O OH O пропанол-2 пропанон-2 (ацетон) Запомните: альдегиды и кетоны содержат карбонильную группу , поэтому их объединяют в группу карбонильных соединений. При окислении вторичных спиртов образуются кетоны СН3–СН–СН3 + [O] → CH3–C–CH3 + H2O OH O пропанол-2 пропанон-2 (ацетон) Запомните: альдегиды и кетоны содержат карбонильную группу , поэтому их объединяют в группу карбонильных соединений.](https://fs3.ppt4web.ru/images/132073/183581/640/img6.jpg)