Презентация на тему: Химия, нефтехимия. Производство неорганических веществ

ХИМИЯ, НЕФТЕХИМИЯ ПРОИЗВОДСТВО НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ

НПЗ вырабатывают: горючие и смазочные материалы, твердые и полужидкие смеси парафинов (парафин, церезин, вазелин), битумы, электродный кокс, растворители, индивидуальные парафиновые, олефиновые (алкены) углеводородыароматические углеводороды.

1. Предварительная стадия обезвоживают, обессоливают, очищают от кокса путем продолжительного отстаивания в подогретом состоянии 180 гр.Своду отделяют термохимическим или электролитическим способом.

2. перегонка НасосТрубчатая печь320 гр.СРектификационная колоннаПары охлаждаются(флегмой)сгущение в конденсаторе БензинЛегроинКеросинЛегкий газоильМазут 275 гр.СТяж. ГазоильВеретенное маслоМашинное маслоЦилиндровое маслоГудрон – твердый осадок

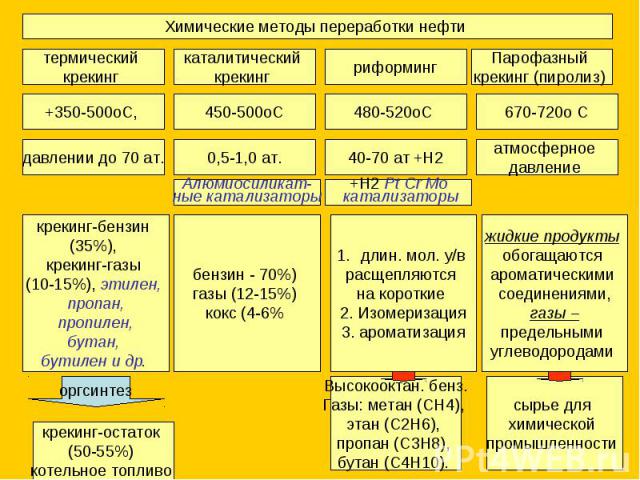
Химические методы переработки нефти
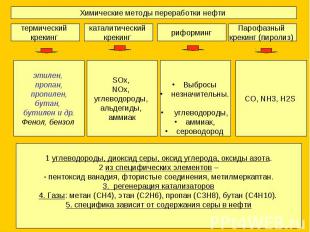
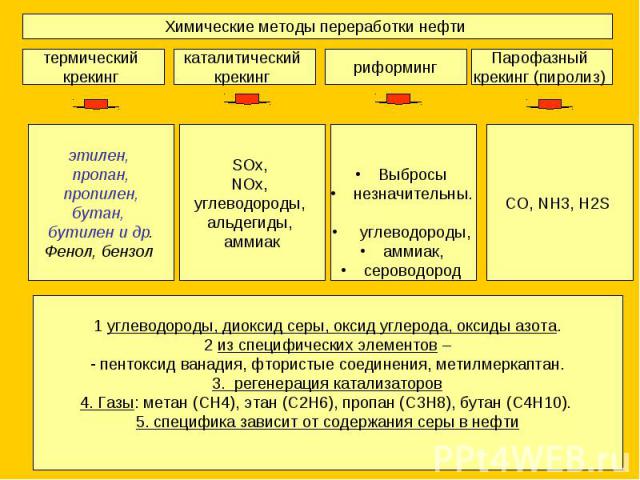
Химические методы переработки нефти 1 углеводороды, диоксид серы, оксид углерода, оксиды азота.2 из специфических элементов – пентоксид ванадия, фтористые соединения, метилмеркаптан.3. регенерация катализаторов4. Газы: метан (СН4), этан (С2Н6), пропан (С3Н8), бутан (С4Н10). 5. специфика зависит от содержания серы в нефти
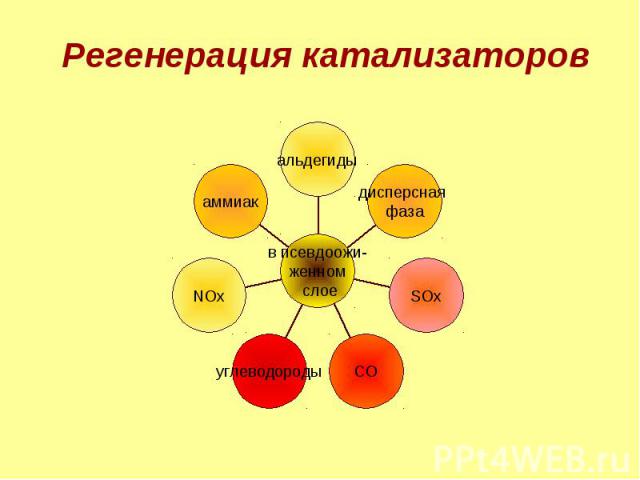
Регенерация катализаторов

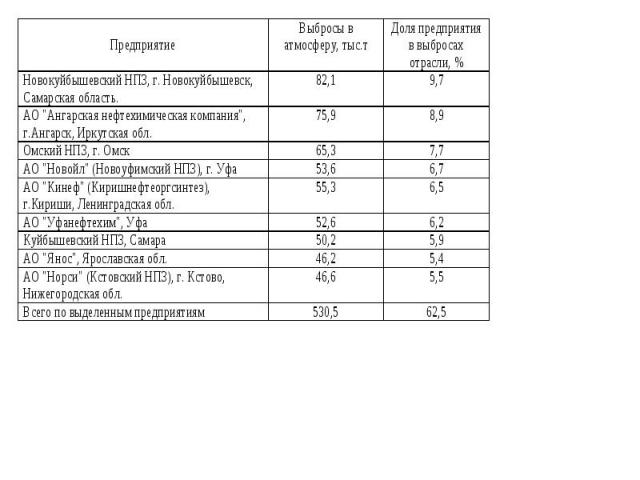
Со сточными водами НПЗ в поверхностные воды поступает нефтепродукты, сульфаты, хлориды, соединения азота, фенолы, соли тяжелых металлов

токсичные отходы состоят из: биологически активного газа, который остается после эксплуатации очистных сооружений, осадков из резервуаров, сернисто-щелочных стоков.

Производство серной кислоты Серная кислота – H2SO4 бесцветная тяжелая маслянистая жидкость, кипящая при 304оС и кристаллизующаяся при 10,4оС.Исходное вещество в производстве серной кислоты является сернистый ангидрид SO2.Для получения SO2. применяется - серный колчедан, - элементарная сера, - сероводородные и сернистые газы, выделяемые при переработке руд цветных и черных металлов, очистке нефти.

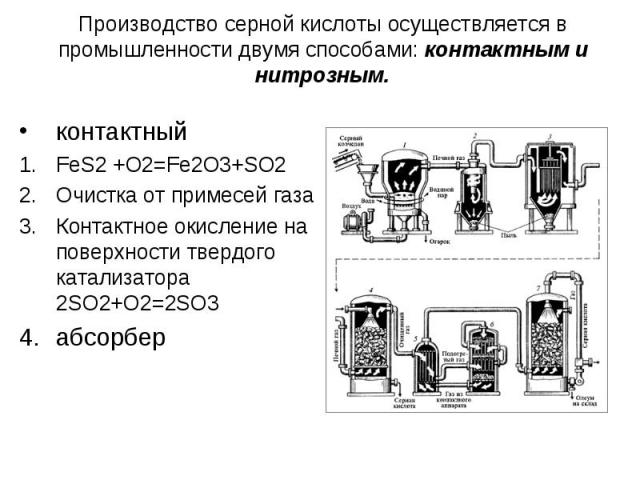
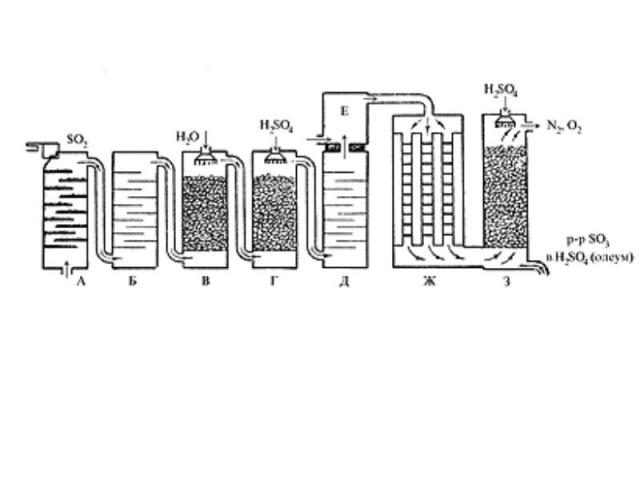
Производство серной кислоты осуществляется в промышленности двумя способами: контактным и нитрозным. контактныйFeS2 +O2=Fe2O3+SO2Очистка от примесей газаКонтактное окисление на поверхности твердого катализатора 2SO2+O2=2SO3абсорбер
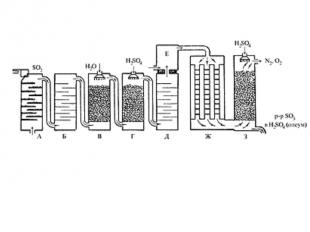

Нитрозный способ – известен с середины 18 в. 1. 2SO2+H2O+NO2=H2SO4+NOОКИСЛИТЕЛЕМ ЯВЛЯЕТСЯ NO2, ОН ВОССТАНАВЛИВАЕТСЯ2. ОКИСЛЕНИЕ КИСЛОРОДОМ ВОЗДУХА 2NO+O2=2NO2До 20-х гг. нашего века он осуществлялся в больших свинцовых камерах, сейчас в специальных башнях

Производство аммиака
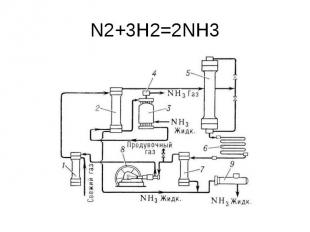
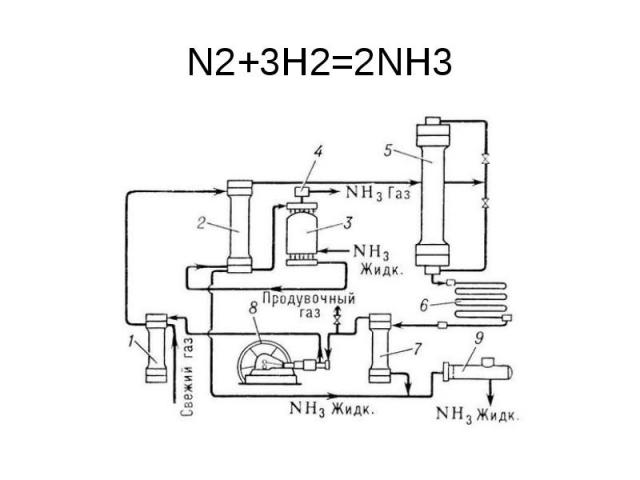
N2+3H2=2NH3

Для получения 1 т NH3 – 3000 куб.м азото-водородной смеси, 90 куб. м воды, 1750 кВт*ч

Производство азотной кислоты

Азотная кислота занимает второе место по объему в производстве кислот после серной.

Исходным веществом для получения азотной кислоты является аммиак – NH3.

Получение слабой азотной кислоты имеет три стадии: 1. окисление аммиака до окиси азота NO; (аммиак и избыток воздуха пропускают над нагретым до 800-900 гр. Pt катализатор4NH3 + 5 O2 = 4 NO + 6 H2O2. окисление оксида азота до двуокиси NO2;2NO + O2 = 2NO23. поглощение NO2 водой с образованием азотной кислоты.3NO2 + H2O = 2HNO3 + NO

Окисление аммиака проводится при температуре 800-900оС в присутствии катализатора, изготовленного из сплава платины и родия.

Кроме платины, могут применяться менее активные катализаторы на основе окиси кобальта или железа с активирующими добавками.

Для получения 1 т разбавленной азотной кислоты в установках с нормальным атмосферным давлением расходуется 300 кг аммиака, 100 м3 воды и 80 кВт.ч электроэнергии.

Выброс HNO3 может составлять до 3 кг на 1 т. в пересчете на 100%-ную кислоту.

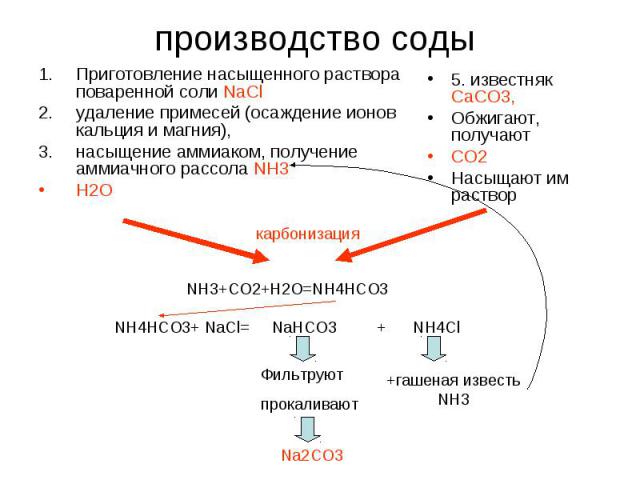
производство соды Приготовление насыщенного раствора поваренной соли NaClудаление примесей (oсаждение ионов кальция и магния), насыщение аммиаком, получение аммиачного рассола NH3H2O5. известняк СаСО3,Обжигают, получают СО2Насыщают им раствор

При получении 1 т соды - образуется около 1 т NH4Cl, раствор которого обрабатывают известковым молоком для регенерации аммиака.Образующуюся дистиллярную жидкость – суспензию нерастворимых соединений в растворе CaCl2 и NaCl направляют в отстойники – шламонакопители. Их называют “белыми морями”. Один только содовый завод может занимать до 3-4 га под шламонакопитель
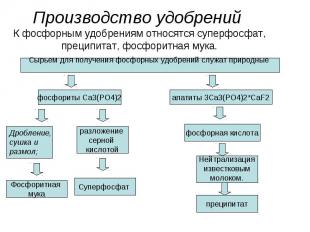
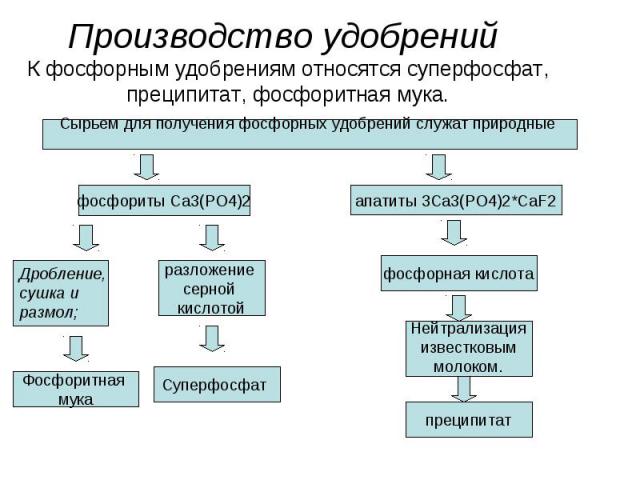
Производство удобрений К фосфорным удобрениям относятся суперфосфат, преципитат, фосфоритная мука.

Главный загрязнитель при производстве фосфорных удобрений – фтористые соединения. Фториды присутствуют как в газообразном состоянии, так и в виде аэрозолей.Нормы выброса фторидов при производстве фосфорных удобрений обычно пропорциональны к количеству P2O5, введенному в производство. Например, в штате Флорида, где производят основную часть фосфорных удобрений, нормируется 1 г фторида на 1 т P2O5, используемого в производстве.

Калийные удобрения это хлорид калия (KCl), сульфат калия (K2SO4) сульфат калия-магния (K2SO4*2MgSO4). Сырьем для получения хлористого калия является сильвинит KCl+NaCl и карналит MgCl2* KCl *6H2O.

Производство калийных удобрений включает:1 отделение хлористого калия от хлорида натрия и глины. 2. Сильвинит размалывают, растворяют, раствор охлаждают, отделяют соли и сушат их.3. если флотируют, обогащая КCl, то образуются галитовые отвалы

В технологии изготовления хлорида калия можно выделить 4 этапа, при которых происходят наиболее существенные выбросы в атмосферу мелких частиц: 1 прессование, 2 дробление, 3 сортировка 4 транспортировка.
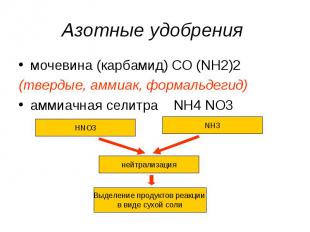
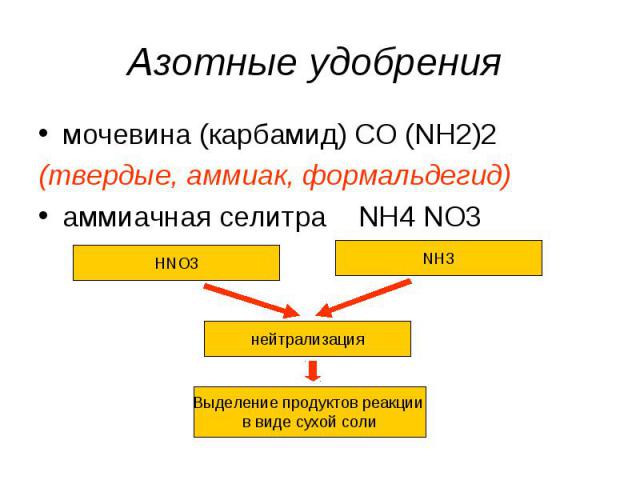
Азотные удобрения мочевина (карбамид) CO (NH2)2(твердые, аммиак, формальдегид)аммиачная селитра NH4 NO3

ядохимикаты Инсектициды:1. парижская зелень 3 Сu(AsO2)2*Cu(CH3COO)2Cырье - As2O3 руды обжигают соли2. Фтористый и кремнефтористый натрий Получают из отходов производст. суперфосфата3. Гексахлоран C6H6Cl6 получается присоединением Cl к бензолу4. ДДТ, тиофос

II. Фунгициды (грибковые заболевания)Бордосская жидкость (медь содерж.)Получается смешиванием медного купороса с известковым молоком2. Серосодержащие (получаются при очистке коксового газа от H2S)3. Формалин4. Гранозан (получается при взаимодействии диэтилртути с сулемой в спиртовом растворе)III. ГербицидыХлор и нитропроизводные фенола

Для производств неорганической химии: 1. в целом 3 основных загрязнителя – SO2, NOx, взвешенные частицы.2. легко испаряющиеся неорганические соединения – Pb, HF, SiF4, HCl и др. галогеноводородные кислоты.3. аммиак – в производстве аммиака, нитрата аммония, фосфата аммония, сульфата аммонияоколо 400 ненормируемых загрязнителей, имеющих широкий диапазон опасных свойств, т.к. называемые некритериальные загрязнителихлорводород – в производстве соляной кислотыфтороводород – в производстве фосфора, фосфорной кислоты.Диоксины - Основными источниками поступления диоксинов в окружающую среду являются хлорфеноловые производства, заводы по производству химических удобрений, полихлорированных бифенилов (ПХБ), массовой хлорной продукции