Презентация на тему: Город металла

Путешествие по городу металлов Andrea Seemann / Shutterstock.com 900igr.net
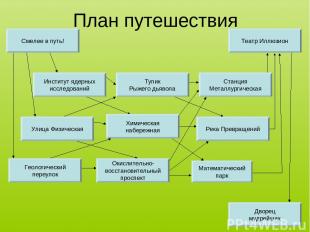
Смелее в путь! Институт ядерных исследований Геологический переулок Улица Физическая Тупик Рыжего дьявола Химическая набережная Река Превращений Станция Металлургическая Театр Иллюзион Окислительно- восстановительный проспект Математический парк Дворец мудрейших План путешествия

Предварительное задание Вычислить степень окисления хрома в K2Cr2O7 Ответ. +6 Фото с сайта http://chemistry-chemists.com Вычислить степень окисления марганца в KMnO4 Ответ. +7 План путешествия

Сравнить строение атомов кальция и магния. У какого элемента сильнее выражены восстановительные свойства? «Институт ядерных исследований» Ответ. Химические элементы кальций и магний расположены во второй группе периодической системы Д.И.Менделеева, поэтому на внешнем электронном слое имеют по 2 электрона. Магний расположен в 3-м периоде, а кальций – в 4-м, радиус атома кальция больше, чем радиус атома магния, а значит и восстановительные свойства кальция выражены сильнее. Фото с сайта http://nucloserv.jinr.ru План путешествия

Перечислите основные физические свойства металлов. Назовите самый пластичный и самый электропроводный металл. «Улица Физическая» Ответ. Металлы обладают пластичностью (ковкостью), тепло- и электропроводностью, имеют металлический блеск. Самый пластичный металл – золото, самый электропроводный металл – серебро. План путешествия

В каком виде металлы встречаются в природе? Назовите самородные металлы. Почему щелочные металлы не встречаются в природе в свободном виде? «Геологический переулок» Ответ. Металлы в природе находятся в виде руд, в водных растворах – в виде солей, а также в самородном виде. В самородном виде встречаются золото, серебро, платина, ртуть. Щелочные металлы имеют высокую химическую активность, реагируют с кислородом воздуха и водой при обычных условиях, поэтому они не могут в природе встречаться в свободном виде. План путешествия

1. Почему коррозию часто называют «рыжим дьяволом»? Какой вред она приносит? «Тупик Рыжего дьявола» Ответ. Продукты коррозии железа имеют красно-коричневый цвет, а вред, приносимый этим процессом, поистине дьявольский, поэтому коррозию и называют «рыжим дьяволом». Ежегодно из-за коррозии теряется около четверти всего производимого в мире железа. Замена и ремонт деталей судов, автомобилей, приборов и коммуникаций требует экономических затрат. Коррозия вызывает серьезные экологические последствия. Например, утечка газа, нефти и других опасных химических продуктов из разрушенных коррозией трубопроводов приводит к загрязнению окружающей среды.

2. Назовите способы защиты от коррозии. (4 способа.) «Тупик Рыжего дьявола» Ответ. Нанесение защитных покрытий (металлических и неметаллических); использование материалов и сплавов, устойчивых к коррозии; протекторная защита (создание контакта с более активным металлом); использование специальных веществ – ингибиторов коррозии.

3. Какое изделие из железа прослужит дольше: оцинкованное или луженое (покрытое оловом)? Объясните, почему? «Тупик Рыжего дьявола» Ответ. Оцинкованное изделие прослужит дольше, т.к. цинк более активный металл по сравнению с железом, – в случае нарушения защитного слоя будет разрушаться именно цинк, сохраняя изделие. Внешний вид изделия ухудшится, но оно останется целым. При нарушении защитного слоя луженого изделия, разрушаться будет железо, т.к. его химическая активность выше, чем у олова. Изделие сохранит красивый внешний вид, но быстро прохудится – в нём образуется дыра. План путешествия

С какими из перечисленных веществ: H2O, Fe, Cl2, KOH, CuO, HCl(г.), K будут реагировать при обычных условиях все три вещества: барий, кальций, магний? «Химическая набережная» Ответ. H2O, Cl2, HCl(г.). При обычных условиях все три металла будут медленно реагировать с хлором и хлороводородом; Ca и Ba будут реагировать с водой (магнию для этого нужно зажечься!). План путешествия

Расставить коэффициенты в уравнениях реакций методом электронного баланса: 1) Ca + O2 → 2) Mg + N2 → 3) Al + Cl2 → «Окислительно-восстановительный проспект» Ответ. План путешествия

1. Как из Cu2O получить медь? 2. Как из Fe3O4 получить железо? 3. Как из ZnO получить цинк? Записать уравнения реакций. «Станция Металлургическая» Ответ. 1) Cu2O + H2 = 2Cu + H2O 2) Fe3O4 + 4H2 = 3Fe + 4H2O 3) 3ZnO + 2Al = 3Zn + Al2О3 Можно использовать ещё углерод и угарный газ. План путешествия

Записать уравнения химических реакций по схемам: Mg → MgO → Mg(NO3)2 → Mg(OH)2 Ca → CaO → CaCl2 → CaCO3 Al → Al2O3 → AlCl3 → Al(OH)3 «Река Превращений» Ответ. 1) 2Mg + O2 = 2MgO MgO + 2HNO3 = Mg(NO3)2 + H2O Mg(NO3)2 + 2NaOH = Mg(OH)2 + 2NaNO3 2) 2Ca + O2 = 2CaO CaO + 2HCl = CaCl2 + H2O CaCl2 + Na2CO3 = CaCO3 + 2NaCl 3) 4Al + 3O2 = 2Al2O3 Al2O3 + 6HCl = 2AlCl3 + 3H2O AlCl3 + 3NaOH = Al(OH)3 + 3NaCl План путешествия

Решите задачи. Вычислить массу NaCl, которую можно получить из натрия массой 4,6 грамма. Вычислить массу CaO, которую можно получить из кальция массой 8 граммов. Вычислить массу MgS, которую можно получить из магния массой 4,8 грамма. «Математический парк» Ответ. 2Na + Cl2 = 2NaCl ν(Na) = 4,6 (г) : 23 (г/моль) = 0,2 моль, ν(NaCl) = ν(Na) = 0,2 моль, m(NaCl) = 0,2 (моль) • 58,5 (г/моль) = 11,7 г 2Ca + O2 = 2CaO ν(Ca) = 8 (г) : 40 (г/моль) = 0,2 моль, ν(CaO) = ν(Ca) = 0,2 моль, m(CaO) = 0,2 (моль) • 56 (г/моль) = 11, 2 г Mg + S = MgS ν(Mg) = 4,8 (г) : 24 (г/моль) = 0,2 моль, ν(MgS) = ν(Mg) = 0,2 моль, m(MgS) = 0,2 (моль) • 56 (г/моль) = 11, 2 г План путешествия

Из имеющихся растворов реактивов FeCl3, CuSO4, BaCl2, Na2CO3, NaOH получите: гидроксид железа(III); гидроксид меди(II); карбонат бария. Запишите уравнения проведенных реакций. «Театр Иллюзион» Ответ. FeCl3 + 3NaOH = Fe(OH)3↓+ 3NaCl CuSO4 + 2NaOH = Cu(OH)2↓ + Na2SO4 BaCl2 + Na2CO3 = BaCO3↓ + 2NaCl План путешествия

1.Записать уравнения реакций в молекулярном и кратком ионном видах: 1) NaOH + HNO3 = 2) KOH + HCl = 3) H2SO4 + BaCl2 = 4) HCl + AgNO3 = 5) CuSO4 + NaOH = «Дворец мудрейших» Ответ. 1) NaOH + HNO3 = NaNO3 + H2O OH- + H+ = H2O 2) KOH + HCl = KCl + H2O OH- + H+ = H2O 3) H2SO4 + BaCl2 = BaSO4↓+ 2HCl SO42- + Ba2+ = BaSO4↓ 4) HCl + AgNO3 = AgCl↓ + HNO3 Cl- + Ag+ = AgCl↓ 5) CuSO4 + 2NaOH = Cu(OH)2↓ + Na2SO4 Cu2+ + 2OH- = Cu(OH)2↓

2. Записать уравнения реакций в кратком ионном видах: 1) Ba(OH)2 + HCl = 2) FeCl3 + KOH = 3) Al(OH)3 + HCl = 4) CaO + HCl = 5) KOH + H2SO4 = «Дворец мудрейших» Ответ. 1) Ba(OH)2 + 2HCl = BaCl2 + 2H2O OH- + H+ = H2O 2) FeCl3 + 3KOH = Fe(OH)3↓ + 3KCl Fe3+ + 3OH- = Fe(OH)3↓ 3) Al(OH)3 + 3HCl = AlCl3 + 3H2O Al(OH)3 + 3H+ = Al3+ + 3H2O 4) CaO + 2HCl = CaCl2 + H2O CaO + 2H+ = Ca2+ + H2O 5) 2KOH + H2SO4 = K2SO4 + 2H2O OH- + H+ = H2O

3. Записать уравнения реакций в кратком ионном видах: 1) CaCl2 + AgNO3 = 2) NaOH + HCl = 3) CuCl2 + KOH = 4) Ba(NO3)2 + Na2SO4 = 5) Mg(OH)2 + HNO3 = «Дворец мудрейших» Ответ. 1) CaCl2 + 2AgNO3 = 2AgCl↓ + Ca(NO3)2 Cl- + Ag+ = AgCl↓ 2) NaOH + HCl = NaCl + H2O OH- + H+ = H2O 3) CuCl2 + 2KOH = Cu(OH)2↓ + 2KCl Cu2+ + 2OH- = Cu(OH)2↓ 4) Na2SO4 + Ba(NO3)2 = BaSO4↓+ 2NaNO3 SO42- + Ba2+ = BaSO4↓ 5) Mg(OH)2 + 2HNO3 = Mg(NO3)2 + 2H2O Mg(OH)2 + 2H+ = Mg2+ + 2H2O План путешествия

Спасибо за внимание!