Презентация на тему: Общие сведения о металлах

Химия металлов Занятие №1 «Общие сведения о металлах»

Особенности электронного строения атомов металлов

Положение металлов в ПСХЭ

Закономерности в изменении свойств элементов – металлов.
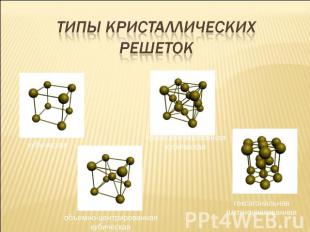
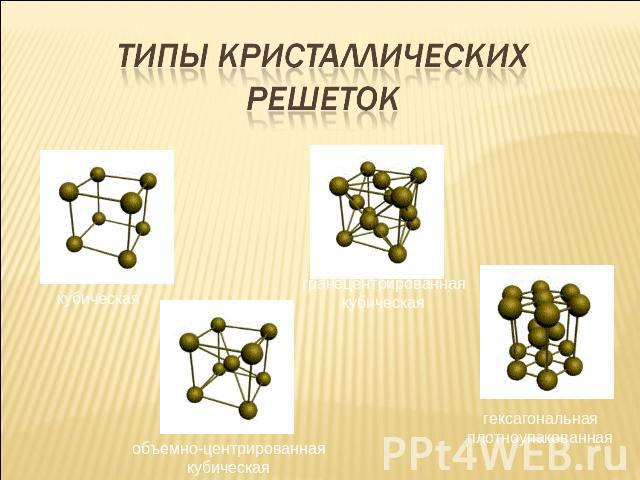
Типы кристаллических решеток

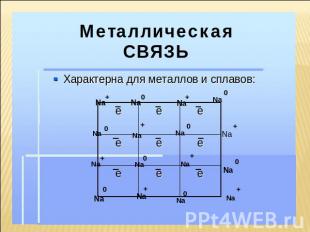
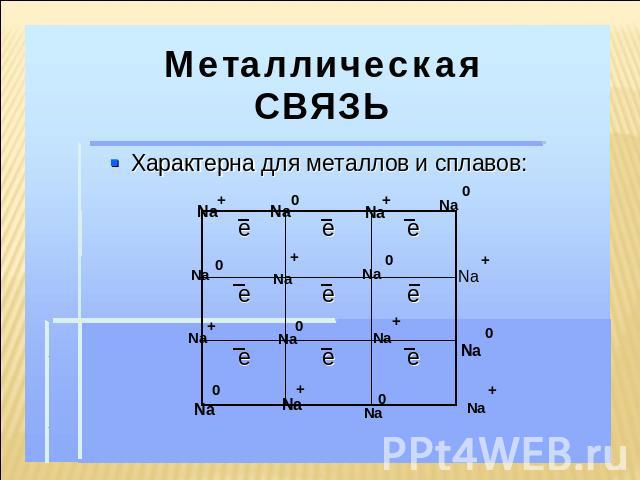
Характеристика металлической связи сравнительно небольшое количество электронов одновременно связывают множество ядер, связь делаколизована; валентные электроны свободно перемещаются по всему куску металла, который в целом электронейтрален; металлическая связь не обладает направляемостью и насыщенностью.

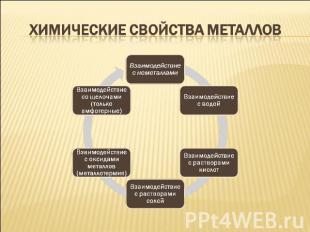
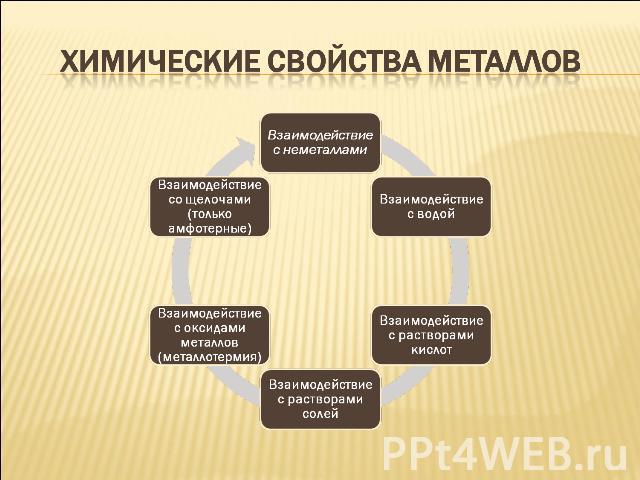
Химические свойства металлов

Взаимодействие с неметаллами (в названиях полученных веществ окончание -иды) 2Mg0+O20—>2Mg2+O2- (оксид магния) Mg0-2e– —>Mg2+ │2 восстановитель 2O0+4e– —>2O2– 1 окислитель Fe0+S0—>Fe2+S2- (сульфид железа II) Fe0-2e– —>Fe2+ 1 восстановитель S0+2e– —>S2– 1 окислитель

Взаимодействие с водой. Самые активные металлы реагируют с водой при обычных условиях, и в результате этих реакций образуются растворимые в воде основания и выделяется водород 2Li0+2H2+O2– —> 2Li+O2-H+ + H20 Li0-1e– —>Li+ 2 восстановитель 2H++2e– —>2H0 1 окислитель Менее активные металлы реагируют с водой при повышенной температуре с выделением водорода и образованием оксида соответствующего металла Zn + H2O = ZnO +H2

Взаимодействие с растворами кислот Происходит при соблюдении ряда условий: Металл должен находиться левее в ряду напряжений металлов; В результате реакции должна образовываться растворимая соль, иначе металл покроется осадком и доступ кислоты к металлу прекратиться; Для этих реакций не рекомендуется использовать щелочные металлы, так как они взаимодействуют с водой в растворе кислоты; По особому взаимодействуют с металлами концентрированные азотная и серная кислоты; 2H+Cl– +Zn0 → Zn2+Cl2- +H20

Взаимодействие с растворами солей При этом соблюдаются следующие условия: Металл должен находиться в ряду напряжений левее металла, образующего соль; В результате реакции должна образовываться растворимая соль, иначе металл покроется осадком и доступ кислоты к металлу прекратиться; Для этих реакций не рекомендуется использовать щелочные металлы, так как они взаимодействуют с водой в растворе соли; Fe0+Cu2+Cl2– →Fe2+Cl2– +Cu0
![Взаимодействие со щелочами (только амфотерные) Be + 2NaOH + 2H2O = Na2[Be(OH)4] Взаимодействие со щелочами (только амфотерные) Be + 2NaOH + 2H2O = Na2[Be(OH)4]](/images/150/8752/310/img13.jpg)
Взаимодействие со щелочами (только амфотерные) Be + 2NaOH + 2H2O = Na2[Be(OH)4] + H2 Магний и щелочноземельные металлы с щелочами не реагируют.

Взаимодействие с оксидами металлов (металлотермия) Некоторые активные металлы способны вытеснять другие металлы из их оксидов при поджигании смеси. 2Al0 + Fe2O3 = Al2O3 +2Fe0

Способы получения металлов

Пирометаллургия из их оксидов углем или оксидом углерода (II)ZnО + С = Zn + СО Fе2О3 + ЗСО = 2Fе + ЗСО2 водородомWO3 + 3H2 =W + 3H2OСоО + Н2 = Со + Н2О алюминотермия 4Аl + ЗМnО2 = 2А12О3 + ЗМn

Гидрометаллургия CuO + H2SO4 = CuSO4 + H2O, CuSO4 + Zn = ZnSO4 + Cu.

Электрометаллургия СuСl2 → Сu2+ 2Сl-Катод(восстановление): Сu2+ - 2е- = Сu0 Анод (окисление): 2Cl- - 2е- = Сl°2

Значение металлов Человек использовал металлы и сплавы с древних времен для изготовлений орудий труда. В история человечества выделяют медный век, бронзовый и железный, который продолжается и в настоящее время. Ведь в настоящее время железные сплавы составляют почти 90% всего количества металлов и металлических сплавов.

Сплавы

роль металлов в организме человека

Задание для самостоятельной работы Напишите уравнения реакций взаимодействия между веществами: а) Li, Na, Ca, Fe c O2, Cl2, S, N2, C: б) Na, Ca, Al c H2O; в) Zn c H2SO4; Al c HCl; г) Zn c CuSO4; Al c NaOH; Be c KOH.

Задание для самостоятельной работы Решите задачу: Смесь порошков железа и меди массой 10 г обработали раствором НСl, при этом выделился газ объёмом 2,24 л. Определите массовую долю металлов в смеси.

Химический диктант Вопросы: 1. Сколько электронов у элементов металлов на внешнем слое? 2. Тип химической связи в металлах? 3. Какие подвижные частицы кристаллической решетки обеспечивают физические свойства металлов? 4. Самый легкий металл? 5. Лучшие проводники электричества среди металлов? 6. В химических реакциях металлы выполняют роль восстановителей или окислителей? 7. Способ получения металлов из их соединений при высоких температурах с помощью различных восстановителей? 8. Важнейшие сплавы на основе железа? 9.Получение металлов из растворов и расплавов при пропускании электрического тока? 10. Способ получения металлов из их оксидов при взаимодействии с алюминием?

Напишите уравнения реакции соответствующие схеме, продукты реакции назовите

Расставить коэффициенты, найти окислитель и восстановитель в уравнениях реакций: Cu + HNO3 (P) → Cu (NO3)2 + NO + H2O Cu + HNO3 (K) → Cu (NO3)2 + NO2 + H2O Na + HNO3 → NaNO3 + N2O + H2O











![Взаимодействие со щелочами (только амфотерные) Be + 2NaOH + 2H2O = Na2[Be(OH)4] + H2 Магний и щелочноземельные металлы с щелочами не реагируют. Взаимодействие со щелочами (только амфотерные) Be + 2NaOH + 2H2O = Na2[Be(OH)4] + H2 Магний и щелочноземельные металлы с щелочами не реагируют.](/images/150/8752/640/img13.jpg)
























