Презентация на тему: «Фосфор».

Фосфор Гафарова Алфинур Замилевна Учитель химии МБОУ «Елховская СОШ» Альметьевского муниципального района Республики Татарстан

ФОСФОР Общая характеристика фосфора. Рассмотрение аллотропных видоизменений фосфора. Изучение химических свойств фосфора. Углубление и систематизация знаний периодического закона и системы химических элементов на примере строения и свойств простых веществ, образованных фосфором

История Фосфор открыт гамбургским алхимиком Хеннигом Брандом в 1669 году. Подобно другим алхимикам, Бранд пытался отыскать филосовский камень, а получил светящееся вещество. Бранд сфокусировался на опытах с человеческой мочой, так как полагал, что она, обладая золотистым цветом, может содержать золото или нечто нужное для его добычи.
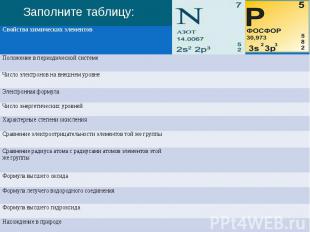
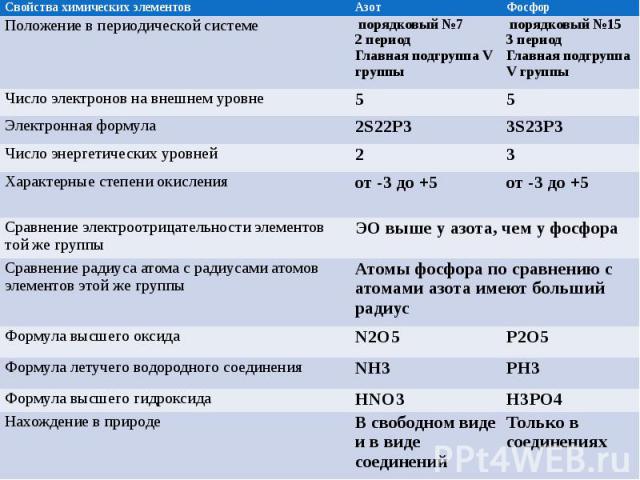
Заполните таблицу:
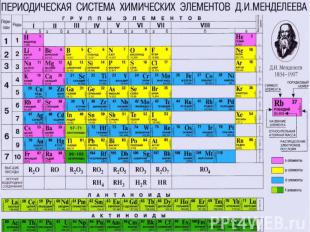
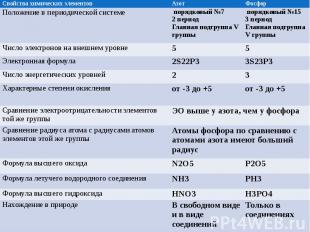

Сравнение фосфора и азота еще один представитель главной подгруппы V группы периодической системы, Так как в атоме фосфора электронных слоев больше, чем в атоме азота, по сравнению с азотом атомы фосфора имеют больший радиус. Ядро фосфора будет слабее притягивать внешний электрон, чем ядро атома азота, отсюда меньшее значение электроотрицательности, а значит, более выраженные восстановительные свойства. Фосфор проявляет степени окисления -3, +3, +5. Самые устойчивые соединения со степенью окисления +5.

Нахождение в природе и организме В свободном состоянии в природе не встречаются вследствие легкой окисляемости фосфора. Природные минералы – фосфорит Сa3(РО4)2, апатит – Сa3(РО4)2•СaCI2 или Сa3(РО4)2•СaF2. Зубная эмаль, представляющая собой в соответствии со своими функциями самое твёрдое из веществ, тот же самый апатит. В растениях фосфор сосредотачивается главным образом в семенах и плодах, в организме животных, птиц и рыб – в скелете и нервной ткани. В среднем тело человека содержится около 1,5 кг фосфора, из которых около 1,4 кг приходится на кости. Если бы фосфор исчез из костей, наше тело превратилось бы в бесформенные массы. Если бы фосфор исчез из мышц, мы утратили бы способность двигаться, из нервной ткани – мы перестали бы мыслить. Академик А.Е. Ферсман назвал фосфор “элементом жизни и мысли”.
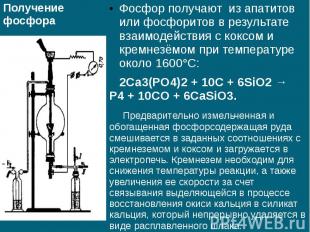
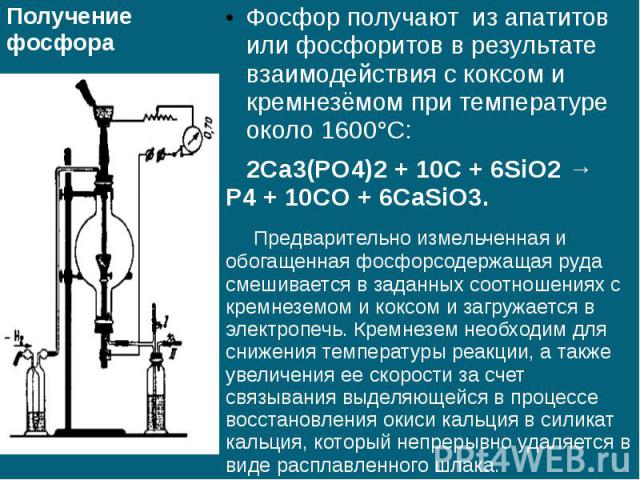
Получение фосфора Фосфор получают из апатитов или фосфоритов в результате взаимодействия с коксом и кремнезёмом при температуре около 1600°С: 2Ca3(PO4)2 + 10C + 6SiO2 → P4 + 10CO + 6CaSiO3. Предварительно измельченная и обогащенная фосфорсодержащая руда смешивается в заданных соотношениях с кремнеземом и коксом и загружается в электропечь. Кремнезем необходим для снижения температуры реакции, а также увеличения ее скорости за счет связывания выделяющейся в процессе восстановления окиси кальция в силикат кальция, который непрерывно удаляется в виде расплавленного шлака.

Аллотропия- явление, когда один и то же химический элемент образует несколько простых веществ
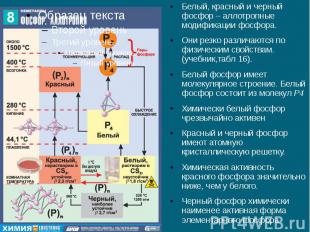
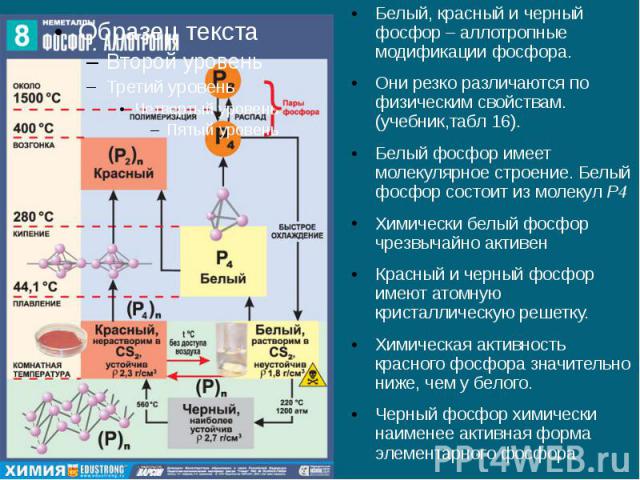
Белый, красный и черный фосфор – аллотропные модификации фосфора. Белый, красный и черный фосфор – аллотропные модификации фосфора. Они резко различаются по физическим свойствам. (учебник,табл 16). Белый фосфор имеет молекулярное строение. Белый фосфор состоит из молекул P4 Химически белый фосфор чрезвычайно активен Красный и черный фосфор имеют атомную кристаллическую решетку. Химическая активность красного фосфора значительно ниже, чем у белого. Черный фосфор химически наименее активная форма элементарного фосфора

Химические свойства фосфора Химические свойства белого и красного фосфора близки, но белый фосфор химически более активен. Белый фосфор самовоспламеняется на воздухе, а красный горит при поджигании: 4P + 5O2 → 2P2O5 (с избытком кислорода), 4P + 3O2 → 2P2O3 (при медленном окислении или при недостатке кислорода). При взаимодействии с металлами образуются фосфиды: 3Ca + 2P = Ca3P2. С водородом фосфор не реагирует, но при разложении водой или кислотами фосфидов образуется фосфин PH3 — ядовитый газ с неприятным запахом: Ca3P2 + 6HCl = 3CaCl2 + 2PH3 ↑. Ca3P2 + 6H2O = 3Ca(OH)2 + 2PH3 ↑ Свойства фосфина - PH3 + 2O2 = H3PO4. PH3 + HI = PH4I .

С неметаллами — восстановитель: С неметаллами — восстановитель: 2P + 3S → P2S3, 2P + 3Cl2 → 2PCl3. Сильные окислители превращают фосфор в фосфорную кислоту: 3P + 5HNO3 + 2H2O → 3H3PO4 + 5NO; 2P + 5H2SO4 → 2H3PO4 + 5SO2 + 2H2O. Реакция окисления также происходит при поджигании спичек, в качестве окислителя выступает бертолетова соль: 6P + 5KClO3 → 5KCl + 3P2O5 В холодных концентрированных растворах щелочей медленно протекает реакция диспропорционирования: 4P + 3KOH + 3H2O = PH3 + 3KH2PO3
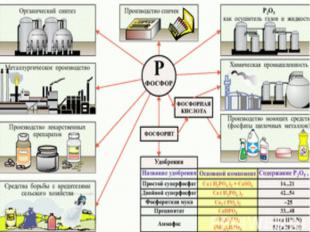

Осуществите превращения: Осуществите превращения Ca3(PO4)2 1 P 2 P2O5 Ca3P2 3 PH3 4 P2O5 Для уравнений 1,2,4 составьте электронный баланс, укажите окислитель и восстановитель.