Презентация на тему: Кислородсодержащие органические соединения




К кислородсодержащим органическим соединениям относят многочисленные органические соединения, как природного происхождения, так и синтетические, являющиеся производными углеводородов, в молекулах которых содержатся углеродные атомы, непосредственно связанные с кислородом. К кислородсодержащим органическим соединениям относят многочисленные органические соединения, как природного происхождения, так и синтетические, являющиеся производными углеводородов, в молекулах которых содержатся углеродные атомы, непосредственно связанные с кислородом. В органических кислородсодержащих веществах кислород в соединении с углеродом образует различные группы, в которых углерод затрачивает на соединении с атомами кислорода одну, две или три валентные связи:

Остальные валентности углерода могут участвовать в образовании связи либо с углеродными атомами, либо с атомами водорода или других элементов. Остальные валентности углерода могут участвовать в образовании связи либо с углеродными атомами, либо с атомами водорода или других элементов. Таким образом, приведённые кислородсодержащие группы, можно представить как различные стадии окисления углеродных атомов в органических молекулах; эти группы связаны между собой так же, как и соединения, в состав которых они входят, взаимными окислительно-восстановительными превращениями. Гидроксильная группа содержится в спиртах, карбонильная – в альдегидах и кетонах, карбоксильная – в карбоновых кислотах.

Производные углеводородов, представляющие собой продукты замещения атома водорода в углеводородной молекуле водным остатком, т.е. гидроксильной группой – OH, называют спиртами. Эти вещества можно рассматривать и как производные воды, в молекуле которой один атом водорода замещён углеводородным радикалом R. Это можно представить схемой: Производные углеводородов, представляющие собой продукты замещения атома водорода в углеводородной молекуле водным остатком, т.е. гидроксильной группой – OH, называют спиртами. Эти вещества можно рассматривать и как производные воды, в молекуле которой один атом водорода замещён углеводородным радикалом R. Это можно представить схемой:

Спирты могут содержать и несколько гидроксильных групп но при разных атомах углерода. Число их характеризует атомность спирта. В соответствии с этим спирты бывают одноатомные и многоатомные; последние подразделяются на двухатомные, трёхатомные и т.д. спирты. Спирты могут содержать и несколько гидроксильных групп но при разных атомах углерода. Число их характеризует атомность спирта. В соответствии с этим спирты бывают одноатомные и многоатомные; последние подразделяются на двухатомные, трёхатомные и т.д. спирты.

Изомерия предельных одноатомных спиртов, общая формула которых CnH2n+1OH, обусловлена изомерией углеродного скелета и изомерией положения гидроксильной группы. Изомерия предельных одноатомных спиртов, общая формула которых CnH2n+1OH, обусловлена изомерией углеродного скелета и изомерией положения гидроксильной группы. Спирту состава C3H7OH соответствует два изомера по положению гидроксильной группы:

Из бутана и изобутана могут быть произведены четыре изомерных бутиловых спирта. Из бутана и изобутана могут быть произведены четыре изомерных бутиловых спирта. В зависимости от положения гидроксильной группы при первичном, вторичном и третичном углеродном атоме спирты могут быть первичными, вторичными и третичными:

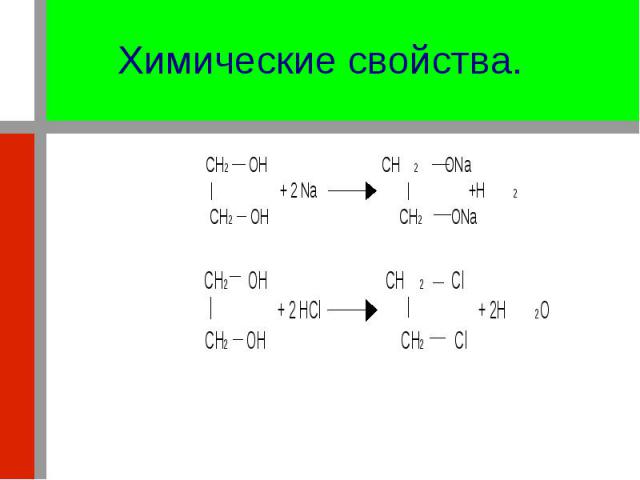
Химические свойства спиртов обусловлены наличием гидроксильной группы. В разнообразных химических превращениях спиртов особая роль принадлежит двум типам реакций: Химические свойства спиртов обусловлены наличием гидроксильной группы. В разнообразных химических превращениях спиртов особая роль принадлежит двум типам реакций: разрыву связи между атомами C и O (1), O и H(2). Положение гидроксильной группы существенно влияет на её поведение в этих превращениях.

Атомы водорода гидроксильных групп в спиртах проявляют определённую подвижность. Подобно воде, спирты реагируют со щелочными металлами, которые замещают водород спиртовых гидроксильных групп; при этом образуются алкоголяты и выделяется водород: Атомы водорода гидроксильных групп в спиртах проявляют определённую подвижность. Подобно воде, спирты реагируют со щелочными металлами, которые замещают водород спиртовых гидроксильных групп; при этом образуются алкоголяты и выделяется водород:

По мере увеличения числа углеродных атомов в углеводородных радикалах спиртов активность последних в этой реакции всё более уменьшается. По мере увеличения числа углеродных атомов в углеводородных радикалах спиртов активность последних в этой реакции всё более уменьшается. Высшие спирты реагируют с натрием лишь при нагревании. Первичные спирты значительно активнее в реакциях со щелочными металлами, чем изомерные им вторичные и особенно третичные. В реакции со щелочными металлами спирты проявляют свойства кислот; но в результате влияния, оказываемого на гидроксильную группу алкильным радикалом, спирты – ещё более слабые кислоты, чем вода. Практически спирты – нейтральные вещества: они не показывают ни кислой, ни щелочной реакции на лакмус, не проводят электрический ток.

Кислород воздуха окисляет спирты только при высокой температуре; при этом они горят. В результате происходит полное разрушение молекул с образованием оксида углерода(IV) и воды.Возможно и умеренное окисление спиртов: при этом они окисляются легче, чем соответствующие предельные углеводороды. Углеводороды на холоду не взаимодействуют с раствором перманганата калия или хромовой смесью, спирты же окисляются ими.Внешне реакция проявляется в том, что в случае перманганата калия (KMnO4) исчезает его фиолетовая окраска, а в случае хромовой смеси (K2Cr2O7+H2SO4) её оранжевый цвет переходит в зеленый. Кислород воздуха окисляет спирты только при высокой температуре; при этом они горят. В результате происходит полное разрушение молекул с образованием оксида углерода(IV) и воды.Возможно и умеренное окисление спиртов: при этом они окисляются легче, чем соответствующие предельные углеводороды. Углеводороды на холоду не взаимодействуют с раствором перманганата калия или хромовой смесью, спирты же окисляются ими.Внешне реакция проявляется в том, что в случае перманганата калия (KMnO4) исчезает его фиолетовая окраска, а в случае хромовой смеси (K2Cr2O7+H2SO4) её оранжевый цвет переходит в зеленый.

Большая склонность спиртов к окислению по сравнению с углеводородами объясняется влиянием имеющейся в их молекулах гидроксильной группы. Молекулы спиртов содержат углеродные атомы, как бы уже подвергшиеся окислению, т.е. связанные с кислородом гидроксида, и поэтому действие окислителя прежде всего направляется на спиртовую группу. При этом окислению легче подвергаются спирты, в которых при углероде спиртовой группы имеется водород, - первичные и вторичные. Большая склонность спиртов к окислению по сравнению с углеводородами объясняется влиянием имеющейся в их молекулах гидроксильной группы. Молекулы спиртов содержат углеродные атомы, как бы уже подвергшиеся окислению, т.е. связанные с кислородом гидроксида, и поэтому действие окислителя прежде всего направляется на спиртовую группу. При этом окислению легче подвергаются спирты, в которых при углероде спиртовой группы имеется водород, - первичные и вторичные.
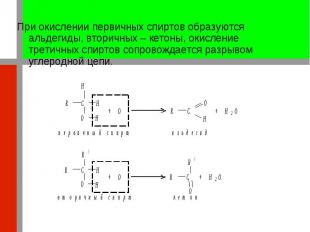
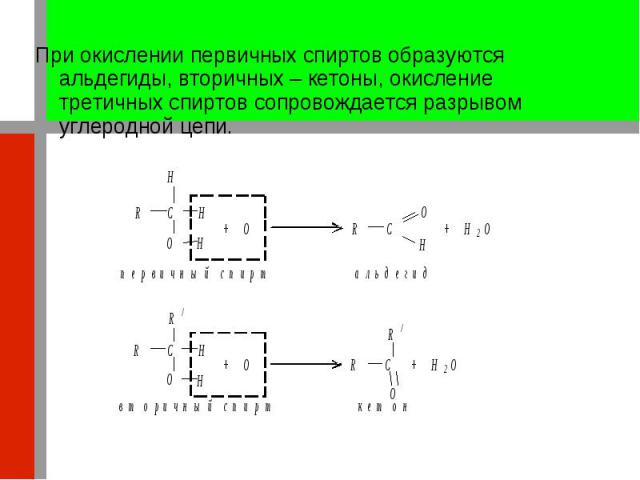
При окислении первичных спиртов образуются альдегиды, вторичных – кетоны, окисление третичных спиртов сопровождается разрывом углеродной цепи. При окислении первичных спиртов образуются альдегиды, вторичных – кетоны, окисление третичных спиртов сопровождается разрывом углеродной цепи.

Дегидратация (отнятие воды от молекулы спирта) приводит к образованию этиленовых углеводородов или простых эфиров. При избытке спирта дегидратация протекает межмолекулярно, что приводит к образованию простого эфира: Дегидратация (отнятие воды от молекулы спирта) приводит к образованию этиленовых углеводородов или простых эфиров. При избытке спирта дегидратация протекает межмолекулярно, что приводит к образованию простого эфира:

Внутримолекулярная дегидратация, т.е. за счёт одной молекулы спирта, приводит к образованию этиленового углеводорода: Внутримолекулярная дегидратация, т.е. за счёт одной молекулы спирта, приводит к образованию этиленового углеводорода:

Взаимодействие спиртов с кислотами (органическими и неорганическими) приводит к образованию производных кислот, называемых сложными эфирами: Взаимодействие спиртов с кислотами (органическими и неорганическими) приводит к образованию производных кислот, называемых сложными эфирами: Эта реакция называется реакцией этерификации.

Гидролиз галогеналканов. Гидролиз галогеналканов. При действии на галогеналкилы воды в присутствии щелочей происходит реакция гидролиза, в результате которой галоген замещается гидроксилом с образованием спирта и галогеноводородной кислоты.

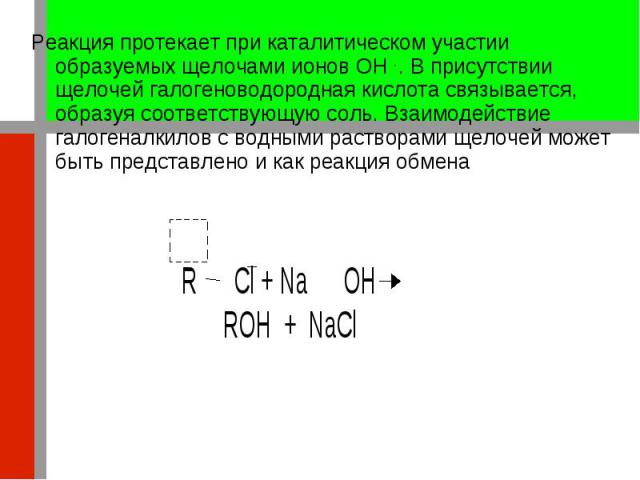
Реакция протекает при каталитическом участии образуемых щелочами ионов OH - . В присутствии щелочей галогеноводородная кислота связывается, образуя соответствующую соль. Взаимодействие галогеналкилов с водными растворами щелочей может быть представлено и как реакция обмена Реакция протекает при каталитическом участии образуемых щелочами ионов OH - . В присутствии щелочей галогеноводородная кислота связывается, образуя соответствующую соль. Взаимодействие галогеналкилов с водными растворами щелочей может быть представлено и как реакция обмена

Таким образом, при действии водного раствора щелочи на галогеналкилы образуются спирты. Например: Таким образом, при действии водного раствора щелочи на галогеналкилы образуются спирты. Например:
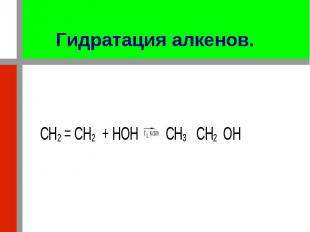
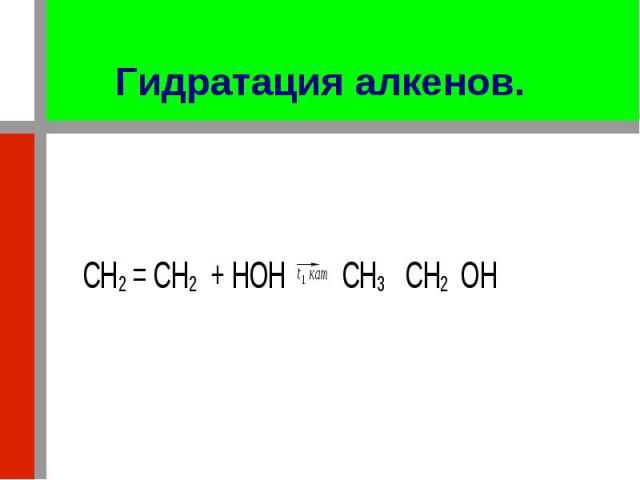
При нагревании в присутствии катализаторов (хлорид цинка, серная кислота) элементы воды (водород и гидроксил) присоединяются к углеродным атомам по месту двойной связи с образованием спиртов При нагревании в присутствии катализаторов (хлорид цинка, серная кислота) элементы воды (водород и гидроксил) присоединяются к углеродным атомам по месту двойной связи с образованием спиртов

С гомологоми этилена реакция протекает по правилу Марковникова. С гомологоми этилена реакция протекает по правилу Марковникова. Например:

При действии водорода в момент выделения (H) на карбонильные соединения альдегиды восстанавливаются в первичные спирты, а кетоны – во вторичные: При действии водорода в момент выделения (H) на карбонильные соединения альдегиды восстанавливаются в первичные спирты, а кетоны – во вторичные: альдегид кетон первичный спирт вторичный спирт

Некоторые спирты получают характерными только для них способами. Так, метанол в промышленности получают при взаимодействии водорода с оксидом углерода (II) при повышенном давлении и высокой температуре на поверхности катализатора: Некоторые спирты получают характерными только для них способами. Так, метанол в промышленности получают при взаимодействии водорода с оксидом углерода (II) при повышенном давлении и высокой температуре на поверхности катализатора: синтез газ - метанол

Синтез газ получают при пропускании паров воды над раскаленным углем: Синтез газ получают при пропускании паров воды над раскаленным углем: Этанол (этиловый спирт) в промышленности получают при спиртовом брожении глюкозы
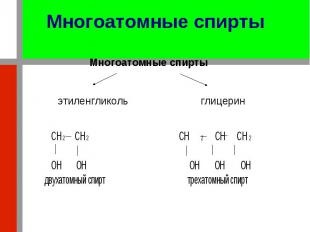
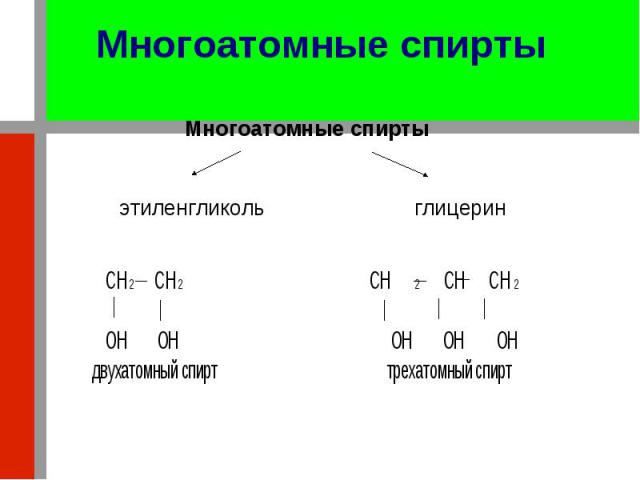
Многоатомные спирты Многоатомные спирты этиленгликоль глицерин
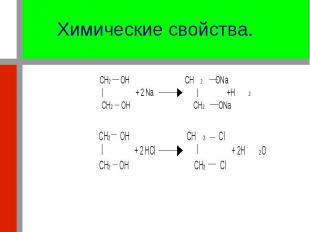
1. Реагируют со щелочными металлами: 1. Реагируют со щелочными металлами: 2. Реагируют с галогеноводородами:

3. Реагируют с кислотами, образуя сложные эфиры: 3. Реагируют с кислотами, образуя сложные эфиры: 4. Реагируют с гидроксидом меди (II) – качественная реакция на многоатомные спирты (ярко-синее окрашивание раствора)