Презентация на тему: Аммиак: состав, строение, свойства, применение

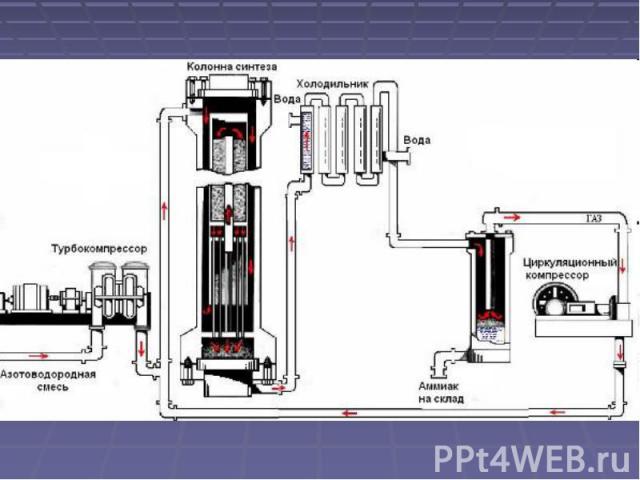
Аммиак: состав, строение, свойства, применение

История названия Аммиак (в европейских языках его название звучит как «аммониак») своим названием обязан оазису Аммона в Северной Африке, расположенному на перекрестке караванных путей. В жарком климате мочевина (NH2)2CO, содержащаяся в продуктах жизнедеятельности животных, разлагается особенно быстро. Одним из продуктов разложения и является аммиак. По другим сведениям, аммиак получил своё название от древнеегипетского слова амониан. Так называли людей, поклоняющихся богу Амону. Они во время своих ритуальных обрядов нюхали нашатырь NH4Cl, который при нагревании испаряет аммиак.

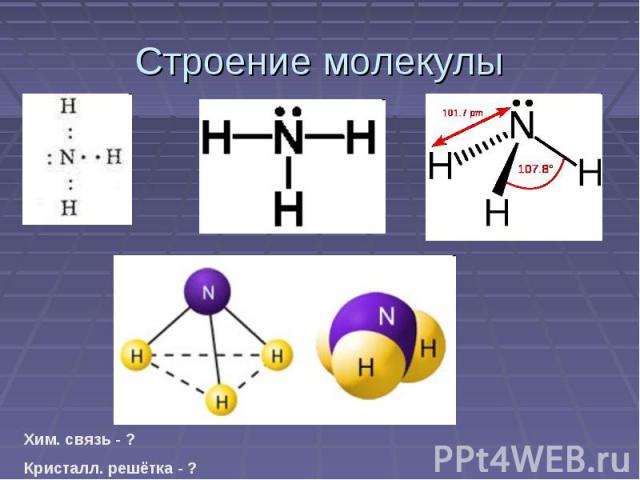
Состав молекулыNH3 или H3N
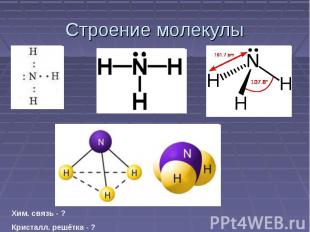
Строение молекулы Хим. связь - ?Кристалл. решётка - ?
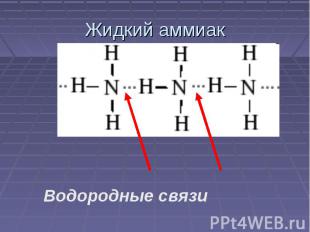
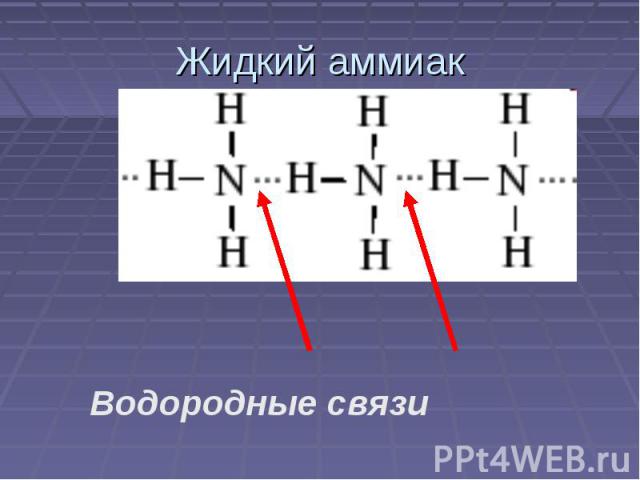
Жидкий аммиак Водородные связи

Физические свойства (при н.у. ) бесцветный газ с резким характерным запахом (запах нашатырного спирта)легче воздуха (М=17 г/моль)хорошо растворяется в воде (1200 объёмов (при 0 °C) и 700 объёмов (при 20 °C) в объёме водыТемпература плавления-77.73 °CТемпература кипения-33.34 °CТоксичен!

Токсикология Относится к группе веществ удушающего и нейротропного действия, способных при ингаляционном поражении вызвать токсический отёк лёгких и тяжёлое поражение нервной системы. Аммиак обладает как местным, так и резорбтивным действием.Пары аммиака сильно раздражают слизистые оболочки глаз и органов дыхания, а также кожные покровы. Пары аммиака вызывают обильное слезотечение, боль в глазах, химический ожог конъюнктивы и роговицы, потерю зрения, приступы кашля, покраснение и зуд кожи. При соприкосновении сжиженного аммиака и его растворов с кожей возникает жжение, возможен химический ожог с пузырями, изъязвлениями. Кроме того, сжиженный аммиак при испарении поглощает тепло, и при соприкосновении с кожей возникает обморожение различной степени. Запах аммиака ощущается при концентрации 37 мг/м³.ПДК в воздухе рабочей зоны производственного помещения составляет 20 мг/м³. Следовательно, если чувствуется запах аммиака, то работать без средств защиты уже опасно. ПДК в атмосферном воздухе населённых пунктов равна: среднесуточная 0,04 мг/м³; максимальная разовая 0,2 мг/м³.В мире максимальная концентрация аммиака в атмосфере (больше 1 мг/м³) наблюдается на Индо-Гангской равнине, в Центральной долине США и в Южно-Казахстанской области.

Аммиак является конечным продуктом азотистого обмена в организме человека и животных. Он образуется при метаболизме белков, аминокислот и других азотистых соединений. Большая часть аммиака конвертируется печенью в более безвредное и менее токсичное соединение — карбамид (мочевину). Мочевина затем выводится почками, причём часть мочевины может быть конвертирована печенью или почками обратно в аммиак.Аммиак может также использоваться печенью для обратного процесса — ресинтеза аминокислот из аммиака и кетоаналогов аминокислот. Этот процесс носит название «восстановительное аминирование».
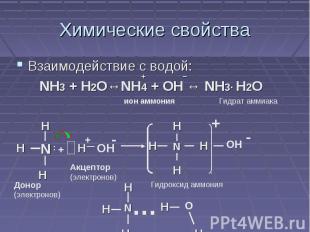
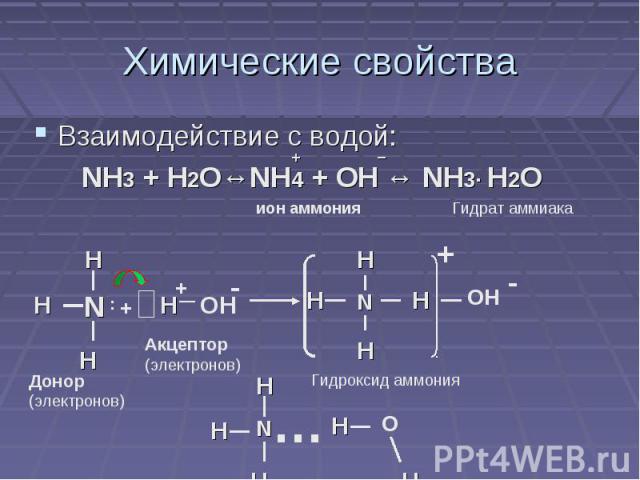
Химические свойства Взаимодействие с водой: NH3 + H2O↔NH4 + OH ↔ NH3· H2O Донор (электронов) Акцептор (электронов) Гидроксид аммония
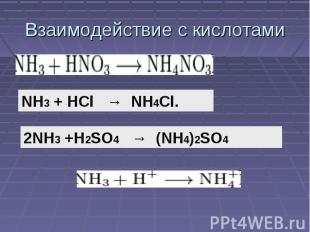
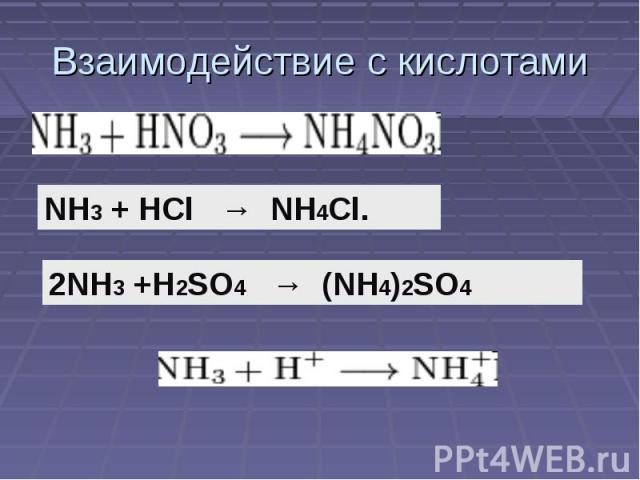
Взаимодействие с кислотами NH3 + HCl → NH4Cl. 2NH3 +H2SO4 → (NH4)2SO4

Восстановительные свойства 4NH3+ 3O2= 2N2+ 6H2O

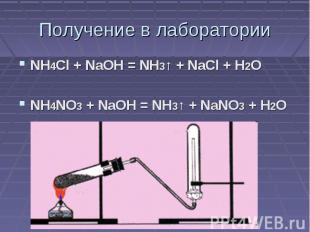
Получение в лаборатории NH4Cl + NaOH = NH3↑ + NaCl + H2ONH4NO3 + NaOH = NH3↑ + NaNO3 + H2O

Интересные факты Пары нашатырного спирта способны изменять окраску цветов. Например, голубые и синие лепестки становятся зелеными, ярко красные — черными.Облака Юпитера состоят из аммиака.Некоторые цветы, не имеющие запаха от природы, после обработки аммиаком начинают благоухать. Например, приятный аромат приобретают астры.