Презентация на тему: Закон постоянства состава

Муниципальное бюджетное образовательное учреждение Изыхская средняя общеобразовательная школа. п. Изыхские Копи, республика Хакасия закон постоянства состава 8 класс Федотова Елена Анатольевна – учитель химии МБОУ Изыхская СОШ

Закон постоянства состава Был открыт французским химиком Прустом: всякое чистое вещество (химическое соединение), каким бы путем оно ни было получено, имеет строго определенный и постоянный состав (качественный и количественный).

Например, вода может быть получена в результате следующих химических реакций: Cu(OH) = H2O + CuO 2Н2 + O2 = 2Н2O Са(ОН)2 + H2SO4 = CaSO4 + 2Н2O

Ясно, что молекула полученной различными способами воды всегда состоит из двух атомов водорода и одного атома кислорода. Этот закон строго выполняется только для веществ молекулярного строения.

На основе закона постоянства состава можно производить различные расчеты Назовите это вещество. Из каких атомов состоит это вещество? Найдите атомные массы серы и железа.

Ar (Fe) = 56 Ar (S) = 32 Ar (Fe) : Ar(S) = 56 : 32 = 7 : 4 Чтобы получить сульфид железа надо смешать железо и серу в массовых соотношениях 7 : 4. Если железа взять 10г,а серы 4 г, химическая реакция произойдет, но 3 г железа в реакцию не вступят.

Задача №1 Сколько граммов железа нужно взять, чтобы прореагировало 2г серы?

Задача №2 Известно вещество, в котором на 2 атома меди приходится 1 атом серы. В каких массовых отношениях нужно взять медь и серу, чтобы оба вещества полностью вступили в реакцию?

решение Масса 2 атомов меди = 64* 2 = 128 Масса1 атома серы = 32. Медь и серу необходимо смешать в соотношении 128 : 32 или 4 : 1
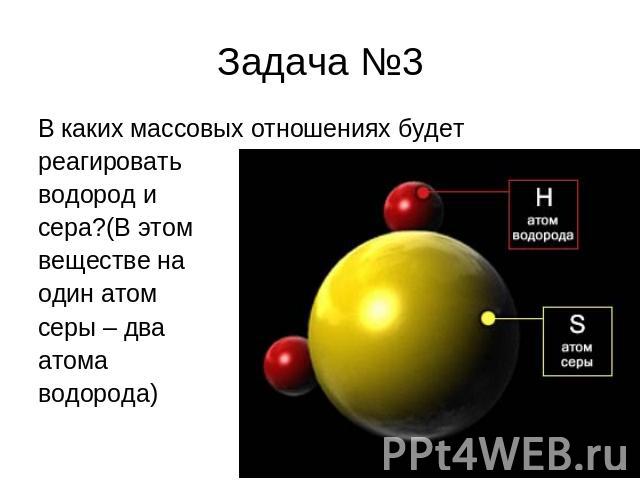
Задача №3 В каких массовых отношениях будет реагировать водород и сера?(В этом веществе на один атом серы – два атома водорода)

решение Находим Ar (S) и Ar (H)*2 32 : 1*2 32 : 2 16 : 1 В этом веществе элементы соединяются в массовых отношениях 16 :1

Домашнее задание: параграф 9, упр №2 стр 31.

литература Учебник «Химия 8 кл» Рудзитис Г.Е, Фельдман Ф.Г.