Презентация на тему: Агрегатные состояния вещества

АГРЕГАТНЫЕ СОСТОЯНИЯ ВЕЩЕСТВА ФИЗИЧЕСКАЯ ХИМИЯ. ЛЕКЦИЯ 2. 900igr.net Физическая химия. Лекция 2
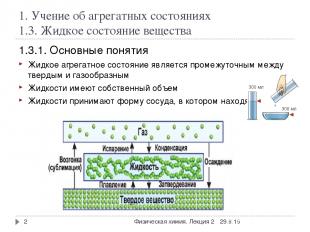
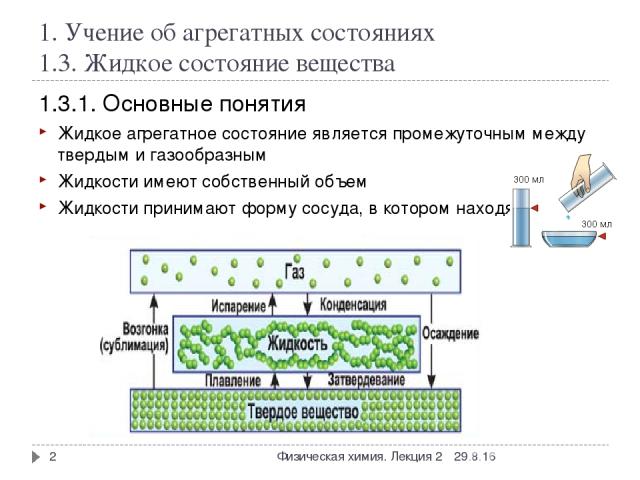
1. Учение об агрегатных состояниях 1.3. Жидкое состояние вещества 1.3.1. Основные понятия Жидкое агрегатное состояние является промежуточным между твердым и газообразным Жидкости имеют собственный объем Жидкости принимают форму сосуда, в котором находятся * * Физическая химия. Лекция 2 Физическая химия. Лекция 2

1. Учение об агрегатных состояниях 1.3. Жидкое состояние вещества Близко расположенные молекулы жидкости могут образовывать упорядоченные структуры, содержащие несколько молекул. Это состояние называется ближним порядком. Ближний порядок — это упорядоченность во взаимном расположении атомов или молекул в веществе, которая повторяется лишь на расстояниях, соизмеримых с расстояниями между частицами, то есть ближний порядок есть закономерность в расположении соседних частиц. * Физическая химия. Лекция 2 * Структура воды: (1) –водяной пар; (2) – жидкая вода Пример ближнего порядка молекул жидкости и дальнего порядка молекул кристаллического вещества: (1) –жидкая вода; (2) – лёд (твердое тело) Физическая химия. Лекция 2

1. Учение об агрегатных состояниях 1.3. Жидкое состояние вещества Факторы, влияющие на поведение жидкости: Химическая природа жидкости В неполярных жидкостях взаимодействия между молекулами слабые, поэтому по свойствам они ближе к газам В полярных жидкостях сильны взаимодействия между молекулами, поэтому такие жидкости по строению и свойствам ближе к твердым телам Внешние условия, в частности, температура Чем ниже температура и чем ближе температура жидкости к температуре ее кристаллизации, тем больше степень упорядоченности частиц и тем ближе свойства жидкости к свойствам твердых веществ Чем выше температура и чем ближе она к температуре кипения, тем больше сходства в поведении жидкостей и газов * * Физическая химия. Лекция 2 Физическая химия. Лекция 2

1. Учение об агрегатных состояниях 1.3. Жидкое состояние вещества Типы связей в жидкостях между молекулами: Ван-дер-Ваальсовы взаимодействия ориентационные силы (диполь-дипольные взаимодействия) дисперсионные силы (взаимодействия между неполярными молекулами) индукционные силы (взаимодействия между полярной и неполярной молекулами) Водородные связи * * Физическая химия. Лекция 2 Физическая химия. Лекция 2

1. Учение об агрегатных состояниях 1.3. Жидкое состояние вещества 1.3.2. Свойства жидкостей Плотность – масса единицы объема жидкости при данной температуре Плотность жидкостей в сотни и тысячи раз больше, чем плотность газов С увеличением температуры плотность всех жидкостей уменьшается (исключение – вода) Аномалии воды!!! * * Физическая химия. Лекция 2 Физическая химия. Лекция 2

1. Учение об агрегатных состояниях 1.3. Жидкое состояние вещества Молярный объем жидкости Для разных жидкостей молярный объем различен!!! Например: для воды * * Физическая химия. Лекция 2 Физическая химия. Лекция 2

1. Учение об агрегатных состояниях 1.3. Жидкое состояние вещества Поверхностное натяжение – это энергия, необходимая для образования новой поверхности. σ – коэффициент поверхностного натяжения А – работа, Дж S – площадь поверхности, м² Зависит от природы жидкости, природы граничащего с ней тела, температуры, наличия примесей в жидкости. Уменьшается с увеличением температуры и при добавлении поверхностно-активных веществ (ПАВ) * * Физическая химия. Лекция 2 Физическая химия. Лекция 2

1. Учение об агрегатных состояниях 1.3. Жидкое состояние вещества Текучесть - способность изменять форму за малое время под действием даже малой силы. Благодаря этому свойству все жидкости льются в виде струй, разбрызгиваются каплями, принимают форму того сосуда, в который их нальют. Текучесть – величина, обратная вязкости. * * Физическая химия. Лекция 2 Физическая химия. Лекция 2

1. Учение об агрегатных состояниях 1.3. Жидкое состояние вещества Вязкость (внутреннее трение, сопротивляемость течению) – это сопротивление, возникающее внутри жидкости при перемещении с различными скоростями одних слоев ее относительно других. Вязкость – термодинамическое свойство текучего тела. Вязкость жидкости уменьшается с увеличением температуры (исключение – вода). Вязкость имеет важное значение в решении производственных вопросов, связанных с транспортировкой текучих материалов по трубопроводам, с перемешиванием жидкостей и газов, с движением судов, самолетов и т.п. * * Физическая химия. Лекция 2 Физическая химия. Лекция 2

1. Учение об агрегатных состояниях 1.3. Жидкое состояние вещества Динамическая вязкость (коэффициент внутреннего трения) µ F – сила сопротивления сдвигу, Н l – расстояние, l = 1м S – площадь поверхности, S = 1 м² v – скорость, v = 1 м/с Кинематическая вязкость ν – отношение динамической вязкости жидкости к ее плотности * * Физическая химия. Лекция 2 Физическая химия. Лекция 2

1. Учение об агрегатных состояниях 1.3. Жидкое состояние вещества 1.3.3. Парообразование Парообразование – переход вещества в газообразное состояние. Для жидкостей различают две формы парообразования: испарение и кипение. При испарении пар образуется только на свободной поверхности жидкости. Кипение – это процесс испарения жидкости, протекающий во всем её объеме. * Физическая химия. Лекция 2 * Испарение Кипение Физическая химия. Лекция 2

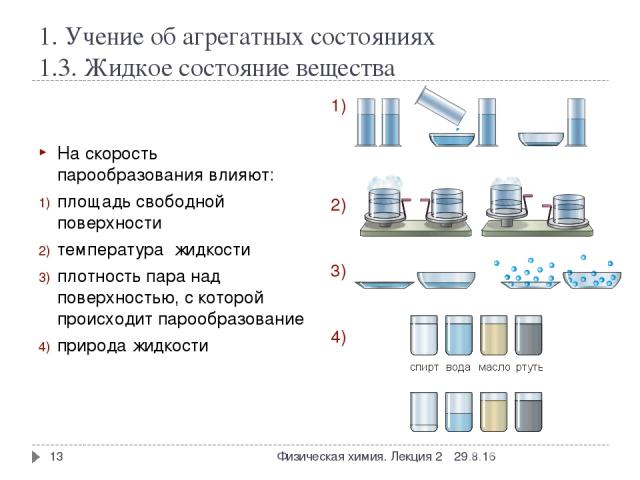
1. Учение об агрегатных состояниях 1.3. Жидкое состояние вещества На скорость парообразования влияют: площадь свободной поверхности температура жидкости плотность пара над поверхностью, с которой происходит парообразование природа жидкости П п п п * * Физическая химия. Лекция 2 Физическая химия. Лекция 2
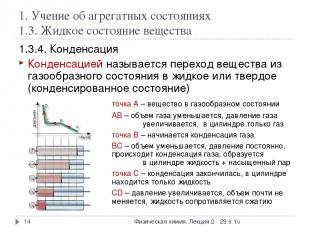
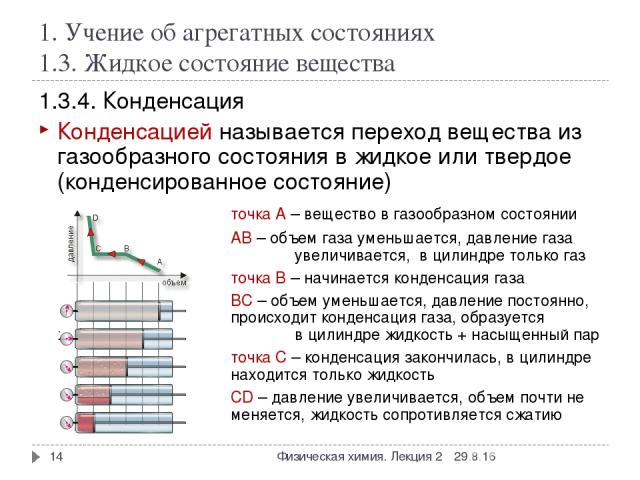
1. Учение об агрегатных состояниях 1.3. Жидкое состояние вещества 1.3.4. Конденсация Конденсацией называется переход вещества из газообразного состояния в жидкое или твердое (конденсированное состояние) точка А – вещество в газообразном состоянии АВ – объем газа уменьшается, давление газа увеличивается, в цилиндре только газ точка В – начинается конденсация газа ВС – объем уменьшается, давление постоянно, происходит конденсация газа, образуется жидкость, в цилиндре жидкость + насыщенный пар точка C – конденсация закончилась, в цилиндре находится только жидкость CD – давление увеличивается, объем почти не меняется, жидкость сопротивляется сжатию * * Физическая химия. Лекция 2 Физическая химия. Лекция 2

1. Учение об агрегатных состояниях 1.3. Жидкое состояние вещества Давление насыщенного пара Газ, находящийся в термодинамическом равновесии со своей жидкостью, называется насыщенным паром. Слово "насыщенный" подчеркивает, что при данной температуре этот пар не может содержать большее число молекул, то есть иметь бóльшую плотность. На участке BC в цилиндре одновременно сосуществуют газ и жидкость (см. слайд 12). Их температура и давление одинаковы. Это давление не зависит от количества жидкости и газа. Вдвигая поршень, мы на мгновение увеличиваем давление газа около поршня, что способствует переходу части молекул в жидкость, и давление вновь становится прежним. В этом случае говорят, что в цилиндре наблюдается термодинамическое равновесие. * * Физическая химия. Лекция 2 Физическая химия. Лекция 2
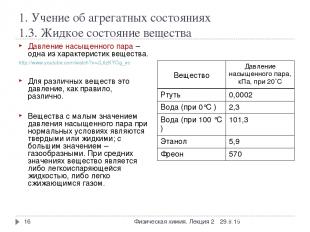
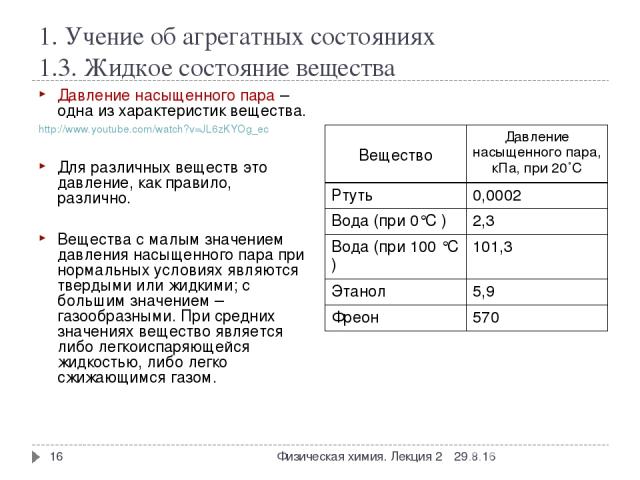
1. Учение об агрегатных состояниях 1.3. Жидкое состояние вещества * Физическая химия. Лекция 2 * Давление насыщенного пара – одна из характеристик вещества. http://www.youtube.com/watch?v=JL6zKYOg_ec Для различных веществ это давление, как правило, различно. Вещества с малым значением давления насыщенного пара при нормальных условиях являются твердыми или жидкими; с большим значением – газообразными. При средних значениях вещество является либо легкоиспаряющейся жидкостью, либо легко сжижающимся газом. Вещество Давление насыщенного пара, кПа, при 20˚С Ртуть 0,0002 Вода (при 0°С ) 2,3 Вода (при 100 °С ) 101,3 Этанол 5,9 Фреон 570 Физическая химия. Лекция 2

1. Учение об агрегатных состояниях 1.3. Жидкое состояние вещества * Физическая химия. Лекция 2 * Давление насыщенного пара растет с ростом температуры Кипение жидкости характеризуется равенством давления насыщенного пара и внешнего давления Вещество Давление насыщенного пара, кПа Внешнее давление, кПа Вода (при 100 °С ) 101,3 101,3 Вещество Давление насыщенного пара, кПа Вода (при 0°С ) 2,3 Вода (при 100 °С ) 101,3 Физическая химия. Лекция 2

1. Учение об агрегатных состояниях 1.3. Жидкое состояние вещества * Физическая химия. Лекция 2 * Зависимость температуры кипения от внешнего давления и от давления насыщенного пара: с ростом внешнего давления температура кипения увеличивается; давление насыщенного пара всегда растет с ростом температуры; увеличивая внешнее давление, можно повышать температуру кипения, но лишь до определённого предела — критической температуры и критического давления, выше которых исчезает граница раздела жидкой и газообразной фазы (флюидная жидкость). Критическая точка воды: Т=647К, р=218,3 бар Физическая химия. Лекция 2

1. Учение об агрегатных состояниях 1.4. Твёрдое агрегатное состояние * Физическая химия. Лекция 2 * Твёрдое вещество имеет собственную форму и оказывает сопротивление всякому действию, направленному на изменение формы Высокая упорядоченность частиц (дальний порядок) Дальний порядок — это упорядоченность во взаимном расположении атомов или молекул в веществе, которая повторяется на неограниченно больших расстояниях. Твердые вещества могут находиться в двух состояниях: кристаллическом аморфном Физическая химия. Лекция 2

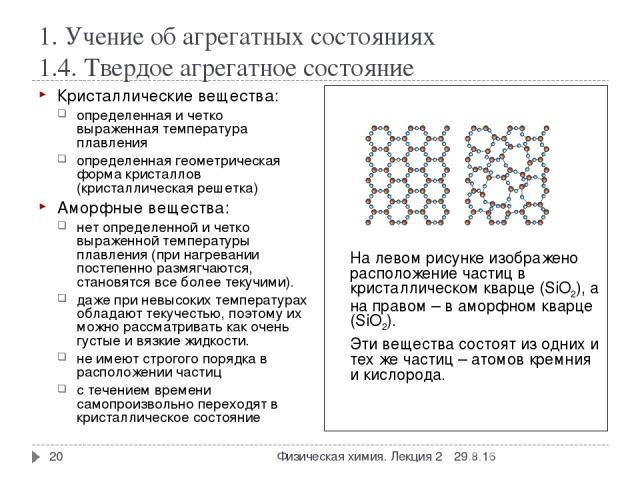
1. Учение об агрегатных состояниях 1.4. Твердое агрегатное состояние * Физическая химия. Лекция 2 * Кристаллические вещества: определенная и четко выраженная температура плавления определенная геометрическая форма кристаллов (кристаллическая решетка) Аморфные вещества: нет определенной и четко выраженной температуры плавления (при нагревании постепенно размягчаются, становятся все более текучими). даже при невысоких температурах обладают текучестью, поэтому их можно рассматривать как очень густые и вязкие жидкости. не имеют строгого порядка в расположении частиц с течением времени самопроизвольно переходят в кристаллическое состояние На левом рисунке изображено расположение частиц в кристаллическом кварце (SiO2), а на правом – в аморфном кварце (SiO2). Эти вещества состоят из одних и тех же частиц – атомов кремния и кислорода. Физическая химия. Лекция 2
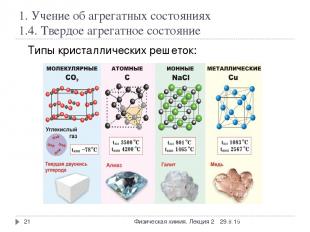
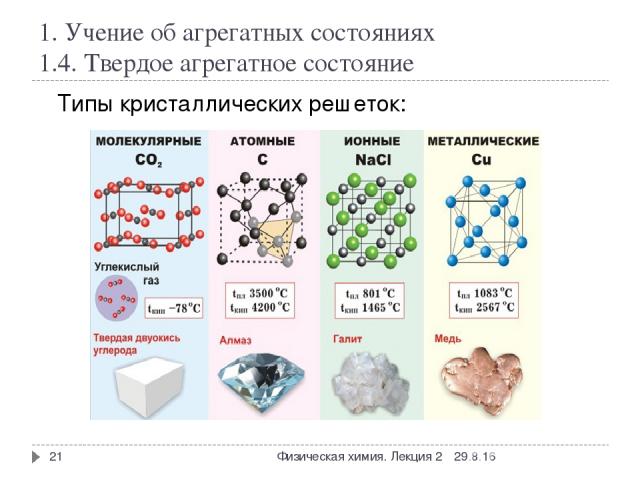
1. Учение об агрегатных состояниях 1.4. Твердое агрегатное состояние * Физическая химия. Лекция 2 * Типы кристаллических решеток: Физическая химия. Лекция 2

1. Учение об агрегатных состояниях 1.4. Твердое агрегатное состояние * Физическая химия. Лекция 2 * Кристалл – твердое тело, состоящее из упорядоченных, периодически повторяющихся в пространстве частиц Наименьшей структурной единицей кристалла является элементарная ячейка Частицы размещаются в ней согласно принципа наиболее плотной упаковки, при которой остается наименьшее по объему свободное пространство между этими частицами Основные элементарные ячейки: Кубическая Тетрагональная или тетраэдрическая Гексагональная Ромбоэдрическая или тригональная Ромбическая Моноклинная Триклинная 1) 2) 3) 4) 5) 6) 7) Физическая химия. Лекция 2

1. Учение об агрегатных состояниях 1.4. Твердое агрегатное состояние Физические свойства кристаллических тел (такие, как прочность на разрыв, эластичность, тепло- и электропроводность, светопроницаемость и т.д.) неодинаковы в различных направлениях, но совпадают в параллельных направлениях. Такое свойство тел называется анизотропностью. Свойства аморфных тел однородны во всех направлениях, т.е. аморфные тела изотропны. * Физическая химия. Лекция 2 * Физическая химия. Лекция 2

1. Учение об агрегатных состояниях 1.4. Твердое агрегатное состояние Кристаллические тела делятся на монокристаллы и поликристаллы. Монокристаллы (монолитные, единые кристаллы) обладают периодически повторяющейся внутренней структурой во всем его объеме. Монокристаллы германия, кремния и др. используют для изготовления полупроводниковой аппаратуры Монокристаллы кварца, германия, фторида лития и др. используют в оптических узлах многих приборов. Монокристаллы алмаза используют при обработке особо твёрдых материалов Украшения – бриллианты, топазы, сапфиры, рубины и др. Поликристаллическое тело представляет собой совокупность сросшихся друг с другом хаотически ориентированных маленьких кристаллов — кристаллитов. Каждый маленький монокристалл поликристаллического тела анизотропен, но поликристаллическое тело изотропно. * Физическая химия. Лекция 2 * Физическая химия. Лекция 2

1. Учение об агрегатных состояниях 1.4. Твердое агрегатное состояние * Физическая химия. Лекция 2 * Кристаллогидраты солей – твердые соли, в состав ионных кристаллов которых входят молекулы воды Кристаллогидраты солей различаются по количеству кристаллизационной воды и по характеру связи молекул воды с другими частицами, составляющими кристалл (координационная, водородная связи) CaCl2•6H2O, CaCl2•4H2O, CaCl2•2H2O, Образование кристаллогидратов всегда сопровождается выделением теплоты Молекулы воды могут связываться как с катионами, так и с анионами Кристалл CuSO4•5H2O Физическая химия. Лекция 2

1. Учение об агрегатных состояниях 1.5. Жидкокристаллическое состояние вещества Жидкокристаллическим (мезоморфным) состоянием вещества называется такое состояние, свойства которого являются промежуточными между свойствами твердого кристалла и жидкости. Жидкие кристаллы сочетают в себе свойства как твердых кристаллических тел (наличие дальнего ориентационного порядка, оптические свойства – рассеяние, поляризация и преломление света, анизотропия), так и жидкостей (проявление текучести, вязкости) Жидкие кристаллы - особое состояние некоторых органических веществ, в котором они обладают текучестью и свойством образовывать пространственные структуры, подобные кристаллическим. Холестерилбензоат , плавится при 145°С с образованием мутного расплава, имеющего жидкокристаллическую структуру; при 179°С становится настоящей прозрачной жидкостью. * Физическая химия. Лекция 2 * Физическая химия. Лекция 2

1. Учение об агрегатных состояниях 1.5. Жидкокристаллическое состояние вещества * Физическая химия. Лекция 2 * Жидкие кристаллы образуются в веществах с продолговатой формой молекул, взаимная ориентация которых обусловливает анизотропию (т.е. неодинаковость) их физических свойств. Жидкие кристаллы могут изменять свою структуру и светооптические свойства под действием электрического напряжения. Обычная вода, свойства которой во всех направлениях одинаковы Жидкий кристалл, ориентационное упорядочение Физическая химия. Лекция 2

1. Учение об агрегатных состояниях 1.5. Жидкокристаллическое состояние вещества В зависимости от способа ориентации молекул в пространстве жидкие кристаллы делят на четыре класса: нематики, смектики, холестерики и дискотики. У нематических жидких кристаллов оси молекул ориентированы параллельно друг другу. Молекулы располагаются послойно, направление осей молекул перпендикулярно слоям (рис. а). Молекулы смектиков также располагаются перпендикулярно слоям (рис. b), однако некоторая часть молекул частично располагается в соседних слоях. У холестериков (рис. c) молекулы также располагаются послойно, но оси молекул ориентированы параллельно плоскостям, в которых они лежат, и направление молекул изменяется по винтовой линии при переходе от одного слоя к другому. У дискотиков (рис. d) длинные молекулы свиваются в клубочки в форме дисков (таблеток). * Физическая химия. Лекция 2 * Физическая химия. Лекция 2

1. Учение об агрегатных состояниях 1.5. Жидкокристаллическое состояние вещества Жидкие кристаллы изменяют свои физические свойства под действием различных физических факторов (температуры, электрических и магнитных полей, механических напряжений, излучения), что широко используется в современных устройствах и технологиях: индикаторные устройства (электроника, часы, мобильные телефоны); жидкокристаллические экраны мониторов, телевизоров, табло и т.п.; термометры, термоскопы, устройства, сигнализирующие о превышении температуры; термокраски (для сигнализации о перегреве поверхности); для сигнализации о химической опасности Устройство сигнализации химической опасности Принцип действия таких устройств основан на способности молекул жидких кристаллов вступать во взаимодействие с некоторыми химическими веществами, образуя более крупные молекулы. Этот процесс сопровождается изменением окраски тонких жидкокристаллических пленок. Устройство представляет собой табло нейтрального цвета, на котором изображен сигнал опасности с помощью жидкокристаллического вещества. Если концентрация вредного вещества (например, толуола) невелика, пленка жидкого кристалла также имеет нейтральную окраску. Когда концентрация толуола в воздухе превысит предельно допустимую, надпись на табло окрашивается в красный цвет. * Физическая химия. Лекция 2 * Физическая химия. Лекция 2

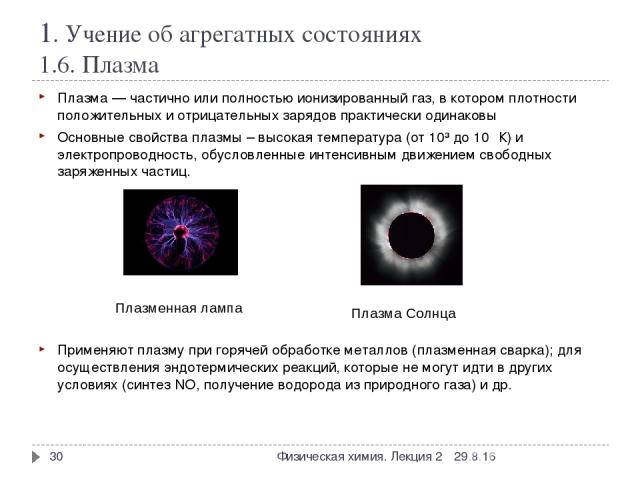
1. Учение об агрегатных состояниях 1.6. Плазма Плазма — частично или полностью ионизированный газ, в котором плотности положительных и отрицательных зарядов практически одинаковы Основные свойства плазмы – высокая температура (от 10³ до 10⁹ К) и электропроводность, обусловленные интенсивным движением свободных заряженных частиц. Применяют плазму при горячей обработке металлов (плазменная сварка); для осуществления эндотермических реакций, которые не могут идти в других условиях (синтез NO, получение водорода из природного газа) и др. * Физическая химия. Лекция 2 * Плазменная лампа Плазма Солнца Физическая химия. Лекция 2