Презентация на тему: Электролиз 9 класс

Тема урока: Электролиз урок – презентация 9 класс

Цель урока: Обобщать и систематизировать знания по теме. Знать о практическом использовании электролиза в промышленном производстве металлов. Уметь обобщать, выделять главное, использовать теоретические знания на практике.

План урока: I. Повторение тем: «Электролитическая диссоциация», «Сильные и слабые электролиты»II. Изучение материала по плану: 1. Определение сущности процесса электролиза. 2. Правила для определения результатов электролиза: а) процессы на катоде; б) процессы на аноде; 3. Закон Фарадея. 4. Области использования электролиза III. Закрепление материала.

Повторение темы: «Электролитическая диссоциация» Электрический ток – это направленное движение электрически заряженных частиц.Вещества, в которых заряженные частицы могут перемещаться на значительные расстояния, называются проводниками. В металлах (проводниках I рода) такими частицами являются электроны.Вещества, водные растворы или расплавы которых проводят электрический ток за счет перемещения ионов, называются электролитами (проводниками II рода).

По рисунку 1 объясните термин «Электролитическая диссоциация». Расскажите о процессе диссоциации. Как называют положительные и отрицательные ионы? Рис.1. Диссоциация электролита с:А) молекулярной;В) кристаллической структурой (ионный кристалл)
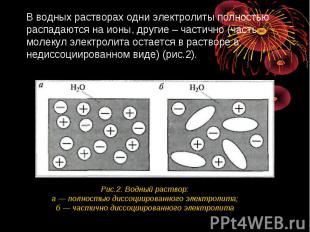
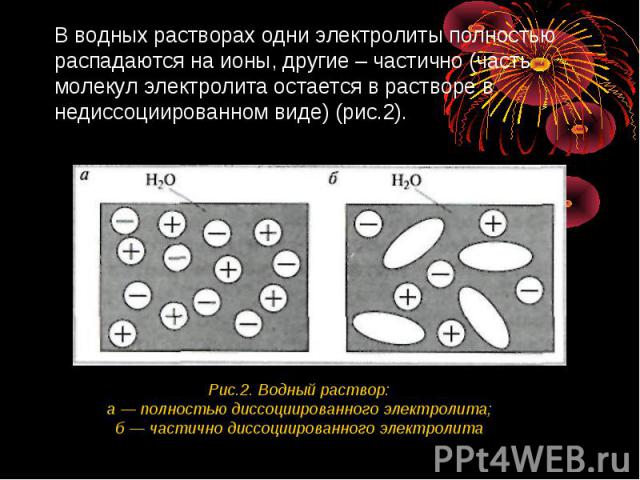
В водных растворах одни электролиты полностью распадаются на ионы, другие – частично (часть молекул электролита остается в растворе в недиссоциированном виде) (рис.2). Рис.2. Водный раствор:а — полностью диссоциированного электролита;б — частично диссоциированного электролита

Чем больше молекул электролита распадается на ионы, тем сильнее электролит. Диссоциация сильных электролитов – необратимый процесс, слабых – обратимый.

II. Изучение нового материала.1. Сущность процесса электролиза. Движение ионов в растворе или расплаве электролита является беспорядочным. Но если в электролит опустить электроды и пропустить постоянный электрический ток, то ионы будут двигаться упорядоченно к электродам: катионы – к катоду, анионы – к аноду. На катоде идет процесс восстановления, катионы принимают электроны. На аноде идет процесс окисления, анионы отдают электроны. Это явление называют электролизом.

Что такое электролиз? В чем заключается сущность электролиза? Электролиз – это окислительно – восстановительный процесс, протекающий на электродах в растворах или расплавах электролитов при пропускании электрического тока.Сущность электролиза заключается в том, что за счет электрической энергии осуществляется химическая реакция, которая не может протекать самопроизвольно.

2. Правила для определения результатов электролиза.а) Электролиз в расплавах (электроды нерастворимые). NaCl ↔ Na+ + Cl- К А Na+ + 1e = Na; 2Cl- – 2e = Cl2 В результате на катоде выделяется металлический натрий, на аноде – газообразный хлор. 2NaCl ↔ 2Na + Cl2

Электролиз в растворах. При электролизе водных растворов могут участвовать не только ионы растворенного вещества, но и ионы и молекулы растворителя.Например: Водный раствор соли МеАn содержит: катионы Ме+ и Н+; анионы Аn- и ОН- и молекулы Н2О.

На катоде возможны восстановительные процессы: Ме+ + е = Ме (1)2Н+ + 2е = Н2 (2) в кисл. ср.2Н2О + 2е = Н2 + 2ОН- (3) в нейтр и щел. Ср.

На аноде возможны окислительные процессы: Окисл. анионов Аn- (4)4ОН- – 4е = 2О2 + 4Н+ (5) в щел. ср.2Н2О – 4е = О2 + 4Н+ (6) в нейтр и кисл Окисл. матер. анода (7) Окисляющийся анод называют активным. Неокисляющийся – инертным. Инертные аноды изготавливают из графита, угля, платины.

Какие из этих процессов будут преобладать?На катоде: В растворах процесс на катоде зависит от активности восстанавливаемого металла:а) Если металл расположен в ряду напряжений справа от олова, то идет процесс (1) – на катоде выделяется металл.б) Если металл расположен слева от алюминия, его катион не восстанавливается; идут процессы (2) или (3) (в зависимости от среды раствора) – выделяется водородв) Если металл расположен между Al и Sn, возможно одновременное протекание процессов (1), и в зависимости от среды раствора (2) или (3), т.е. выделяются и металл и водород.

На аноде: 1. Если анод активный, окисляется материал анода – процесс 7На инертном аноде:2. Анионы безкислородных кислот (кроме НF) окисляются легче, чем ОН и НО; идет процесс 43. Анионы кислородных кислот и фторидов окисляются труднее, чем ОН и НО идут процессы 5 или 6 в зависимости от среды раствора, т.е выделяется кислород

1-й закон Фарадея: Массы веществ, выделившихся на катоде и аноде, пропорциональны количеству прошедшего через раствор или расплав электричества. m = Э∙I∙t ∕ F где Э – эквивалент вещества(г∕моль) t – время электролиза, (с) I – сила тока (А) F – постоянная Фарадея (F=96,500Кл∕моль)
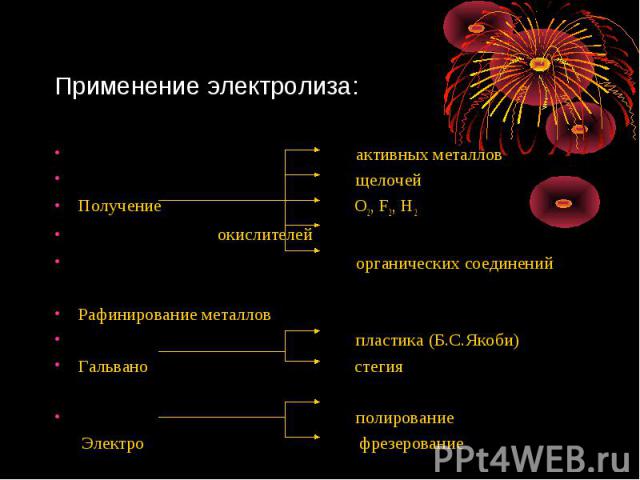
Применение электролиза: активных металлов щелочейПолучение О2, F2, Н2 окислителей органических соединенийРафинирование металлов пластика (Б.С.Якоби)Гальвано стегия полирование Электро фрезерование

Тест по теме «Электролиз»При электролизе раствора сульфата цинка с инертными электродами на аноде выделяется: а) цинк; б) кислород; в) водород; г) сера.

2. Объем кислорода (н.у.) выделившегося на инертном аноде при пропускании электрического тока силой 20 А в течение 2.5 ч через раствор сульфата калия, равен: а) 10,4; б) 11,2; в) 6,8; г) 20,6.

3. При электролизе 240 г 15%-го раствора гидро-ксида натрия на аноде выделилось 89,6 л (н. у.) кислорода. Массовая доля вещества в растворе после окончания электролиза равна (в %): а) 28,1; б)32,1; в) 37,5; г) 40,5.

4. При электролизе раствора хлорида натрия образуются: а)натрий и хлор; б)гидроксид натрия, хлор и водород; в)кислород и хлор; г)натрий, хлор и соляная кислота.

5.При электролизе расплава гидроксида натрия на аноде выделяется: а) натрий; б) водород; в) кислород; г) вода.

6.При электролизе раствора хлорида кальция на катоде выделилось 5,6 г водорода. Какова масса (в г) вещества, выделившегося на аноде? а) 198,8; б) 99,4; в) 89,6; г) 44,8.

7.Медный купорос массой 100 г растворили в воде и провели электролиз до обесцвечивания раствора. объем (в л, н. у.) собранного газа равен: а) 2,24; б)4,48; в) 11,2; г) 22,4.

8.Платиновый электрод: а)инертный; б)растворимый; в)расходуется в процессе электролиза; г)не расходуется в процессе электролиза.

9.Процесс на катоде при электролизе растворов солей зависит от: а)природы катода; б)активности металла; в)состава аниона; г)не зависит от перечисленных факторов.

10.При электролизе раствора нитрата меди( П) с медными электродами на аноде будет происходить: а)выделение диоксида азота; б)выделение монооксида азота; в)растворение анода; г)выделение кислорода.

Правильно

Неправильно