Презентация на тему: Электрический ток в электролитах

Тема: «Электрический ток в электролитах».Работу выполнила: Ученица 11 «А» класса МОУ «СОШ № 95 им. Н. Щукина п. Архара»Никитенко Анастасия.

Цель:Изучить электрические и химические процессы в электролитах.

Задачи:Доказать что концентрация раствора электролита влияет на силу тока. Установить, как влияет расстояния между электродами на силу тока. Выяснить, как влияет природа электролита на силу тока в нём.

ПланI.Введение.II.Основная часть.К истории законов электролиза.Библиографическая справка о М. Фарадеи. Электрический ток в электролитах. III.Практическая часть.IV. Выводы.


ФАРАДЕЙ (Faraday) Майкл (1791-1867) Английский физик, основоположник учения об электромагнитном поле, иностранный почетный член Петербургской АН (1830). Обнаружил химическое действие электрического тока, взаимосвязь между электричеством и магнетизмом, магнетизмом и светом. Открыл (1831) электромагнитную индукцию — явление, которое легло в основу электротехники. Установил (1833-34) законы электролиза, названные его именем, открыл пара- и диамагнетизм, вращение плоскости поляризации света в магнитном поле (эффект Фарадея). Доказал тождественность различных видов электричества. Ввел понятия электрического и магнитного поля, высказал идею существования электромагнитных волн.

Термин «электролит» (от греческого «разлагаемый электричеством») впервые предложил английскийхимик и физик М.Фарадей

Электролитами принято называть проводящие среды, в которых протекание электрического тока сопровождается переносом вещества.

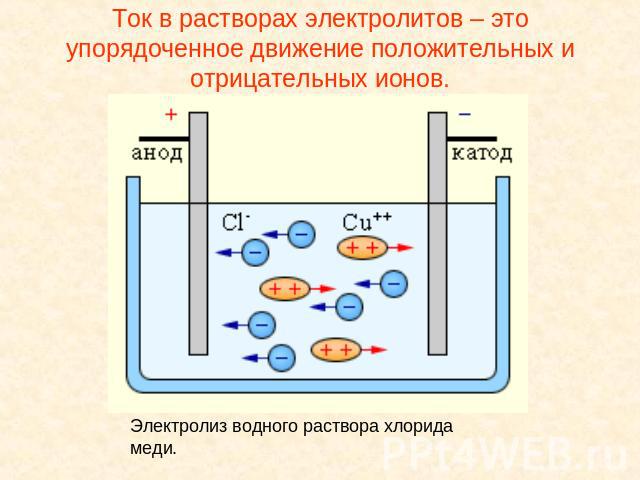
Прохождение электрического тока через электролит сопровождается выделением веществ на электродах. Это явление получило название электролиза.
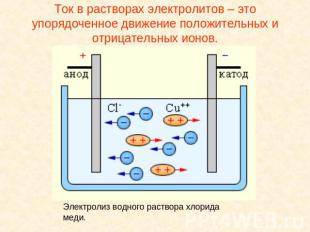
Ток в растворах электролитов – это упорядоченное движение положительных и отрицательных ионов.

Первый закон электролиза. Закон электролиза был экспериментально установлен английским физиком М. Фарадеем в 1833 году. Закон Фарадея определяет количества первичных продуктов, выделяющихся на электродах при электролизе.

Первый закон электролиза.Масса m вещества, выделившегося на электроде, прямо пропорциональна заряду q, прошедшему через электролит: m=kq=kIt.

Второй закон Фарадея Данный закон отвечает на вопрос от чего зависит электрохимический эквивалент. Электрохимические эквиваленты различных веществ пропорциональны их атомным весам и обратно пропорциональны числам, выражающим их химическую валентность.

Внешний вид установки.
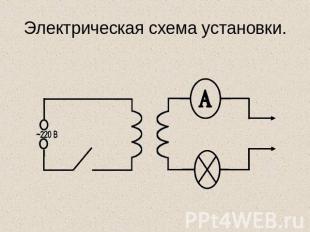
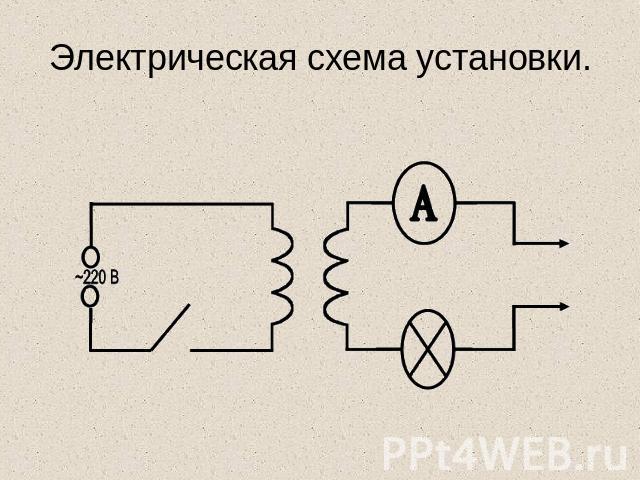
Электрическая схема установки.

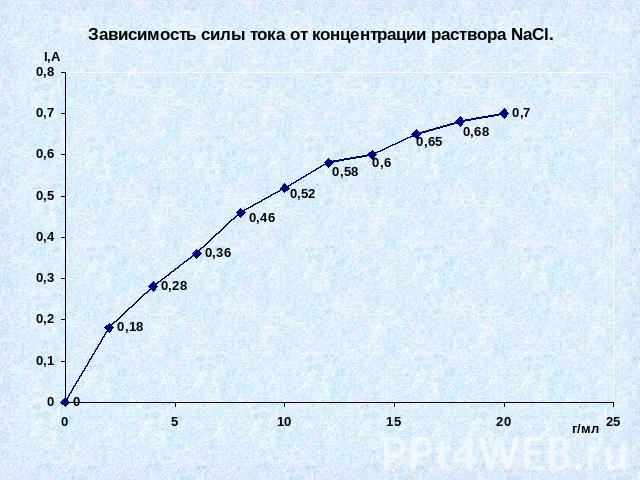
Практическая часть №1Доказать что концентрация раствора электролита влияет на силу тока.
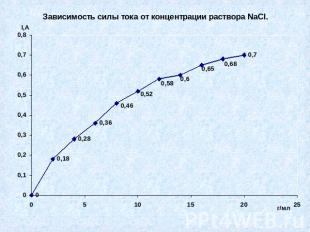

Вывод № 1.Сила тока зависит от концентрации раствора, чем насыщение раствор, тем больше сила тока.

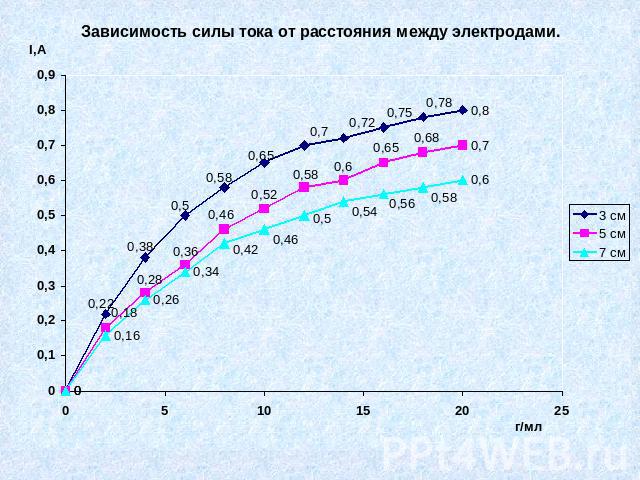
Практическая часть № 2.Установить, как влияет расстояния между электродами на силу тока.
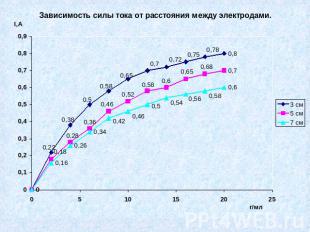

Вывод № 2.Сила тока зависит от расстояния между электродами, чем меньше расстояние тем больше сила тока и наоборот.

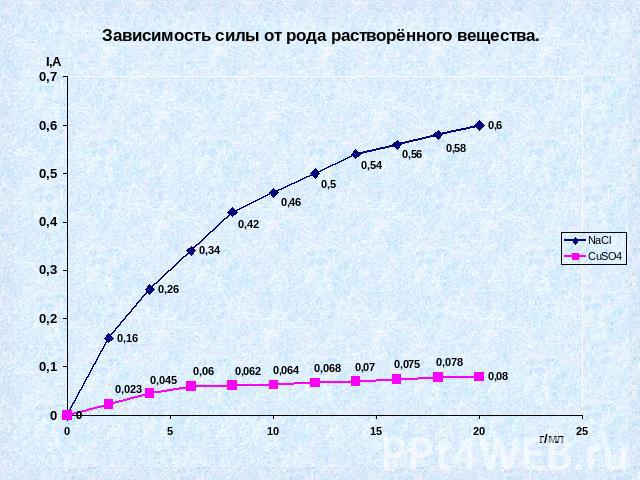
Практическая часть № 3.Выяснить, как влияет природа электролита на силу тока в нём.
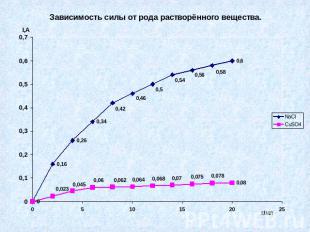

Вывод № 3.Различные электролиты по-разному проводят электрический ток.

Применение электролиза Электрический метод получения чистых металлов. Гальваностегия. Гальванопластика. Электрическая полировка.Электрометаллургия.

Сам факт разложение электролитов при прохождении через них тока показывает, что в них движения зарядов сопровождается движение атомов или групп атомов, связанных друг с другом; эти атомы или атомные группы представляют собой части молекулы растворенного вещества. Естественно предположить, что заряжены именно эти части молекул в растворе и что они являются носителями электрического заряда. Их перемещение под действием сил электрического поля и представляют собой электрический ток, идущий через электролит. Тщательно поставленные опыты позволили установить, что для электролитов справедлив закон Ома.

Глинка Н.Л.Общая химия: - Л.: Химия 1985.-704с. Под ред. В.А. Рабиновича.Детлаф А. А., Яворский Б. М.Курс физики: Учеб. Пособие для втузов.- М.:Высш. Шк.1989 Фролов В.В.Химия: - М.: Высш. Шк., 1986.- 543с. «Элементарный учебник физики под редакцией академика Г.С. Ландсберга - Том II – электричество и магнетизм». Москва, «Наука» 1972 год.