Презентация на тему: Электрический ток в электролитах

Электрический ток в жидкостях Электрический ток в электролитах 900igr.net

Электролиты Проводниками электрического тока являются не только металлы и полупроводники. Электрический ток проводят растворы многих веществ в воде. Как показывает опыт, чистая вода не проводит электрический ток, то есть в ней нет свободных носителей электрических зарядов. Не проводят электрический ток и кристаллы поваренной соли, хлорида натрия. Однако раствор хлорида натрия является хорошим проводником электрического тока. Растворы солей, кислот и оснований, способные проводить электрический ток, называются электролитами.

Электролиз Прохождение электрического тока через электролит обязательно сопровождается выделением вещества в твёрдом или газообразном состоянии на поверхности электродов. Выделение вещества на электродах показывает, что в электролитах электрические заряды переносят заряженные атомы вещества – ионы. Этот процесс называется электролизом.

Закон электролиза Майкл Фарадей на основе экспериментов с различными электролитами установил, что при электролизе масса m выделившегося на электроде вещества пропорциональна прошедшему через электролит заряду ∆q или силе тока I и времени ∆t прохождения тока: m=k∆q= kI∆t. Это уравнение называется законом электролиза. Коэффициент k, зависящий от выделившегося вещества, называется электрохимическим эквивалентом вещества.

Проводимость электролитов Проводимость жидких электролитов объясняется тем, что при растворении в воде нейтральные молекулы солей, кислот и оснований распадаются на отрицательные и положительные ионы. В электрическом поле ионы приходят в движение и создают электрический ток.
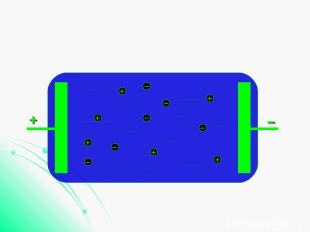
+ − + − + − + − + − + + − −
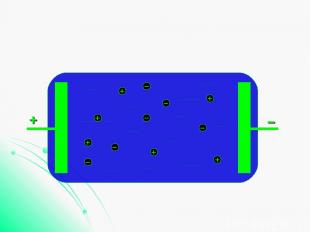
+ − + − + − + − + − + + − −

Агрегатное состояние электролитов Существуют не только жидкие, но и твёрдые электролиты. Примером твёрдого электролита может служить стекло. В составе стекла имеются положительные и отрицательные ионы. В твёрдом состоянии стекло не проводит электрический ток, так как ионы не могут двигаться в твёрдом теле. При нагревании стекла ионы получают возможность перемещаться под действием электрического поля и стекло становится проводником.

Применение электролиза Явление электролиза применяется на практике для получения многих металлов из раствора солей. С помощью электролиза для защиты от окисления или для украшения производится покрытие различных предметов и деталей машин тонкими слоями таких металлов, как хром, никель, серебро, золото.