Презентация на тему: структурные уровни

Раздел «Структурные уровни и системная организация материи» Мальцев Алексей Владимирович, Доцент кафедры общей психологии и психологии личности [email protected]

Тема «Микро-, макро-, мегамиры» Изучается самостоятельно на семинарских занятиях в виде деловой игры

Тема «Системные уровни организации материи»

Свойства материи (природы) Целостность Системность Аддитивность Интегративность

Целостность природы Природное тело (объект) сочетает в себе много свойств (физических, химических, биологических) т.е. обладает целостностью Рассмотрение природы как системы, представляет единое целое и в то же время как подсистему для вышестоящих уровней, поэтому целость относительна.

Целостность природы

Системность природы Природа рассматривается как совокупность взаимосвязанных элементов, которая образует целостный объект, имеющий новые качества, не свойственные элементам составляющим эту систему. Природным системам присуще следующие качества: Множественность элементов (сложные системы) Связь элементов с окружающей средой Согласованная организация элементов в системе как в пространстве так и во времени, направленное на осуществление функций системы

Примеры систем совокупность звезд нашей Галактики буквы, составляющие текст звезды, входящие в состав шарового скопления двойные звезды Примеры антисистем звезды, составляющие созвездие атомы, составляющие химический элемент буквы, составляющие алфавит совокупность всех звезд спектрального класса G

Системность природы

Аддитивные свойства систем Свойство системы, состоящее в том, что значение, соответствующее целому объекту, равно сумме значений, соответствующих его частям. Наблюдаются для отдельных элементов системы Распространены в физических явлениях когда величина объекта в целом равна сумме величин составных частей.

Примеры аддитивных величин: Энергия; Импульс; Энтропия; Мощность; Давление, плотность (в случае смеси идеальных газов); Электрический заряд; Свойство аддитивности для физических величин называется принципом суперпозиции

Аддитивные свойства систем Мало распространены при химических явлениях. Например количество вещества (в случае смеси не взаимодействующих химически ингредиентов); Отсутствуют в живой природе

Интегративные свойства систем Такие свойства, которые присущи системе в целом, но не свойственны ни одному из ее элементов в отдельности. Наличие интегративных свойств показывает, что свойства системы хотя и зависят от свойств элементов, но не определяются ими полностью. Таким образом, во-первых – система не сводится к простой совокупности элементов; во-вторых – расчленяя систему на части, изучая каждую из них в отдельности, нельзя познать все свойства системы в целом.

Примеры интегративности Экологические системы (биогеоценозы) Живой организм – особенно организм человека не сводится к сумме составляющих его органов, тканей и клеток Взаимодействие химических веществ (химические реакции): перераспределение атомов химических элементов в составе молекул продуктов реакции. Взаимодействие элементарных частиц с образованием новых частиц (ядерные реакции)
Интегративность живых систем

Иерархичность природных систем порядок подчинённости низших звеньев высшим, организация их в структуру типа «дерево»;

Иерархичность физических систем Фундаментальные частицы (кварки) Составные элементарные частицы (протон) Атомные ядра Атомы Молекулы Макроскопические тела

Иерархичность астрономических систем звёзды с их планетными системами галактики скопления галактик сверхскопления галактик метагалактика

Иерархичность химических систем атом простая молекула (молекула из одного вида химического элемента) сложная молекула (молекула из разных видов химических элементов) Макромолекула (полимер, состоящий из мономеров) вещество (тела)

Иерархичность биологических систем Рассмотреть самостоятельно в рамках темы Особенности биологического уровня организации материи

Тема «Структуры микромира»

Элементарные частицы Это частицы, входящие в состав атома. Электрон был открыт Томсоном в 1867 году Протон был открыт Резерфордом в 1919 году Нейтрон был открыт Чедвиком в 1932 году Нейтрино было открыто Паули в 1930 году В настоящее время известно более 350 элементарных частиц

Фундаментальные частицы микрочастицы, внутреннюю структуру которой нельзя представить в виде объединения других свободных частиц.
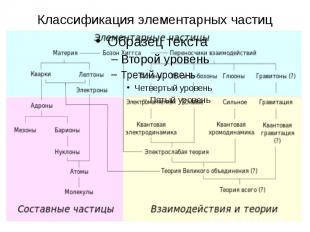
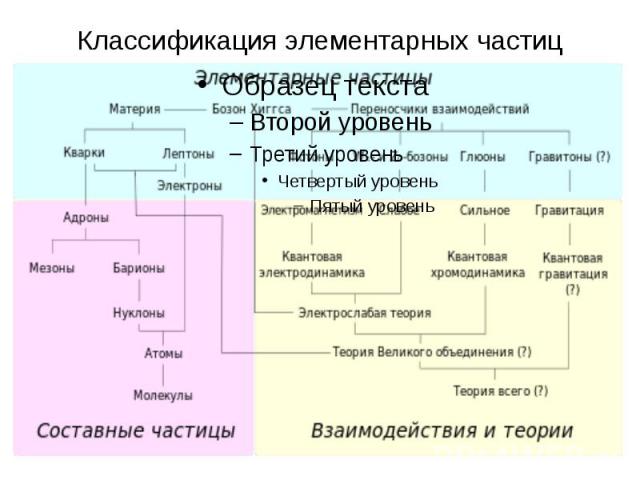
Классификация элементарных частиц

Частицы, образующие вещество Адроны – составные частицы, состоят из кварков, участвуют в сильных взаимодействиях (например протон и нейтрон). Имеют размер 10-15 м. Лептоны не имеют составного строения, участвуют в слабых взаимодействиях (например электрон и нейтрино) Имеют размер 10-18 м.

Частицы, образующие поле Фотон – переносчик электромагнитного взаимодействия Глюон – переносчик сильного взаимодействия Бозон – переносчик слабого взаимодействия Гравитон – переносчик гравитационного взаимодействия

По продолжительности жизни стабильные (протон, электрон, нейтрино, фотон), остальные не стабильные! нестабильные (свободный нейтрон) и резонансы, самопроизвольно распадаются от 1000 секунд (для свободного нейтрона) до 10−22 сек. для резонансов.

Античасти ца Частица-двойник некоторой другой элементарной частицы, обладающая той же массой, но отличающаяся от неё знаком заряда. Электрон — античастица — позитрон — была открыта в 1932 году Протон — античастица — антипротон — была открыта в 1955 году В 1970 году открыт антигелий, а в 1998 году - антиводород, т.е. элементы антивещества или антиэлементы. Античастиц нет у фотона это истинно нейтральная частица

Взаимопревращения элементарных частиц 1.Распад нейтрона (Бета распад ): (нейтрон) n = p+ (протон) + e- (электрон) + (антинейтрино электронное) 2.При столкновении элементарных частиц с большой энергией рождаются другие частицы но всегда парами: Фотон + фотон = электрон e- + позитрон e+ 3. Аннигиляция (исчезновение вещества ): электрон e- + позитрон e+ = фотон (E=mc2) Частица+Античастица=Энергия Соотношение вещества и поля в материи: (вещество) : поле (фотоны) = 1 : 109

β − распад превращение нейтрона в протон, при этом испускаются электрон и антинейтрино:

Вещество как совокупность корпускулярных структур кварки нуклоны (протоны и нейтроны) атомные ядра атомы с их электронными оболочками

Строение атома Атом состоит из ядра атома и электронной оболочки В ядре атома сосредоточена практически вся масса атома и весь его положительный заряд. Ядро состоит из нуклонов – протонов и нейтронов ( p и n). Протон несет элементарный положительный заряд, нейтрон – частица незаряженная. Масса ядра не равна сумме масс протонов и нейтронов, входящих в него (т.н. «дефект масс»). Удержание протонов в ядре происходит за счет сильного взаимодействия
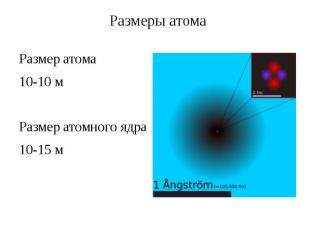
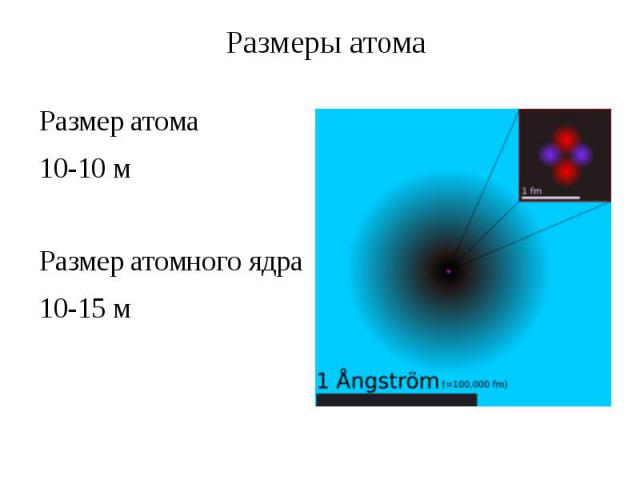
Размеры атома Размер атома 10-10 м Размер атомного ядра 10-15 м

Строение атома Число электронов в атоме равно порядковому номеру Z элемента в таблице Менделеева Число протонов равно числу электронов. Число нейтронов в ядре определяется следующим образом: NP = A – Z, где А – массовое число, т.е. целое число, ближайшее к атомной массе элемента в таблице Менделеева, Z – зарядовое число (число протонов).

Тема «Химические системы»

Химический элемент Для обозначения химических элементов применяется запись - ZXA где Х – символ химического элемента в таблице Менделеева, Z зарядовое число, A массовое число Первый химический элемент водород 1Н1: Зарядовое число Z =1, массовое число A=1 Второй химический элемент гелий 2Не4

Изотопы химических элементов Ядра с одинаковыми Z, но разными А называются изотопами. изотопы кальция: 20Са40(20p20n) 20Са42(20p22n) 20Са43(20p23n)

Организация электронных состояний атома в электронные оболочки Электронная оболочка атома — область пространства вероятного местонахождения электронов, характеризующихся значением главного квантового числа n, определяющим энергетический уровень электронов: Электронные уровни обозначаются буквами K, L, M, N, O, P, Q или цифрами от 1 до 7.

Организация электронных состояний атома в электронные оболочки n – главное квантовое число (энергетический уровень оболочки) l – орбитальное квантовое число (форма оболочки) m – магнитное квантовое число (направление движения) ms – спиновое квантовое число (собственное вращение электрона) Принцип Паули: в атоме может быть только один электрон с одинаковым набором значений квантовых чисел n, l, m, ms

Число электронов в оболочке на уровнях (n) и подуровнях (l )

Электронные конфигурации основного состояния элементов

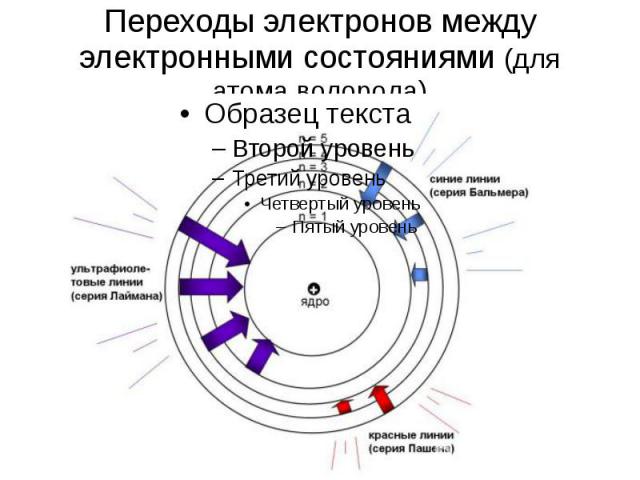
Переходы электронов между электронными состояниями Квантовое состояние с наименьшей энергией атома называют основным. Остальные квантовые состояния с более высоким уровнем энергии называют возбужденным. Когда атом находится в возбужденном состоянии, связь электрона с ядром ослабевает вплоть до отрыва электрона от атома. В основном состоянии атом может существовать неограниченно долго, а в возбужденном же состоянии – доли секунды.
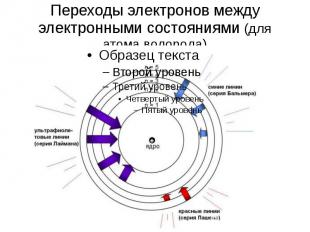
Переходы электронов между электронными состояниями (для атома водорода)

Вещества простые и сложные Простые – химические вещества, образованные атомами одного рода. О2 Вещества сложные (соединения) – химические вещества, образованные 2 или большим количеством атомов разного рода. Н2О - сложная молекула ДНК – сложная (полимерная) макромолекула

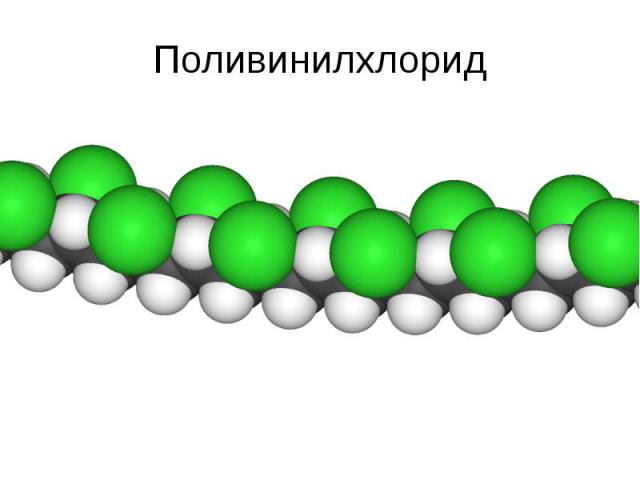
Полимеры и мономеры Полимеры – молекулы сложного строения, образованные последовательно связанными повторяющимися мономерными звеньями. Полимер – это высокомолекулярное соединение: количество мономерных звеньев в полимере (степень полимеризации) должно быть достаточно велико. Большинство полимеров на основе атома углерода Мономеры – мономерное звено входит в составе полимерной молекулы.
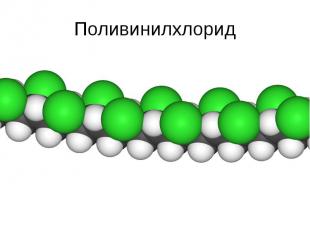
Поливинилхлорид

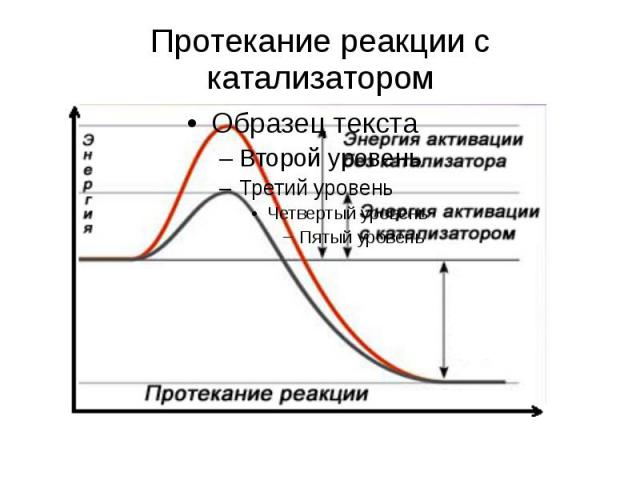
Катализаторы Химические вещества, ускоряющие скорость химических реакций, но не входящие в состав продуктов реакции. Биокатализаторы (ферменты или энзимы) обычно белковые молекулы, ускоряющие химические реакции в живых системах.
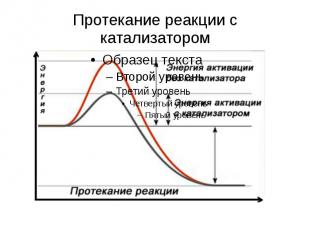
Протекание реакции с катализатором

Ферменты Отличительной особенностью ферментов по сравнению с небелковыми катализаторами является их высокая специфичность. При этом эффективность ферментов значительно выше эффективности небелковых катализаторов — ферменты ускоряют реакцию в миллионы и миллиарды раз, небелковые катализаторы — в сотни и тысячи раз. Например, одна молекула фермента ренина, содержащегося в слизистой оболочке желудка телёнка, створаживает около 106 молекул казеиногена (белка) молока за 10 мин при температуре 37 °C.

Ферменты

Тема «Особенности биологического уровня организации материи» Изучаются самостоятельно и рассматриваются на семинаре