Презентация на тему: Получение карбоновых кислот

Соли. Гаврилова Светлана Викторовна учитель химии МБОУ лицей «Престиж» городского округа Самара Презентация для учащихся 8 класса LOGO
Вопросы Кислоты Оксиды Физические и химические свойства солей, применение и получение Основания Определение и классификацию солей Задачи Тестовое задание Содержание План урока

Повторим гидроксид кальция щелочи голубую двухосновная, кислородсодержащая, сильная кислота содержание
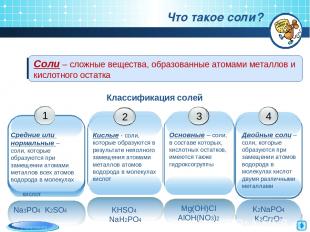
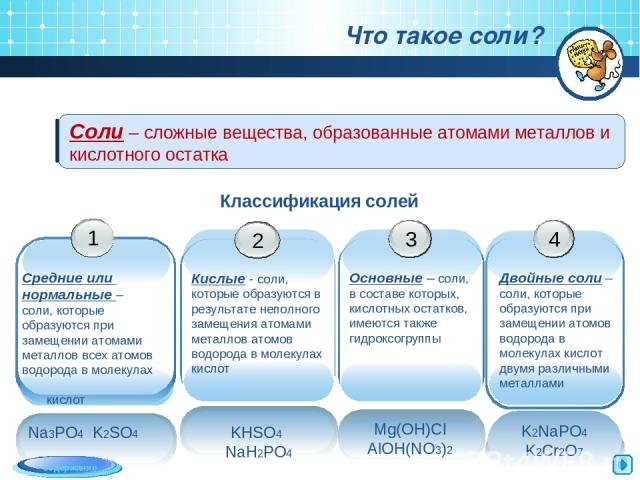
Соли – сложные вещества, образованные атомами металлов и кислотного остатка Что такое соли? Классификация солей Na3PO4 K2SO4 содержание

Свойства солей Физические свойства Соли - твердые вещества разного цвета. Растворимость их различна. Некоторые хорошо растворимы, например все нитраты. Другие же, например: CaCO3, BaSO4 - практически нерастворимы. Нитраты – все растворимы Сульфаты – все, кроме CaSO4, SrSO4, BaSO4, PbSO4, Ag2SO4 Хлориды – все, кроме AgCl, PbCl2 Сульфиды, карбонаты, силикаты, фосфаты – все соли нерастворимые, кроме солей K, Na и групп NH4 содержание

Химические свойства Соли реагируют с металлами ( исключения активные металлы: Li, Na, K, Ca, Ba - которые при обычных условиях реагируют с водой): Fe + CuSO4 = FeSO4 + Cu Соли реагируют с кислотами: Na2CO3 + 2HCl = 2NaCl + CO2 + H2O Карбонаты, сульфиты разлагаются при нагревании: СaCO3 = CaO + CO2 Некоторые соли способны реагировать с водой с образованием кристаллогидратов: CuSO4 + 5H2O = CuSO4 5H2O + Q

Соли реагируют с некоторыми кислотными оксидами: CaCO3 + SiO2 = CaSiO3 + CO2 Соли реагируют с неметаллами, стоящими в ряду, составленным Н. Н. Бекетовым правее, чем неметалл входящий в состав соли: 2NaBr + Cl2 = 2NaCl + Br2 Соли реагируют с другими солями с образованием новых нерастворимых солей: Na2SO4 + BaCl2 = BaSO4 + 2NaCl Соли реагируют с растворимыми основаниями с образованием нерастворимого основания: AlCl3 + 3KOH = Al(OH)3 + 3KCl

Получение солей Взаимодействие металлов и неметаллов: 2Fe + 3Cl2 = 2FeCl3 Взаимодействие кислотных оксидов с основными и амфотерными оксидами: CaO + CO2 = CaCO3 ZnO + SiO2 = ZnSiO3 Взаимодействие двух разных солей с образованием новой нерастворимой соли: Na2CO3 + CaCl2 = CaCO3 + 2NaCl Взаимодействие оснований и кислот: NaOH + HCl = NaCl + H2O 2Fe(OH)3 + 3H2SO4 = Fe2(SO4)3 +6H2O Ca(OH)2 + CO2 = CaCO3 + CO2 Взаимодействие более активного металла с солями: FeCl2 + Zn = ZnCl2 + Fe Действие кислот - неокислителей на металлы, стоящие в ряду напряжений металлов до водорода: Zn + 2HCl = ZnCl2 + H2 содержание
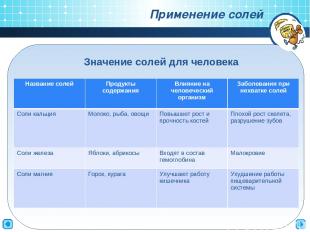
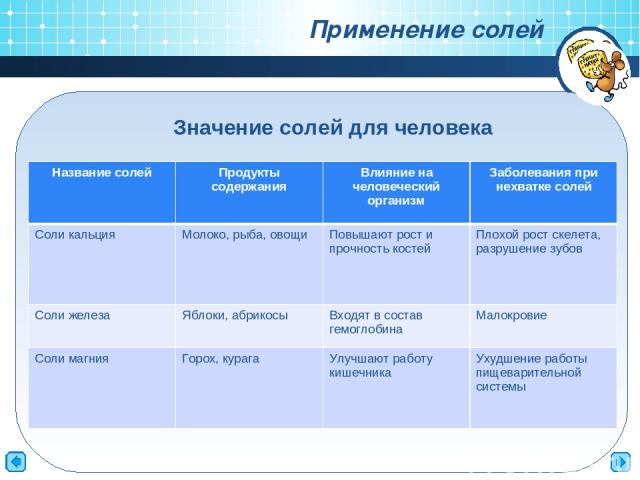
Применение солей Значение солей для человека Название солей Продукты содержания Влияние на человеческий организм Заболевания при нехватке солей Соли кальция Молоко, рыба, овощи Повышают рост и прочность костей Плохой рост скелета, разрушение зубов Соли железа Яблоки, абрикосы Входят в состав гемоглобина Малокровие Соли магния Горох, курага Улучшают работу кишечника Ухудшение работы пищеварительной системы

m = 18,8 г n = 0,1 моль Задачи содержание ответ

Дано: Решение: n (CuO) = 0,1 моль CuO + 2HNO3 = Cu(NO3)2 + H2O HNO3 n = 1 моль n = 1 моль _________________________ m (Cu(NO3)2) - ? n (CuO) = n (Cu(NO3)2 = 0,1 моль n (Cu(NO3)2) - ? m = n Х M M (Cu(NO3)2 = 64 + 2(14 + 3 Х16) = 188 (г/моль) m (Cu(NO3)2 = 0,1 моль Х 188 г/моль = 18,8 (г) Ответ: масса нитрата меди (II) равна 18,8 грамм, а его количество вещества – 0,1 моль. Решение задачи

СaCO3 = CaO + CO2 CaO + H2O = Ca(OH)2 Ca(OH)2 + CO2 = CaCO3 + H2O CaCO3 + 2HNO3 = Ca(NO3)2 + 2H2O Решение генетической цепочки

Список литературы Рудзитис Г. Е., Фельдман Ф. Г. Химия. Неорганическая химия. 8 класс: Учебник для общеобразовательных учреждений – М.: Просвещение, 2011. – 176 с. Презентация «Полупроводники» – Жуков В.В., учитель Новлянской СШ Заволжского района Ивановской области.