Презентация на тему: Железо

Железо

План: I. ЖЕЛЕЗО КАК ХИМИЧЕСКИЙ ЭЛЕМЕНТ. II. НАХОЖДЕНИЕ В ПРИРОДЕ И ПРИМЕНЕНИЕ ЖЕЛЕЗА III. ФИЗИЧЕСКИЕ СВОЙСТВА. IV. ХИМИЧЕСКИЕ СВОЙСТВА

i. как химический элемент Химический элемент VIII гр. Периодической системы Д.И. Менделеева. Атомный номер 26, атомная масса 55.847.

II. Нахождение в природе В земной коре железо распространено достаточно широко. На его долю приходится: Около 4,1% массы земной коры (4-е место среди всех элементов, 2-е среди металлов). Известно большое число руд и минералов, содержащих железо. По запасам железных руд Россия занимает первое место в мире. В морской воде 1·10–5 — 1·10–8% железа.
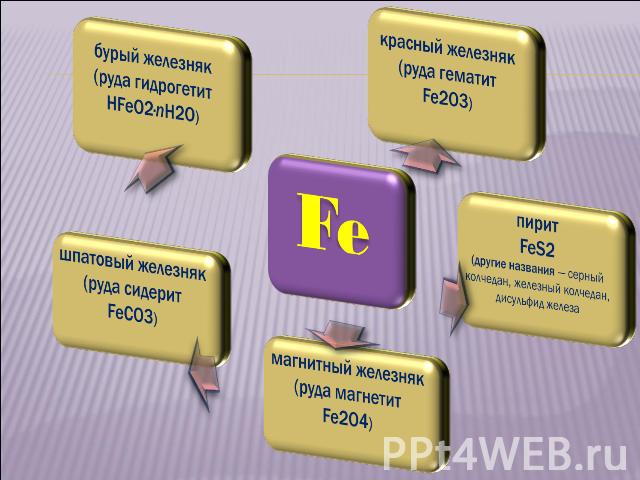
бурый железняк (руда гидрогетит НFeO2·nH2O) красный железняк (руда гематит Fe2O3) шпатовый железняк (руда сидерит FeСO3) магнитный железняк (руда магнетит Fe2O4) пирит FeS2 (другие названия — серный колчедан, железный колчедан, дисульфид железа Fe

бурый железняк (руда гидрогетит НFeO2 · nH2O) красный железняк(руда гематит Fe2O3)

шпатовый железняк (руда сидерит FeСO3) магнитный железняк (руда магнетит Fe2O4)
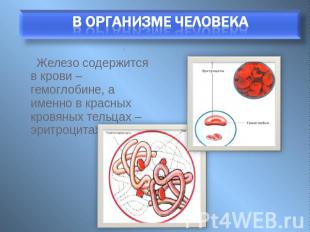
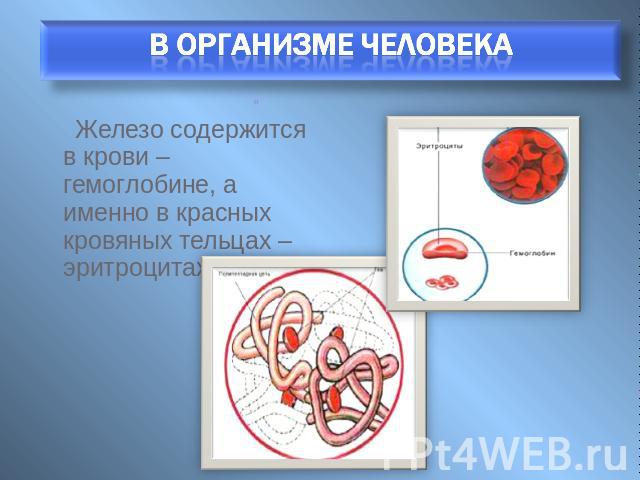
В организме человека Железо содержится в крови – гемоглобине, а именно в красных кровяных тельцах – эритроцитах.

В растениях Железо влияет на процесс фотосинтеза.

В быту человека Из железа изготавливают различные виды транспорта

В военной промышленности

Железо в истории В истории железо известно очень давно. из него изготовляли многое. Например доспехи, латы, оружие и т. д.

IiI. ФИЗИЧЕСКИЕ СЫВОЙСТВА Железо - сравнительно мягкий ковкий серебристо-серый металл. Температура плавления – 1535 0С Температура кипения около 2800 0С При температуре ниже 770 0С железо обладает ферромагнитными свойствами (оно легко намагничивается, и из него можно изготовить магнит). Выше этой температуры ферромагнитные свойства железа исчезают, железо «размагничивается».

Iv. Химические свойства Железо, отдавая два внешних электрона, проявляет степень окисления +2; отдавая три электрона (два внешних и один сверхоктетный с предпоследнего энергетического уровня), проявляет степень окисления +3.Fe-2e=Fe+2 Fe-3e=Fe+3 Электронные структуры 3d- и 4s-орбиталей атома железа и ионов Fe+2 и Fe+3 можно изобразить так:

Железо — активный металл.На воздухе образуется защитная оксидная пленка, препятствующая ржавению металла. 3Fe + 2O2 = Fe2O3 • FeO (Феррит железа) 2. Во влажном воздухе железо окисляется и покрывается ржавчиной, которая частично состоит из гидратированного оксида железа (III). 4Fe + 3О2 + 6Н2О = 4Fe(ОН)3

3. Взаимодействие с простыми веществами: 3.1 Горит в кислороде 3 Fe + 2 O2 =Fe3 O4 3.2 Реагирует с хлором 2Fe + 3 Cl2 = 2FeCl3 3.3 Взаимодействует с серой Fe + S = FeS

4.Железо вытесняет из растворов солей металлы, находящиеся в электрохимическом ряду напряжений правее железа:Fe + CuSO4 = FeSO4 + Cu 5. При высокой температуре (700-900°С) железо реагирует с парами воды: 3Fe+4Н2O=Fe3O4+4Н2

6. с кислотами: С соляной и разбавленной (приблизительно 20%-й) серной кислотами железо реагирует с образованием солей железа(II): Fe + 2HCl = FeCl2 + H2 Fe + H2SO4 = FeSO4 + H2 С концентрированными серной и азотной кислотами железо не реагирует. Эти кислоты создают на поверхности металла такую прочную и плотную пленку оксида, что металл становится совершенно пассивным и уже не вступает в другие реакции.Растворяется железо в разбавленной азотной кислоте. 8Fe+30HNO3=8Fe(NO3)3+3NH4NO3+9H2O

7. окисление железа При хранении водных растворов солей железа(II) наблюдается окисление железа(II) до железа(III): 4FeCl2 + O2 + 2H2O = 4Fe(OH)Cl2 8.Соединения железа (III) в растворах восстанавливаются металлическим железом: Fe + 2FeCl3 = 3FeCl2

Оксид железа 1. Проявляет основные свойства, взаимодействуя с кислотами: FeO+H2SO4 = FeSO4 + H2O 2. Оксид железа (III) проявляет слабые амфотерные свойства, взаимодействуя при нагревании с основными оксидами с образованием ферритов: МnO + Fe2O3 =Mn (FeO2)2
![Качественные реакции на ионы Fe2+ и Fe3+. FeSO4 + K3 [Fe(CN)6 ] = KFe +2 [Fe +3( Качественные реакции на ионы Fe2+ и Fe3+. FeSO4 + K3 [Fe(CN)6 ] = KFe +2 [Fe +3(](/images/150/8023/310/img20.jpg)
Качественные реакции на ионы Fe2+ и Fe3+. FeSO4 + K3 [Fe(CN)6 ] = KFe +2 [Fe +3(CN)6 ] + K2SO4 красная кровяная соль турнбулева синь FeCI3 + K4 [Fe(CN)6 ] = KFe+3 [Fe +2(CN)6 ] +3KCI желтая кровяная соль берлинская лазурь FeCI3 + 3 KCNS = Fe(CNS )3 +3KCI кроваво-красный

Когда открыто железо никто не знает и не узнает, так как это было слишком давно. Но пользуются железом до сих пор, и в настоящее время железо не заменимо в промышленности и труде.
1.http://images.yandex.ru/yandsearch?text=пирит фото&rpt=simage&img_url=vibrate.files.wordpress.com%2F2007%2F07%2Fpyrite.jpg%3Fw%3D556%26h%3D411&spsite=vibrate.wordpress.com&p 2.http://images.yandex.ru/yandsearch?rpt=simage&img_url=morethinking.files.wordpress.com%2F2009%2F08%2Fpyrite-fools-gold.jpg%3Fw%3D400%26h%3D334&text=%D0%BF%D0%B8%D1%80%D0%B8%D1%82%20%D1%84%D0%BE%D1%82%D0%BE&spsite=morethinking.wordpress.com&p=3 3. http://ru.wikipedia.org/wiki/Fe 4. http://all-met.narod.ru/fe.html 5. http://www.chem100.ru/elem.php?n=26 6.http://images.yandex.ru/yandsearch?ed=1&rpt=simage&text=%D1%85%D0%B8%D0%BC%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B5%20%D1%81%D0%B2%D0%BE%D0%B9%D1%81%D1%82%D0%B2%D0%B0%20%D0%B6%D0%B5%D0%BB%D0%B5%D0%B7%D0%B0&img_url=www.o8ode.ru%2Fimage%2Farticle%2F0001%2F20090509081505.jpg&spsite=fake-006-9684324.ru&p=0 7.http://images.yandex.ru/yandsearch?ed=1&rpt=simage&text=%D1%85%D0%B8%D0%BC%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B5%20%D1%81%D0%B2%D0%BE%D0%B9%D1%81%D1%82%D0%B2%D0%B0%20%D0%B6%D0%B5%D0%BB%D0%B5%D0%B7%D0%B0&img_url=www.catalogmineralov.ru%2Fpic%2F200842131005.jpg&spsite=fake-056-11462585.ru&p=53



















![Качественные реакции на ионы Fe2+ и Fe3+. FeSO4 + K3 [Fe(CN)6 ] = KFe +2 [Fe +3(CN)6 ] + K2SO4 красная кровяная соль турнбулева синь FeCI3 + K4 [Fe(CN)6 ] = KFe+3 [Fe +2(CN)6 ] +3KCI желтая кровяная соль берлинская лазурь FeCI3 + 3 KCNS = Fe(CNS )3 … Качественные реакции на ионы Fe2+ и Fe3+. FeSO4 + K3 [Fe(CN)6 ] = KFe +2 [Fe +3(CN)6 ] + K2SO4 красная кровяная соль турнбулева синь FeCI3 + K4 [Fe(CN)6 ] = KFe+3 [Fe +2(CN)6 ] +3KCI желтая кровяная соль берлинская лазурь FeCI3 + 3 KCNS = Fe(CNS )3 …](/images/150/8023/640/img20.jpg)