Презентация на тему: Законы газового состояния вещества


Ваша цель: 1.Познакомиться с молярным объемом газов; 2. Изучить основные законы химии: закон Авогадро, закон Гей – Люссака; 3. Научится решать типовые задачи;

Девиз урока: У пространства нет размера, а у знаний нет предела!

Проверка домашнего задания:

1. Что такое стехиометрия?

2. С какими законами вы познакомились на прошлом уроке?

3. В чем заключается сущность закона сохранения массы веществ?

4. Сформулируйте закон постоянства состава и укажите, для каких веществ он всегда строго выполняется?

5. Что такое массовая доля и как она рассчитывается?

1. Газовое состояние вещества:

Вопрос: В каких агрегатных состояниях могут находится вещества?

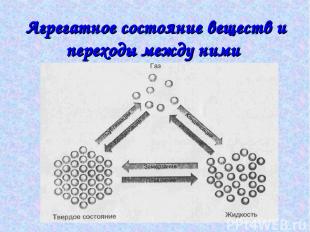
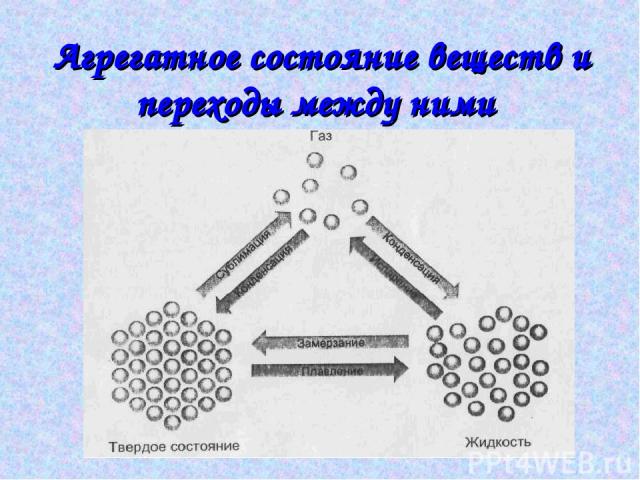
Агрегатное состояние веществ и переходы между ними

2. Закон Авогадро:

Амедео Авогадро высказал предположение в 1811 году, что в одинаковых объемах различных газов находится одно и тоже число молекул. Позже эта гипотеза стала законом Авогадро.

Закон Авогадро: В равных объемах различных газов при одинаковых условиях (температура, давление) содержится одинаковое число молекул.

Первое следствие из закона Авогадро: Одинаковое число молекул различных газов при одинаковых условиях занимают одинаковый объем.

3. Молярный объем газов:

Молярный объем газа Vm — величина, определяемая отношением объема данной порции газа V к химическому количеству вещества n в этой порции:

Нормальные условия: температура — 0°С давление — 101,325 кПа

Молярный объем любого газа при нормальных условиях: Второе следствие из закона Авогадро

Вычисление по уравнению реакции объема газа по известному химическому количеству одного из веществ

Задача: Какой объем водорода (н. у.) можно получить при действии соляной кислоты HCl на цинк химическим количеством 0,5 моль?

4. Закон объемных отношений (закон Гей-Люссака):

Гей-Люссак (1778-1850) При неизменных температуре и давлении объемы вступающих в реакцию газов относятся друг к другу, а также к объемам образующихся газообразных продуктов как небольшие целые числа.

Расчет объемных отношений газов по химических уравнениям

Обобщение Объем газов определяется не размером молекул, а расстоянием между ними, которые при одинаковых условиях для всех газов примерно одинаковы.

Задача: Найдите V хлора который потребуется для получения 80 г хлороводорода? какой V азота имеет такую же массу, что и 40,32 л NH3 (н.у.)?

В равных объемах различных газов при одинаковых условиях (давление, температура) содержится одинаковое число молекул.

Молярный объем газа есть объем его порции химическим количеством 1 моль. При нормальных условиях (температура 0°С и давление — 101,325 кПа) молярный объем любого газа является величиной постоянной, равной 22,4 дм3/моль.

Коэффициенты перед газообразными веществами в уравнениях химических реакций соответствуют объемным отношениям этих веществ.

Закрепление Какой V (при н. у.) занимают (I вариант) – любой газ химическим количеством 2 моль, (II - вариант) – азот массой 2 г.

I вариант Какой объем углерод (IV) – оксида можно получить действием избытка разбавленной серной кислоты на натрий-карбонат химическим количеством 0,35 моль? II вариант Какой объем кислорода потребуется для полного сжигания 200 дм3 (при н.у.) метана и какой объем углерод (IV)-оксида при этом образуется?

Оцените своё состояние после урока Мне хорошо Как всегда Уныло Я много знаю Я плохо понял и умею

Домашнее задание: § 5 стр. 29-32, 35-37. Упр. 1-7, 12.

Спасибо за внимание!