Презентация на тему: Обобщение по типам химических реакций

Обобщение по типам химических реакций

превращение одних веществ в другие. Вещества, полученные в результате реакции, отличаются от исходных веществ составом, строением и свойствами. Химическая реакция – Реагент 1 + Реагент 2 = Продукты

Признаки химических реакций Появление запаха Выделение газа Изменение окраски Выпадение осадка Растворение осадка Образование воды Выделение теплоты Поглощение теплоты

Классификация по тепловому эффекту Эндотермические – с поглощением тепла + Q Экзотермические – с выделением тепла - Q

Классификация по числу и составу исходных и образующихся веществ Реакции соединения: А + В = АВ Реакции разложения: АВ = А + В Реакции замещения: АВ + С = А + СВ Реакции обмена: АВ + CD = AD + CB

Тестовое задание. 1. Соотнесите: Тип реакции Схема реакции 1. замещения; а) 2 gO 2 g+O2 ; 2. обмена; б) 4AI + 3O2 2AI2O3 ; 3. соединения; в) 2KBr + CI2 2KCI + Br2 ; 4. разложения. г) Сu(OH)2 + 2HCI 2H2O+ CuCI2 . 2. В уравнении реакции, схема которой Fe2O3+ H2 Fe + H2O Коэффициент перед формулой железа равен: а) 3, б) 6, в) 2, г) 1. 2 3 6

3. Реакции, в результате которых из одного сложного вещества образуется несколько более простого состава относятся к: а) реакциям соединения; б) реакциям разложения; в) реакциям замещения; г) реакциям обмена. 4. Веществом «А» в схеме уравнения реакции является: Mg + HCI MgCI2 + А а) H2 б) CI2 в)Mg г) O2 2
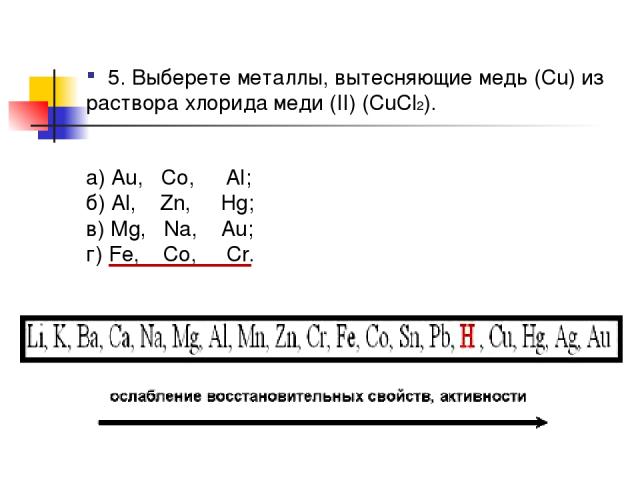
5. Выберете металлы, вытесняющие медь (Cu) из раствора хлорида меди (II) (CuCl2). а) Au, Co, Al; б) Al, Zn, Hg; в) Mg, Na, Au; г) Fe, Co, Cr.

6. По данным схемам реакций, запишите уравнения реакций. 1. Гидроксид меди (II) = оксид меди (II) + вода 2. Соляная кислота + цинк = хлорид цинка + водород 3. Хлорид бария + сульфат натрия = … 4. Оксид фосфора (V) + вода = …

6. Составьте уравнения последовательных реакций, используя подходящие реактивы: а) Ba → BaO → Ba(OH)2 → BaSO4 б) Al → Al2O3 → AlCl3 → Al(OH)3 → Al2O3

Домашнее задание Осуществите цепочку переходов S → SO2 → H2SO3 → Na2SO3 → SO2

Вычислите массу алюминия, необходимого для реакции с кислородом объемом 11,2 л. Схема реакции: 4Al + 3O2 → 2Al2O3