Презентация на тему: Виды химической связи

урок химии в 11 классе Учитель: Иванова Ирина Викторовна


Повторить теоретический материал по данному вопросу. Проделать упражнения из заданий ЕГЭ

Химическая связь – это такое взаимодействие атомов, которое связывает их в молекулы, ионы, радикалы, кристаллы. Различают четыре типа химических связей: ионную, ковалентную, металлическую и водородную.

это связь, возникающая между атомами за счет образования общих электронных пар. это связь, возникающая между атомами за счет образования общих электронных пар. По степени смещенности общих электронных пар к одному из связанных ими атомов ковалентная связь может быть полярной и неполярной.

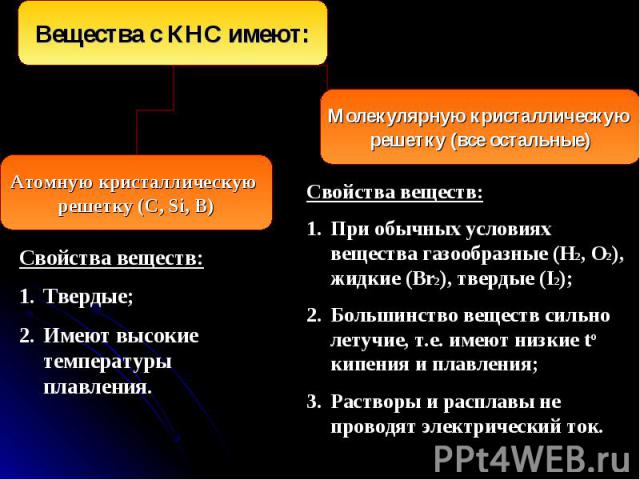
КНС образуют атомы одного и того же химического элемента. КНС образуют атомы одного и того же химического элемента. Механизм образования связи. Каждый атом неметалла отдает в общее пользование другому атому наружные неспаренные электроны. Образуются общие электронные пары. Электронная пара принадлежит в равной мере обоим атомам. Примеры образования КНС: H . + . H H : H H-H H2 .. .. .. .. : F . + . F : : F : F : F-F F2 .. .. .. .. . . : O : + : O : : O :: O : O=O O2 . . .. ..


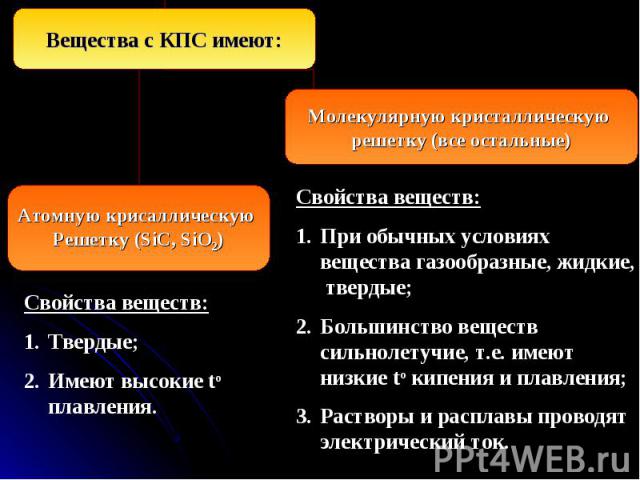
КПС образуют атомы разных неметаллов (с разной электороотрицательностью). Электроотрицательность (ЭО)- это свойство атомов одного элемента притягивать к себе электроны от атомов других элементов. КПС образуют атомы разных неметаллов (с разной электороотрицательностью). Электроотрицательность (ЭО)- это свойство атомов одного элемента притягивать к себе электроны от атомов других элементов. Самый электроотрицательный элемент – F. Механизм образования связи. Каждый атом неметалла отдает в общее пользование другому атому свои наружные неспаренные электроны. Образуются общие электронные пары. Общая электронная пара смещена к более электроотрицательному элементу. Примеры образования связи. .. .. + - H + . Cl H . Cl : H Cl + - Диполь .. ..


ИС образуется между атомами металлов и неметаллов, т.е. между атомами резко отличающимися друг от друга по электроотрицательности. ИС образуется между атомами металлов и неметаллов, т.е. между атомами резко отличающимися друг от друга по электроотрицательности. Механизм образования связи. Атом неметалла забирает наружные электроны у атома металла и превращается в анион (отрицательно заряженный ион). Атом металла теряет электроны и превращается в катион (положительно заряженный ион). Ионы связаны электростатическими силами. Пример образования связи. .. .. Na + . Cl : [ Na ] + [ . Cl : ]- или Na+ Cl- .. ..

Свойства веществ: Свойства веществ: Все вещества при обычных условиях твердые. Имеют высокие температуры кипения и плавления. Расплавы и растворы проводят электрический ток.

Металлическая связь – связь в металлах и сплавах, которую выполняют относительно свободные электроны между ионами металлов в металлической кристаллической решетке. Металлическая связь – связь в металлах и сплавах, которую выполняют относительно свободные электроны между ионами металлов в металлической кристаллической решетке. Схема образования металлической связи (М – металл): _ М0 – ne M n+ Свойства веществ: Твердость, ковкость, электрическая проводимость и теплопроводность, ковкость, пластичность, металлический блеск.

Водородная связь – связь между атомами водорода одной молекулы и сильноотрицательными элементами (O, N, F) другой молекулы. Водородная связь – связь между атомами водорода одной молекулы и сильноотрицательными элементами (O, N, F) другой молекулы. Примеры межмолекулярной водородной связи: … О - - Н + … О - - Н + … | | H + H + вода … О - - Н + … О - - Н + … | | + С2H5 + С2H5 этиловый спирт

Механизм возникновения связи: Механизм возникновения связи: Протон одной молекулы притягивается неподеленной электронной парой атома другой молекулы. Примеры веществ: водородные соединения F, O, N (реже Cl и S), спирт. Белки, нуклеиновые кислоты и др.

А-1 В каком ряду написаны вещества только с ковалентной полярной связью? А-1 В каком ряду написаны вещества только с ковалентной полярной связью? а) хлор, аммиак, хлороводород б) бромоводород, оксид азота (+2), бром в) сероводород, вода, сера г) иодоводород, вода, аммиак

1) сероводорода 2) азотной кислоты 3) озона 4) фторида кальция

1) ионная 2) металлическая 3) ковалентная полярная 4) ковалентная неполярная

1) различием в строении атомов углерода и кремния 2) различием в значениях масс молекул 3) разным видом химической связи 4) разным типом кристаллической решётки

1) ковалентная неполярная 2) ковалентная полярная 3) ионная 4) водородная 2

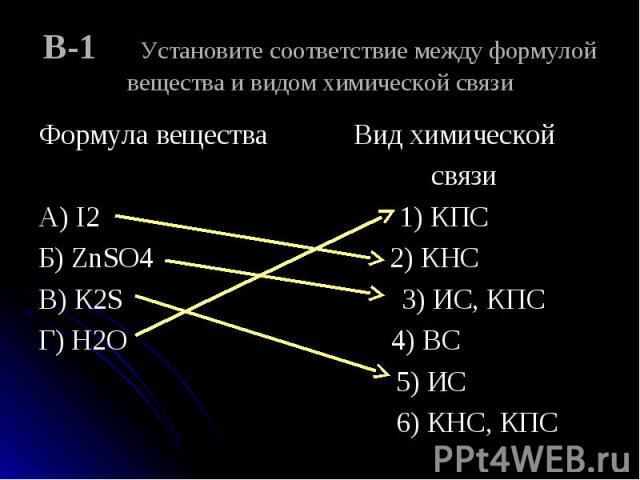
Формула вещества Вид химической Формула вещества Вид химической связи А) I2 1) КПС Б) ZnSO4 2) КНС В) К2S 3) ИС, КПС Г) Н2О 4) ВС 5) ИС 6) КНС, КПС
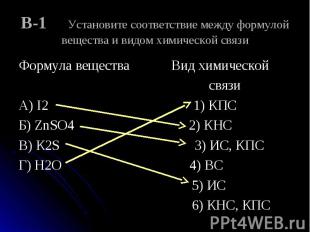
Формула вещества Вид химической Формула вещества Вид химической связи А) I2 1) КПС Б) ZnSO4 2) КНС В) К2S 3) ИС, КПС Г) Н2О 4) ВС 5) ИС 6) КНС, КПС



Повторить по записям виды хим.связи и типы кристаллических решёток Повторить по записям виды хим.связи и типы кристаллических решёток Придумать свой тест или сделать творческое задание по теме урока