Презентация на тему: УРОК в 8 классе основания

УРОК в 8 классе по теме: «Основания» Гудихина Светлана Рамилевна учитель химии и географии МБОУ «Кураловская СОШ с углубленным изучением отдельных предметов» Верхнеуслонского муниципального района РТ

1. Что такое бинарные соединения? 2. Какие классы неорганических веществ вам известны? 3.Что такое оксиды? 4. В каких агрегатных состояниях при нормальных условиях встречаются оксиды?

Задание выберите из перечня веществ ФОРМУЛЫ ОКСИДОВ . Дайте им названия. СuO CO2 Na2O Cu(OH)2 N2 KOH Cu(OH)2 AL(OH)3 CsOH Mg(OH)2 H2O Li2 O P2O5 Fe2O3

Тема урока: Основания Цель урока: познакомиться с новым классом веществ – основания изучить номенклатуру , классификацию , строение, свойства и применение оснований

Основания – сложные вещества, состоящие из атомов металла и одной или нескольких групп -ОН (гидроксильная группа). Общая формула – Ме(ОН)n где n – валентность металла.
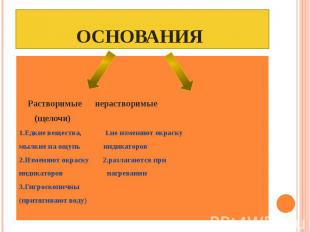
ОСНОВАНИЯ Растворимые нерастворимые (щелочи) 1.Едкие вещества, 1.не изменяют окраску мылкие на ощупь индикаторов 2.Изменяют окраску 2.разлагаются при индикаторов нагревании 3.Гигроскопичны (притягивают воду)

ЗАДАНИЕ: из выбранного перечня формул оснований выберите щелочи и нерастворимые основания, используя таблицу растворимости KOH Cu(OH)2 AL(OH)3 CsOH Mg(OH)2 Ca(OH)2 Zn(OH)2 Fe(OH)3 LiOH Cr(OH)2

получение оснований 1) Активный металл + вода: 2Na + 2H2O = 2NaOH + H2 2) Оксид активного металла + вода: CaO +H2O= Ca (OH)2 3)Нерастворимые основания получают путем реакции обмена между солями и щелочами: CuCl2 + 2NaOH = Cu(OH)2 + 2NaCl

действие индикаторов на щелочи в три пробирки с растворами гидроксида калия приливайте соответственно по каплям лакмус, метилоранж и фенолфталеин. Наблюдения запишите в тетради, сделайте вывод

химические свойства оснований взаимодействие с кислотами NaOH+HCL=NaCL+H2O взаимодействие щелочей кислотными оксидами NaOH+CO2=Na2 CO3+H2O разложение при нагревании нерастворимых оснований Cu(OH)2= CuO+H2O

В.1 Что такое основания? В.2 Какие по растворимости бывают основания? В.3 Каким оксидам соответствуют основания? Задание Составьте формулы гидроксидов, соответствующим им оксидам : K2O, BaO, Cr2O3. Дайте им названия.

Домашнее задание : §31 упр.1,3-4.

Используемая литература: 1.Андреева Л.С. Урок по теме «Основания». //Химия в школе. – 2009.- №3.- с. 30-32. 2. Гара, Н. Н. Химия. Уроки в 8 классе : пособие для учителя / Н. Н. Гара. - М. : Просвеще­ние, 2009. - 95 с. 3.Настольная книга учителя химии / авт.-сост. Н. Н. Гара, Р. Г. Иванова, А. А. Каверина. - М.: ACT : Астрель, 2002. - 190 с. 3. Рудзитис Г.Е., Фельдман. Химия. 8 класс. М: «Просвещение», 2008.-176с.