Презентация на тему: Неорганические и органические основания

Неорганические и органические основания. МБОУ «СОШ с.Озерки»учитель химии Добренькая Т.М.

Цель урока: обобщение, систематизация и углубление знаний о составе, классификации и свойствах оснований.

Основания - это… Основания —это сложные вещества, в состав которых входят атомы металла, связанные с одной или несколькими гидроксогруппами (в зависимости от степени окисления металла) Основания –это электролиты, которые образуют в качестве отрицательных ионов только гидроксид –анионы

Согласно протолитической теории Брёнстеда-Лоури основания-это молекулы или ионы, которые являются акцепторами катионов водорода.

Классификация оснований 1. Растворимые в воде основания (щёлочи) 2. Малорастворимые в воде гидроксиды 3. Нерастворимые в воде основания Деление на растворимые и нерастворимые основания практически полностью совпадает с делением на сильные и слабые основания, или гидроксиды типичных и не типичных металлов.

Выполните задание. Выберите среди предложенных веществ основания: C2 H5 OH , NH3, Al(OH)2Cl, NaOH, Ca(OH)2 , Cu(OH)2 , Cu(OH)2 CO3 , CH3 –NH2 Выберите бескислородные основания: NH3 , NaOH, Ca(OH)2 , Cu(OH)2 CH3 –NH2 Выберите нерастворимые и малорастворимые основания: NH3 , NaOH, Ca(OH)2 , Cu(OH)2 , CH3 –NH2 Выберите двухкислотные основания :NH3 , NaOH, Ca(OH)2 , Cu(OH)2 , CH3 –NH2 Выберите однокислотные основания : NH3 , NaOH, Ca(OH)2 , Cu(OH)2 , CH3 –NH2 Запишите ответы в тетради. 1) NH3, NaOH, Ca(OH)2 , Cu(OH)2 , CH3 –NH2 2) NH3 , CH3 –NH2 3) Ca(OH)2 , Cu(OH)2 4) Ca(OH)2 , Cu(OH)2 5) NH3, NaOH, CH3 –NH2 Оцените свой результат после проверки!

Свойства растворимых оснований 1) Изменяют окраску индикаторов 2) Взаимодействие с кислотными оксидами Ca(OH)2 + CO2 = CaCO3 + H2O 3)Взаимодействие с кислотами Щёлочь + Кислота = Соль + Вода -реакция обмена (нейтрализация) Са(OH)2 + 2HNO3 = Ca(NO3)2 + 2H2O 4) С растворами солей, если в результате образуется осадок или газ Соль (раствор) + Щёлочь = Нерастворимое основание↓ + Новая соль FeCI3 + 3NaOH = Fe(OH)3↓ + 3NaCl 2NH4 Cl+Ca(OH)2 =CaCl2 +2NH3↑ +2H2 O 5)С амфотерными оксидами и гидроксидами 2NaOH+Al2 O3 =2NaAlO2 +H2O 2КOH+Zn(OH)2=K2 ZnO2+2H2O

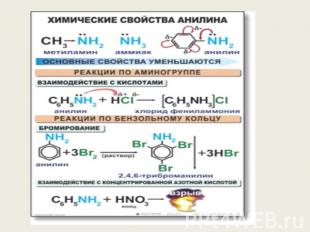

химические свойства аминов Основные свойства: а)СН3 NH2 + H2O = СН3 NH3OH Этиламин гидроксид метиламмония б)(С 2Н5)2 NH + HСl = (С 2Н5)2 NH2Cl Диэтиламин хлориддиэтил аммония

Проверьте ваши знания Ответы: I. Вариант II. Вариант 1.-2 1.-1 2.-3 2.-2 3.-4 3.-3 4.-1 4.-4 5.-2 5.-2 6.-3 6.-3

Практическое значение оснований

Домашнее задание Для учащихся, сдающих ЕГЭ по химии . § 21 № 2,5, 7, по учебнику «Химия 11класс» Профильный уровень . О.С.Габриелян, Г.Г.Лысова Для учащихся, не сдающих ЕГЭ по химии. § 23 №4, 5а,7 по учебнику «Химия 11класс» Базовый уровень . О.С.Габриелян,