Презентация на тему: Обучающая программа по химии


Обучающая программа для 8 класса «Периодический закон и Периодическая система химических элементов Д. И. Менделеева»


Биография Д. И. Менделеева Д. И. Менделеев родился 27 января 1834 года в г. Тобольске в семье директора Тобольской гимназии Ивана Павловича Менделеева и его жены Марии Дмитриевны. В 1849 г. Митя окончил Тобольскую гимназию. В 1850 г. Менделеевы переехали в Петербург. В конце лета 1850 г., после вступительных экзаменов, Дмитрий Менделеев был зачислен на физико-математический факультет Главного педагогического института. Он увлекался математикой, химией и физикой, интересовался предметами историко-философского факультета, а на старших курсах уделял большое внимание химии и минералогии. Его первой значительной исследовательской работой, выполненной под руководством профессора А. А. Воскресенского при выпуске из института, стала диссертация «Изоморфизм в связи с другими отношениями кристаллической формы при различии в составе». В 1855 г. Д. И. Менделеев окончил институт с золотой медалью, получил диплом старшего учителя. В 1855 - 1856 гг. работал учителем гимназии при Ришельевском лицее в Одессе. С 1857 -1890 гг. преподавал в Петербургском университете, одновременно с 1864 по 1872 год работал профессором Технологического института в Петербурге. Кроме того, Д.И. Менделеев был преподавателем Владимировских и Бестужевских женских курсов. В 1857 г. Д.И. Менделеев защитил диссертацию на тему «Удельные объемы». В 1859 - 1861 г. Менделеев был в заграничной командировке где, работал в основном в организованной им лаборатории в Гейдельберге.

Биография Д. И. Менделеева Вернувшись в Петербург, Менделеев погрузился в активную педагогическую, исследовательскую и литературную работу. В 1860 г. открыл «температуру абсолютного кипения жидкостей». В 1861 г. написал первый в России учебник по органической химии, удостоенный престижной Демидовской премии. Тесно связаны с вопросами технологии перегонки первые работы Менделеева по переработке нефти. В 1863 году он посетил нефтеперегонные предприятия в Сураханах вблизи Баку, где в те годы применялась технология, сходная с перегонкой древесины, дал ряд важных рекомендаций, касающихся условий транспортировки нефти. В 1865 г. он защищает докторскую диссертацию на тему «О соединении спирта с водой». В 1867 г. Д.И. Менделеев впервые стал читать курс неорганической химии в Петербургском университете. Тогда и родился замысел написать учебник «Основы химии» - фундаментальный труд Д. И. Менделеева. Учебник выдержавший только при жизни автора восемь изданий. В ходе работы над 1-м изданием Д.И. Менделеев пришел к идее о периодической зависимости свойств химических элементов от их атомных весов. В 1869-1871 гг. изложил основы учения о периодичности свойств химических элементов, открыл периодический закон – фундаментальный закон природы и разработал периодическую систему химических элементов. На основе открытого им закона Д.И. Менделеев впервые предсказал (1870) существование и свойства 11 не открытых еще

Биография Д. И. Менделеева элементов, в том числе «экаалюминия» — галлия (открыт в 1875 г.), «экабора» — скандия (1879 г), «экасилиция» — германия (1886 г.), свойства которых прогнозировал с исключительной точностью и очень подробно. Последним из одиннадцати (1940) был открыт элемент № 85, предсказанный ученым экаиод, известный сегодня под названием астат. Выход «Основ химии» был значительным событием научной жизни России того времени. Появились восторженные отзывы в официальных журналах, коллеги выражали свою оценку в письмах к Д. И. Менделееву. Кроме того, «Основы химии» были переведены на английский, французский и немецкий языки. Учебником пользовались студенты и ученые многих стран Европы, а также Соединенных Штатов Америки. Число читателей было исключительно велико — от гимназистов до академиков. Молодые ученые брали в «Основах химии» идеи, которые затем нередко развивали в своих трудах в течение многих лет. В качестве примера можно указать на известного металлурга академика А. А. Байкова и крупного радиохимика В. А. Бородовского, которые приобщились к химии благодаря учебнику Д.И.Менделеева, или на академика А. Е. Арбузова, которого заинтересовали сведения о производных фосфористой кислоты, что послужило толчком для исследований в этой области и возникновению новой области химии — химии фосфорорганических соединений . Изучая газы, вывел в 1874 г. общее уравнение состояния идеального газа (уравнение Клапейрона - Менделеева).

Биография Д. И. Менделеева Высказал в 1877 г. гипотезу о неорганическом происхождении нефти из карбидов тяжелых металлов; предложил принцип дробной перегонки при переработке нефти. Д. И. Менделеев принимал участие в разработке технологий запущенного в 1879 г. первого в России завода по производству машинных масел в посёлке Константиновский в Ярославской губернии, который ныне носит его имя. Работы Менделеева по изучению свойств газов инициировали его интерес к проблемам в области геофизики и метеорологии. Разрабатывая эти вопросы, Менделеев заинтересовался исследованиями атмосферы (особенно ее верхних слоев) с помощью летательных аппаратов. 7-го августа 1887 г. Менделеев совершил полет на воздушном шаре. За совершение этого полёта Д.И. Менделеев был удостоен медали Французского общества воздухоплавания. В 1888 г. выдвинул идею о подземной газификации углей. Разработал в 1891-1892 г. технологию изготовления нового типа бездымного пороха. В 1892 г. — Дмитрий Иванович Менделеев — учёный-хранитель Депо образцовых гирь и весов, которое в 1893 г. по его инициативе было преобразовано в Главную палату мер и весов. Разнообразие интересов Менделеева поражают: он собирал и систематизировал фотографии, любил фотографировать сам. Коллекционировал репродукции произведений искусства, виды мест, в которых бывал. Еще одним увлечением Д.И. Менделеева было изготовление чемоданов и рамок для портретов. До последних дней великий ученый трудился на благо своей Родины.

Биография Д. И. Менделеева 20 января 1907 г. Дмитрий Иванович Менделеев скончался. Похоронили его на Волковом кладбище в Петербурге. На траурной процессии люди несли огромный транспарант с изображением Периодической системой. Его заслуги высоко оценены во всем мире. Д.И. Менделеев был избран членом и почетным членом более 90 академий наук, научных обществ, университетов и институтов разных стран мира. Имя Д.И. Менделеева носят химический элемент № 101, город Менделеевск в Татарстане, минерал, кратер на обратной стороне Луны, подводный горный хребет, Научно-исследовательский институт метрологии, Российский химико-технологический университет, вулкан и др. Вопросы

Вопрос №1

Молодец! Молодец!

Вопрос №2

Молодец! Молодец!

Вопрос №3

Молодец! Молодец!

Вернись обратно Вернись обратно

Вопрос №4

Молодец! Молодец!

Вопрос №5

Молодец! Молодец!

Вопрос №6

Молодец! Молодец!

Вопрос №7

Молодец! Молодец!

Вопрос №8

Молодец! Молодец!

Вопрос №9

Молодец! Молодец!

Вопрос №10

Молодец! Молодец!

Вопрос №11

Молодец! Молодец!

Вопрос №12

Молодец! Молодец!

Молодец! Молодец! Ты ответил на все вопросы данного раздела правильно!


Классификация химических элементов до Д. И. Менделеева Многие учёные до Д. И. Менделеева предприняли попытки классификации химических элементов. Ко времени открытия Периодического закона были известны 63 химических элемента, описаны не только состав и свойства их многочисленных соединений, но и подмечены некоторые закономерности в их изменении. Было до 50 попыток классификации химических элементов. Одна из первых классификаций элементов основывалась на их распределении на металлы и неметаллы по общими физическим свойствам. Выдающийся шведский химик Йенс Якоб Берцелиус разделил все элементы на металлы и неметаллы на основе различий в свойствах, образованных ими простых веществ и соединений. Он определил, что металлам соответствуют основные оксиды и основания:Na→Na2O→NaOH, а неметаллам - кислотные оксиды и кислоты: S →SO2→H2SO3. Но групп было всего две, они были велики, включали значительно отличающиеся друг от друга элементы. Наличие амфотерных оксидов и гидроксидов у некоторых металлов вносило путаницу. Классификация была несовершенной. Каждый химический элемент весьма индивидуален по своей природе, но, в то же время, между отдельными элементами имеются сходные признаки. Основываясь на них немецкий учёный Иоганн Вольф Дёберейнер в 1829 г. предпринял значимую попытку классификации элементов. Он заметил, что некоторые сходные по свойствам элементы можно объединить по 3 в группы, которые он назвал триадами, триады Дёберейнера. Разделил элементы по три на основе сходства в свойствах

Классификация химических элементов до Д. И. Менделеева образуемых им веществ так, чтобы величина, которую мы сейчас понимаем как относительную атомную массу элемента, была равна среднему арифметическому масс двух крайних элементов в триаде: М (Na) = ( 7 + 39 ) / 2 = 23 г/моль. Несмотря на то, что триады Дёберейнера в какой-то мере являются прообразами менделеевских групп, эти представления в целом ещё слишком несовершенны. Отсутствие магния в едином семействе кальция, стронция и бария или кислорода в семействе серы, селена и теллура является результатом ограничения совокупностей сходных элементов лишь тройственными союзами. Очень показательна в этом смысле неудача Дёберейнера выделить триаду из четырех близких по своим свойствам элементов: P, As, Sb, Bi. Дёберейнер отчётливо видел глубокие аналогии в химических свойствах фосфора и мышьяка, сурьмы и висмута, но, заранее ограничив себя поисками триад, он не смог найти верного решения. Хотя разбить все известные элементы на триады Дёберейнеру, естественно, не удалось, закон триад явно указывал на наличие взаимосвязи между атомной массой и свойствами элементов и их соединений. Все дальнейшие попытки систематизации основывались на размещении элементов в соответствии с их атомными массами. А. Бегье де Шанкуртуа профессор Парижской высшей школы. В 1862 г. Александр Бегье де Шанкуртуа предложил расположить все известные в то время химические элементы в единой последовательности возрастания их атомных масс и полученный ряд наносил на поверхность

Классификация химических элементов до Д. И. Менделеева цилиндра по линии, исходящей из его основания под углом 45° к плоскости основания (т. н. земная спираль). При развертывании поверхности цилиндра оказывалось, что на вертикальных линиях, параллельных оси цилиндра, находились химические элементы со сходными свойствами. Недостатком спирали А. Бегье де Шанкуртуа было то обстоятельство, что на одной линии с близкими по своей химической природе элементами оказывались при этом и элементы совсем с другими химическими свойствами. Так, на одну вертикаль попадали литий, натрий, калий; бериллий, магний, кальций; кислород, сера, селен, теллур и т. д. В группу щелочных металлов попадал марганец, в группу кислорода и серы — ничего общего с ними не имеющий титан. Английский учёный Джон Ньюлендс в 1865 г. сделал попытку сопоставить химические свойства элементов с их атомными массам. Расположив элементы в порядке возрастания их атомных масс, Ньюлендс заметил, что сходство в свойствах проявляется между каждым восьмым элементом. Найденную закономерность Ньюлендс назвал законом октав по аналогии с семью интервалами музыкальной гаммы. В своей таблице он располагал химические элементы в вертикальные группы по семь элементов в каждой и при этом обнаружил, что (при небольшом изменении порядка некоторых элементов) сходные по химическим свойствам элементы оказываются на одной горизонтальной линии. Джон Ньюлендс, безусловно, первым дал ряд элементов, расположенных в порядке

Классификация химических элементов до Д. И. Менделеева возрастания атомных масс, присвоил химическим элементам соответствующий порядковый номер и заметил систематическое соотношение между этим порядком и физико-химическими свойствами элементов. Он писал, что в такой последовательности повторяются свойства элементов, эквивалентные веса (массы) которых отличаются на 7 единиц, или на значение, кратное 7, т. е. как будто бы восьмой по порядку элемент повторяет свойства первого, как в музыке восьмая нота повторяет первую. Ньюлендс пытался придать этой зависимости, действительно имеющей место для лёгких элементов, всеобщий характер. В его таблице в горизонтальных рядах располагались сходные элементы, однако в том же ряду часто оказывались и элементы совершенно отличные по свойствам. Кроме того, в некоторых ячейках Ньюлендс вынужден был разместить по два элемента; наконец, таблица не содержала свободных мест. Лотар Майер немецкий химик в 1864 г. расположил химические элементы в порядке увеличения их атомных масс и по валентности, появилась первая таблица химических элементов. В неё были включены 28 элементов, размещённые в шесть столбцов.

Классификация химических элементов до Д. И. Менделеева Майер намеренно ограничил число элементов в таблице, чтобы подчеркнуть закономерное (аналогичное триадам Дёберейнера) изменение атомной массы в рядах сходных элементов. Недостаток был в том, что в его таблицу входило всего 28 химических элементов, т.е. меньше половины известных в то время. По мере того как число химических элементов возрастало, учёные стали предпринимать попытки выделить из их числа естественные семейства элементов со сходными свойствами. Так были выделены щелочные металлы, щелочноземельные металлы, халькогены, галогены.

Классификация химических элементов до Д. И. Менделеева Классификация на естественные группы не объединяла химические элементы в единое целое, т. е. классификация оставалась несовершенной. Ни одна из попыток классификации химических элементов до Д. И. Менделеева не привела к созданию системы, отражающей взаимосвязь элементов и выявляющей природу их сходства и различия. Классификация химических элементов до Д. И. Менделеева была неточной, ненаучной, несовершенной, т. к. за основу классификации бралось не главное свойство («коренной признак») химического элемента. Вопросы

Вопрос №1

Молодец! Молодец!

Вопрос №2

Молодец! Молодец!

Вопрос №3

Молодец! Молодец!

Вопрос №4

Молодец! Молодец!

Вопрос №5

Молодец! Молодец!

Вопрос №6

Молодец! Молодец!

Вопрос №7

Молодец! Молодец!

Вопрос №8

Молодец! Молодец!

Вопрос №9

Молодец! Молодец!

Вопрос №10

Молодец! Молодец!

Вопрос №11

Молодец! Молодец!

Вопрос №12

Молодец! Молодец!

Молодец! Молодец! Ты ответил на все вопросы данного раздела правильно!

Вернись обратно Вернись обратно

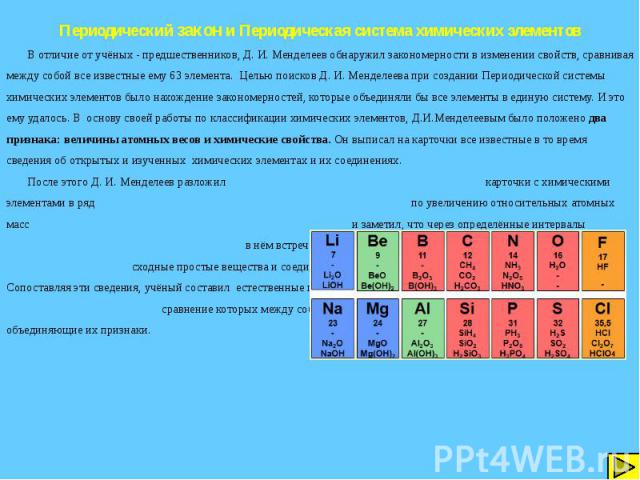
Периодический закон и Периодическая система химических элементов В отличие от учёных - предшественников, Д. И. Менделеев обнаружил закономерности в изменении свойств, сравнивая между собой все известные ему 63 элемента. Целью поисков Д. И. Менделеева при создании Периодической системы химических элементов было нахождение закономерностей, которые объединяли бы все элементы в единую систему. И это ему удалось. В основу своей работы по классификации химических элементов, Д.И.Менделеевым было положено два признака: величины атомных весов и химические свойства. Он выписал на карточки все известные в то время сведения об открытых и изученных химических элементах и их соединениях. После этого Д. И. Менделеев разложил карточки с химическими элементами в ряд по увеличению относительных атомных масс и заметил, что через определённые интервалы в нём встречаются элементы, которые образуют сходные простые вещества и соединения. Сопоставляя эти сведения, учёный составил естественные группы сходных по свойствам элементов, сравнение которых между собой показало, что даже элементы несходных групп имеют объединяющие их признаки.

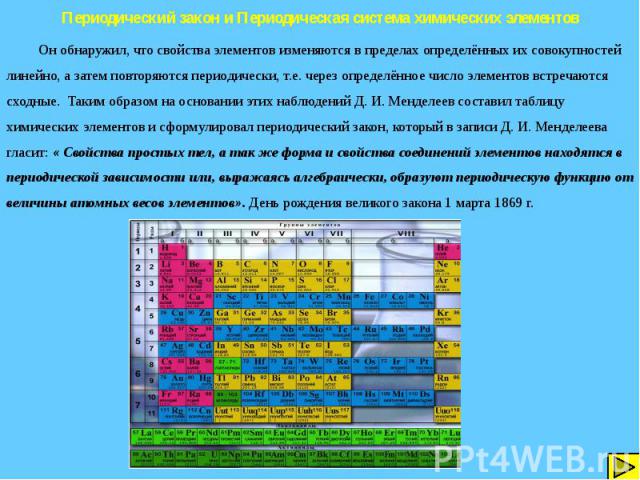
Периодический закон и Периодическая система химических элементов Он обнаружил, что свойства элементов изменяются в пределах определённых их совокупностей линейно, а затем повторяются периодически, т.е. через определённое число элементов встречаются сходные. Таким образом на основании этих наблюдений Д. И. Менделеев составил таблицу химических элементов и сформулировал периодический закон, который в записи Д. И. Менделеева гласит: « Свойства простых тел, а так же форма и свойства соединений элементов находятся в периодической зависимости или, выражаясь алгебраически, образуют периодическую функцию от величины атомных весов элементов». День рождения великого закона 1 марта 1869 г.
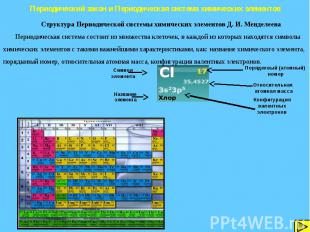
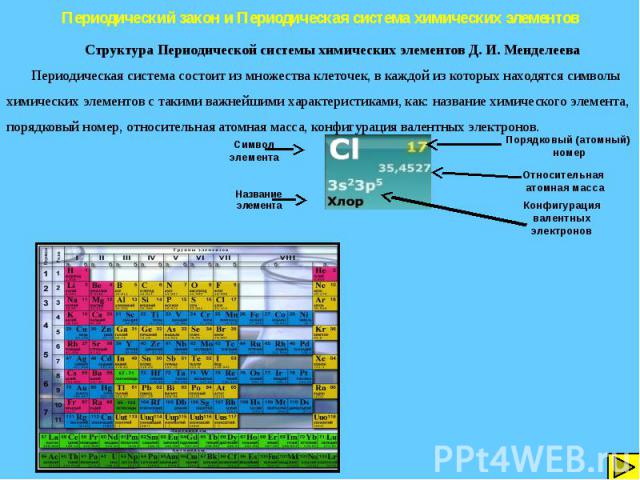
Периодический закон и Периодическая система химических элементов Структура Периодической системы химических элементов Д. И. Менделеева Периодическая система состоит из множества клеточек, в каждой из которых находятся символы химических элементов с такими важнейшими характеристиками, как: название химического элемента, порядковый номер, относительная атомная масса, конфигурация валентных электронов.

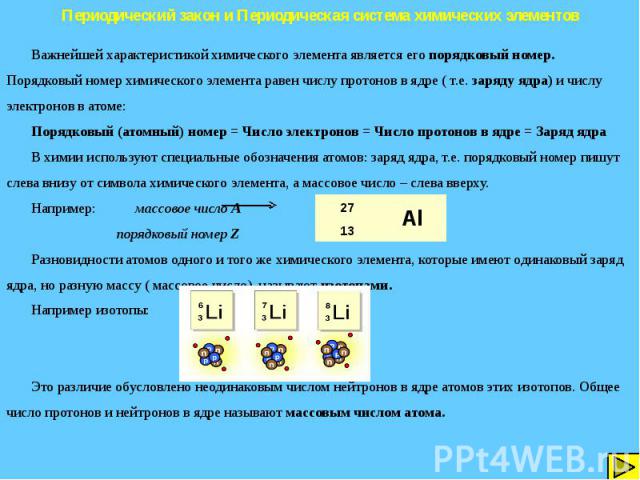
Периодический закон и Периодическая система химических элементов Важнейшей характеристикой химического элемента является его порядковый номер. Порядковый номер химического элемента равен числу протонов в ядре ( т.е. заряду ядра) и числу электронов в атоме: Порядковый (атомный) номер = Число электронов = Число протонов в ядре = Заряд ядра В химии используют специальные обозначения атомов: заряд ядра, т.е. порядковый номер пишут слева внизу от символа химического элемента, а массовое число – слева вверху. Например: массовое число А порядковый номер Z Разновидности атомов одного и того же химического элемента, которые имеют одинаковый заряд ядра, но разную массу ( массовое число), называют изотопами. Например изотопы: Это различие обусловлено неодинаковым числом нейтронов в ядре атомов этих изотопов. Общее число протонов и нейтронов в ядре называют массовым числом атома.

Периодический закон и Периодическая система химических элементов Число нейтронов (N) = Массовое число (A) - Число протонов (Z) Для того чтобы рассчитать число нейтронов в атоме, необходимо взять округлённое значение массового числа в ПСХЭ или в таблице изотопов и вычесть заряд ядра, который равен порядковому номеру. Например Al: массовое число (А) = 27, заряд ядра (Z) = 13, тогда число нейтронов равно N = 27 – 13 = 14 Периодическая система химических элементов представляет собой таблицу, в которой выделяют периоды и группы. Период – это горизонтальный ряд химических элементов , расположенных в порядке возрастания их атомных масс, начинающийся с щелочного металла (или с водорода для 1-го периода) и заканчивающийся благородным газом. Различают: 1) малые периоды (1, 2, 3) – состоят из 1-ого ряда. В первом периоде 2 химических элемента , во втором и третьем по восемь. 2) большие периоды (4-7) – состоят из 2-х рядов. Содержат по 18 и более химических элементов. Седьмой период не завершён, в настоящее время не все предсказанные для этого периода химические элементы (№№ 113-118) открыты учеными.

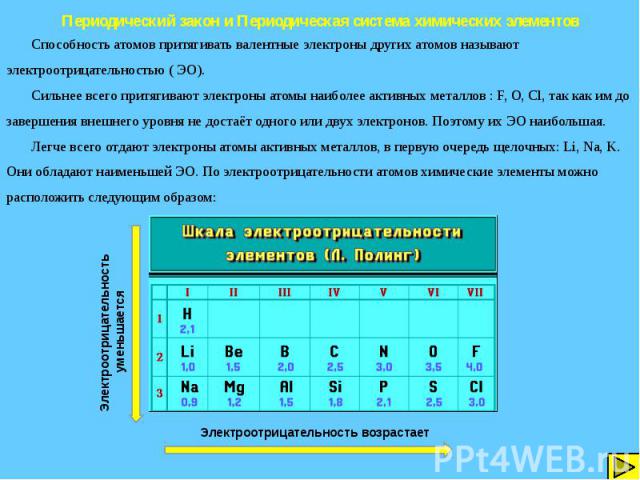
Периодический закон и Периодическая система химических элементов Изменение химических свойств в периода Свойства элементов, а так же образованных ими простых веществ и соединений в пределах периода закономерно изменяются. В каждом периоде с увеличением порядкового номера химического элемента заряд ядра и число валентных электронов в атомах последовательно возрастают. Валентные электроны – это электроны, которые обладают наибольшей энергией. Число валентных электронов равно номеру группы, в которой находиться химический элемент. I. Радиус атомов в периоде слева на право уменьшается, а притяжение электронов к ядру увеличивается:

Периодический закон и Периодическая система химических элементов
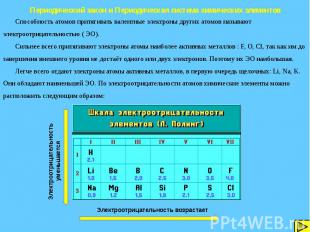
Периодический закон и Периодическая система химических элементов

Периодический закон и Периодическая система химических элементов

Периодический закон и Периодическая система химических элементов Значение Периодического закона - Его открытие дало мощнейший толчок в развитии физических и химических знаний; - Были разработаны теории строения атома и химической связи. Благодаря Периодической системе химических элементов Д. И. Менделеева - Сложилось современное понятие о химическом элементе; - Были уточнены представления о простых веществах и соединениях; - Появление периодической системы открыло новую, научную эру в истории химии и ряде смежных наук, появилась естественная система химических элементов, на основе которой стало возможным обобщать, делать выводы, предвидеть свойства химических элементов, способов их получения и строения их атомов. Периодический закон и Периодическая система химических элементов Д. И. Менделеева являются основой современной химии. Они относятся к таким научным закономерностям, которые отражают явления, реально существующие в природе, и поэтому никогда не потеряют своего значения свойств. «Периодическому закону будущее не грозит разрушением, а только надстройка и развитие обещаются» Д. И. Менделеев


Вопрос №1

Молодец! Молодец!

Вопрос №2

Молодец! Молодец!

Вопрос №3

Молодец! Молодец!

Вопрос №4

Молодец! Молодец!

Вопрос №5

Молодец! Молодец!

Вопрос №6

Молодец! Молодец!

Вопрос №7

Молодец! Молодец!

Вопрос №8

Молодец! Молодец!

Вопрос №9

Молодец! Молодец!

Вопрос №10

Молодец! Молодец!

Вопрос №11

Молодец! Молодец!

Вопрос №12

Молодец! Молодец!

Вопрос №13

Молодец! Молодец!

Вопрос №14

Молодец! Молодец!

Вопрос №15

Молодец! Молодец!

Вопрос №16

Молодец! Молодец!

Вопрос №17

Молодец! Молодец!

Вопрос №18

Молодец! Молодец!

Вопрос №19

Молодец! Молодец!

Вопрос №20

Молодец! Молодец!

Вопрос №21

Молодец! Молодец!

Молодец! Молодец! Ты ответил на все вопросы данного раздела правильно!

Вернись обратно Вернись обратно

Список источников основного содержания http://ru.wikipedia.org/wiki/%CF%E5%F0%E8%EE%E4%E8%F7%E5%F1%EA%E0%FF_%F1%E8%F1%F2%E5%EC%E0_%F5%E8%EC%E8%F7%E5%F1%EA%E8%F5_%FD%EB%E5%EC%E5%ED%F2 http://festival.1september.ru/articles/550165/ http://festival.1september.ru/articles/518766/ http://festival.1september.ru/articles/518545 http://festival.1september.ru/articles/subjects/4?page=59.

Список источников иллюстраций http://school1174.ru/about/news/Konkurs_Uchenik_goda/ мальчик в очках http://900igr.net/kartinki/russkij-jazyk/Slovarnye-slova-trenazhjor/014-E.html мальчик с карандашом и с книгой http://www.liveinternet.ru/showjournal.php?journalid=3371375&keywordid=1220333 книга с очками, бумага с чернильницей и пером, книга с бумагой и чернильницей http://www.liveinternet.ru/users/4652061/post259349852 химические элементы (фон 1 и 2-ого слайда) http://piqoge.teleskoro.ru/63743.html мальчик за партой, мальчик сидит с книгами, мальчик идёт с книгами, мальчик и рядом вопросительный знак http://gorinalw.3dn.ru/index/vitaminy/0-66 птица с книгами http://www.freetorg.com.ua/lead/search/?q=%E6%E8%E4%EA%EE%F1%F2%E5%E9&p=7 http://prodlenka93.ru/ мальчик сидит за столом с тетрадями,учебниками о чёч-то думает

Список источников иллюстраций http://alexlat.ucoz.ru/_pu/12/49704461.jpg Д.И.Менделеев (цветное фото) http://rudocs.exdat.com/docs/index-226819.html?page=3 картинка опыты системы элементов http://fcior.edu.ru/card/3875/otkrytie-periodicheskogo-zakona.html (информационный модуль) учёные:Берцелиус, Ньюлендс, Дёберейнер, Шанкуртуа, таблички с химическими элементами http://aksakal.info/science-news/21389-v-tablice-mendeleeva-poyavitsya-element-nazvannyy-v-chest-moskvy.html жёлтая картинка с химическими элементами http://h2o.u-sonic.ru/teor/teors/pic3_1.htm шкала электроотрицательности элементов по Полингу http://turservice-ram.ru/i/bg/referati/tematicheskoe-planirovanie-po-himii-11-klass-1-chas-gabrielyan.html на картинке 2 колбы,учебник и доска http://900igr.net/kartinki/khimija/Viktorina/082-1911-g.-God-rozhdenija-atomnoj-fiziki-a-XX-vek-atomnyj-vek.html орбитали слайд 117

Список источников иллюстраций http://www.liveinternet.ru/users/4491121/post180303977/ человек с пробиркой (слайд 13) http://45.ru/forum/theme.php?id=599508 человечек с указкой на книге http://www.doodoo.ru/smiles/verybig/vb070.gif смайлик показывает класс анимация http://www.doodoo.ru/smiles/verybig/vb061.gif смайлик читает книгу анимация http://www.sapo.biz.pl/ang/18/isotopes-in-nuclear-symbol-notation изотопы лития http://physik.ucoz.ru/photo/atomnaja_i_jadernaja_fizika/26 изотопы водорода http://900igr.net/fotografii/khimija/Jod-v-organizme-cheloveka/004-Jod.html иод http://www.topic.lt/miru_mir/173999-kniga-vseobshhix-zabluzhdenij.-chast-2.-30-foto.html атомы (слайд 119) http://ru.wikipedia.org/wiki/%CC%E5%ED%E4%E5%EB%E5%E5%E2,_%C4%EC%E8%F2%F0%E8%E9_%C8%E2%E0%ED%EE%E2%E8%F7 родители Д.И. Менделеева (4 слайд)

Список источников иллюстраций http://www.omgtu.ru/general_information/institutes/petrochemical_institute/department_of_quot_physical_chemistry_quot/the_teaching_process_1.php колба http://forum.homka-spb.com/lite/referati/magazin-uchebnikov-angliyskogo-yazika.html три книги http://zhigyly.org/page-shkola-molodie-g-moskvi колба и химические элементы http://byfly.ws/lastnews/page/82/ Периодическая система химических элементов Д.И.Менделеева http://www.km.ru/referats/73E0B0ECE2154735977663F7FE9DAECE табличка с химическими элементами (в центре магний) http://school20.hostedu.ru/ незнайка http://www.liveinternet.ru/showjournal.php?journalid=1547340&keywordid=426618&page=5 сова (анимация) http://ostx.pp.ua/kak-sdelat-lazernuyu-ukazku.html сова с указкой http://wap.mobilmusic.ru/fileanim.html?id=855462 книга (анимация) http://koledj.ru/docs/index-6579.html уравнение состояния идеального газа

Список источников иллюстраций http://for-foto.ru/661-klipart-knigi.html лист с пером и чернильницей http://ivan-off.com/vektornyj-klipart/page/6/ Земля http://rc983.com/cgi/medal медаль http://oblichitel.ru.com/razdeli/yagodi/kak-pravilno-narisovat-frukti-yagodi.html нарисованные горы http://good-in.ru.com/?s=t&g=%D0%92%D0%B5%D1%81%D0%B5%D0%BB%D0%B0%D1%8F+%D1%85%D0%B8%D0%BC%D0%B8%D1%8F колбы и стаканчик с палочкой