Презентация на тему: "Типы химических реакций

«Типы химических реакций»

ЦЕЛЬ УРОКА:

Вопросы для повторения Что изучает химия? Что такое химические превращения или химические реакции? Каковы признаки химических реакций?

ГОРЕНИЕ СВЕЧИ Признак химической реакции: выделение тепла и света

Реакция между раствором хлорида кальция и раствором щелочи.

Действие индикаторов на растворы кислоты, щелочи и воды.

Реакция между раствором перманганата калия и раствором хлорида хрома (II)

Реакция между раствором хлорида железа (III) и раствором щелочи.

ГОРЕНИЕ СТАЛЬНОЙ ПРОВОЛОКИ В КИСЛОРОДЕ Признак химической реакции: выделение тепла и света

РЕАКЦИЯ МЕДИ С АЗОТНОЙ КИСЛОТОЙ Признак химической реакции: выделение бурого газа

Условия, необходимые для осуществления химической реакции: Соприкосновение веществ Перемешивание веществ Определенная температура

Вопросы для повторения Что такое химическое уравнение? Какие реакции называются реакциями соединения? Какие реакции называются реакциями разложения? Какие реакции называются реакциями замещения? Какие реакции называются реакциями обмена?

Типы химических реакций: Соединение Разложение Замещение Обмен

Реакция соединения. А

Реакция соединения. Cu

Реакция разложения А

Реакция разложения H2

Реакция замещения А

Реакция замещения Fe

Реакция обмена A

Реакция обмена Ag

С какими типами химических реакций мы сегодня познакомились? Соединение Разложение Замещение Обмен

Определите типы реакций

Определите типы реакций Cu + CI2 → CuCI2 2Fe + 3CI2 → 2FeCI3

Определите типы реакций

Определите типы реакций SiO2 + Mg → MgO + Si SiO2 + 2Mg → 2MgO + Si Реакция замещения
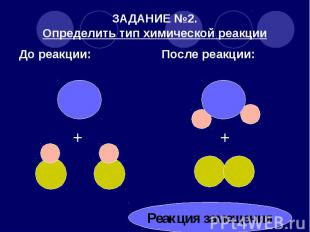
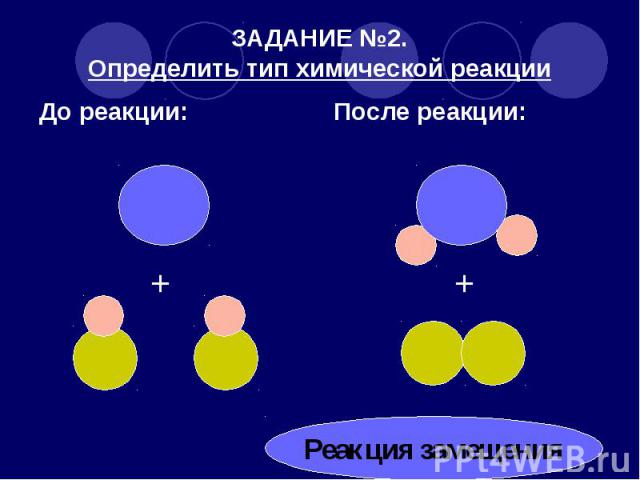
ЗАДАНИЕ №2. Определить тип химической реакции

Игра «ТРЕТИЙ ЛИШНИЙ-1» 1. 2NaCl = 2Na + Cl2 2. CaO + CO2 = CaCO3 3. C + O2 =CO2

Игра «ТРЕТИЙ ЛИШНИЙ-2» 1.2CuO + C = 2Cu + O2 2. 2NO + O2 = 2NO2 3. Mg +H2S = MgS + H2

ЗАДАНИЕ Царь зовет к себе Стрельца - удалого молодца И дает ему поручение государственного значения: «Чтоб я стал очень богат, нужен мне алюминия сульфид Ночь даю тебе подумать, утром буду ждать доклад! Не смогешь – кого винить? Должен я тебя казнить. Запиши себе названье, чтоб со страху не забыть».

AI + S = AI2S3

Лабораторная работа

Техника безопасности
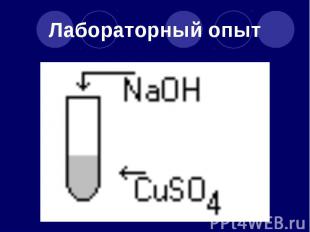
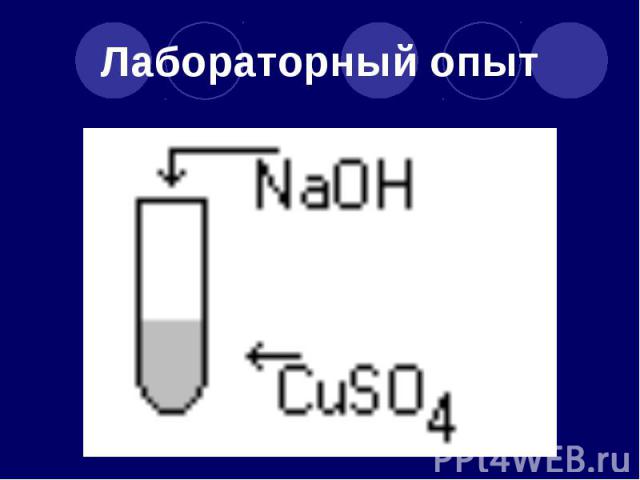
Лабораторный опыт

Напишите уравнение реакции и определите тип реакции CuSO4 + NaOH → Cu(OH)2 + Na2SO4 CuSO4 + 2NaOH → Cu(OH)2 + Na2SO4 Тип реакции – реакция обмена

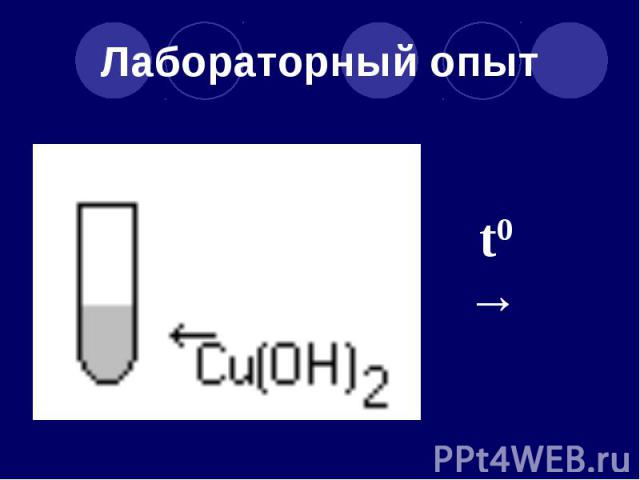
Лабораторный опыт

Напишите уравнение реакции и определите тип реакции

Проверочная работа

Задание № 1 Расставьте коэффициенты и определите тип реакции в следующих уравнениях реакций:

1 вариант Расставьте коэффициенты и определите тип реакции в следующих уравнениях реакций: А) Cu + O2 =; Б) NaOH + HNO3 =; В) H2 + CuO =; Г) Ag2O =; Д) MgO + HF=.

2 вариант Расставьте коэффициенты и определите тип реакции в следующих уравнениях реакций: А) Ва + O2 =; Б) KOH + H3PO4 =; В) H2 + FeO =; Г) HgO =; Д) BaO + HBr =.

1 вариант 2. Приведены схемы реакций. Составьте уравнения химических реакций, расставьте коэффициенты и укажите их тип: а) нитрат серебра + хлорид железа (III) → → хлорид серебра + нитрат железа (III); б) гидроксид свинца (II) → оксид свинца (II) + вода.

2 вариант 2. Приведены схемы реакций. Составьте уравнения химических реакций, расставьте коэффициенты и укажите их тип: а) нитрат бария + сульфат натрия → → сульфат бария + нитрат натрия; б) оксид лития + вода → гидроксид лития.

1 вариант 3. Выберите на ваш взгляд, правильный ответ. В реакциях обмена могут образоваться: а) несколько простых веществ; б) два сложных вещества; в) одно сложное вещество; г) одно простое вещество.

2 вариант 3. Выберите на ваш взгляд, правильный ответ. В реакции замещения могут вступать: а) одно простое и одно сложное вещество; б) одно сложное вещество; в) несколько простых веществ; г) несколько сложных веществ.

Проверка выполненной работы

1 вариант А) 2Cu + O2 = 2CuO – соединение Б) NaOH + HNO3 = NaNO3 + H2O – обмен В) Н2 + FeO = Fe + Н2O - замещение Г) 2Ag2O= 4Ag + O2 – разложение Д) MgO + 2HF = MgF2 + H2O - обмен А) 3AgNO3 + FeCI3 = 3AgCI +Fe(NO3)3 (обмен) Б) Pb(OH)2 = PbO + H2O (разложение) Ответ: Б

2 вариант А) 2Ва + O2 = 2ВаO – соединение Б) 3КOH + H3РО4 = К3РO4 + 3H2O – обмен В) H2 + FeO = Fe +H2O – замещение Г) 2HgO= 2Hg + O2 – разложение Д) ВаO + 2HВr = BaBr2 + H2O - обмен А) Ва(NO3)2 + FeCI 3 = 3AgCI +Fe(NO3)3 (обмен) Б) Li2O + H2O = 2LiOH (соединение) Ответ: А

Домашнее задание: § 29; § 30, упр. 1 (а, б); § 31, упр. 2 (в, г, д); § 32, упр. 3, 4 (г, д, е).

Что вам сегодня понравилось на уроке? Что вам сегодня понравилось на уроке?

Спасибо за работу на уроке!