Презентация на тему: Алкины


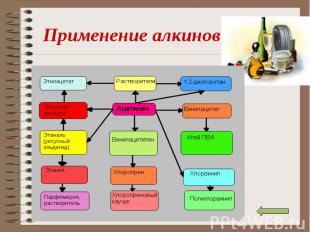
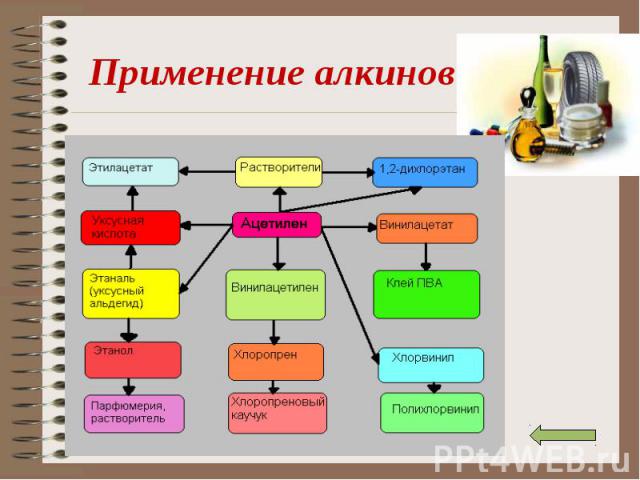
Понятие о непредельных углеводородах. Понятие о непредельных углеводородах. Характеристика тройной связи. Изомерия и номенклатура алкинов. Физические свойства. Получение алкинов. Свойства алкинов. Применение алкинов.

Алкины – углеводороды, содержащие в молекуле одну тройную связь между атомами углерода, а качественный и количественный состав выражается общей формулой Алкины – углеводороды, содержащие в молекуле одну тройную связь между атомами углерода, а качественный и количественный состав выражается общей формулой СnН2n - 2, где n ≥ 2. Алкины относятся к непредельным углеводородам, так как их молекулы содержат меньшее число атомов водорода, чем насыщенные.

Вид гибридизации – sp Вид гибридизации – sp Валентный угол – 180 Длина связи С = С – 0,12 нм Строение ─ линейное Вид связи – ковалентная полярная По типу перекрывания – δ и 2 π



C2H2 C2H2 C3H4 C4H6 C5H8 C6H10 C7H12


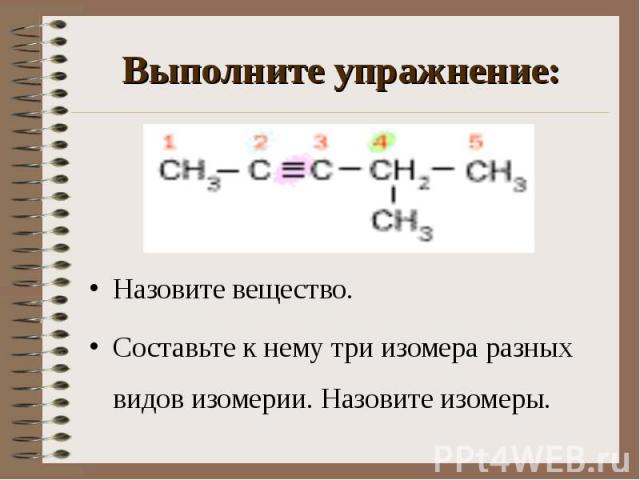
Назовите вещество. Назовите вещество. Составьте к нему три изомера разных видов изомерии. Назовите изомеры.

Температуры кипения и плавления алкинов, так же как и алкенов, закономерно повышаются при увеличении молекулярной массы соединений. Температуры кипения и плавления алкинов, так же как и алкенов, закономерно повышаются при увеличении молекулярной массы соединений. Алкины имеют специфический запах. Они лучше растворяются в воде, чем алканы и алкены.


Химические свойства ацетилена и его гомологов в основном определяются наличием в их молекулах тройной связи. Наиболее характерны для алкинов реакции присоединения. Химические свойства ацетилена и его гомологов в основном определяются наличием в их молекулах тройной связи. Наиболее характерны для алкинов реакции присоединения.

1. Галогенирование 1. Галогенирование Обесцвечивание бромной воды является качественной реакцией на все непредельные углеводороды

2. Гидрогалогенирование. 2. Гидрогалогенирование. 3. Гидрирование. 4. Гидратация.


При сгорании (полном окислении) ацетилена выделяется большое количества тепла: При сгорании (полном окислении) ацетилена выделяется большое количества тепла: HC CH + 2О2 2СО2 + Н2О + Q


1. Димеризация под действием водного раствора CuCl и NH4Cl: 1. Димеризация под действием водного раствора CuCl и NH4Cl: НC CH + НC CH Н2C=CH C CH (винилацетилен) 2. Тримеризация ацетилена над активированным углем приводит к образованию бензола (реакция Зелинского): С, 600 С 3НC CH С6H6 (бензол)