Презентация на тему: Сера и её производные

Сера. Сероводородная, серная и сернистая кислоты. 900igr.net

Сера Сера – халькоген, довольно активный неметалл. Сущетсвует три аллотропных модификации серы: ромбическая S8 пластическая моноклинная

Характеристика серы Сера в ПСХЭ: положение (период, группа) строение атома свойства элемента по периоду / в главной п/гр высший оксид высший гидроксид ЛВС

Получение При сливании растворов сероводородной и сернистой кислот: H2SO3 + 2H2S = 3S + 3H2O При неполном сгорании сероводорода (при недостатке воздуха): 2H2S + O2 = 2S + 2H2O

Химические свойства Не смачивается и не реагирует с водой. Как окислитель реагирует с: металлами (кроме золота) Hg + S = HgS (обезвреживание разлитой ртути) водородом и неметаллами, у которых с.о. меньше (углеродом, фосфором и т.п.)

Химические свойства Как восстановитель реагирует с: кислородом хлором фтором
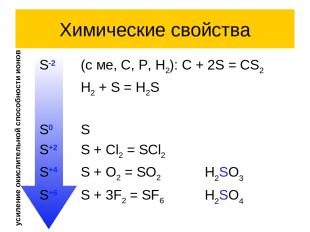
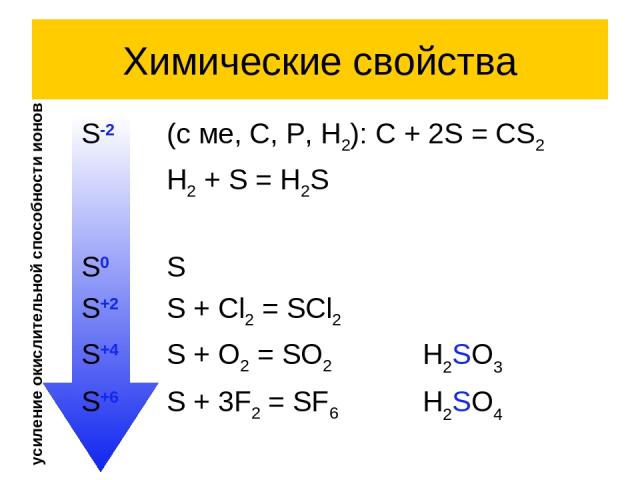
Химические свойства S-2 (с ме, C, P, H2): C + 2S = CS2 H2 + S = H2S S0 S S+2 S + Cl2 = SCl2 S+4 S + O2 = SO2 H2SO3 S+6 S + 3F2 = SF6 H2SO4 усиление окислительной способности ионов

Сероводород H2S – сероводород. Его раствор в воде называется сероводородной кислотой. Кислота слабая двухосновная, поэтому диссоциирует ступенчато: I: H2S ↔ H+ + HS– II: HS– ↔ H+ + S–

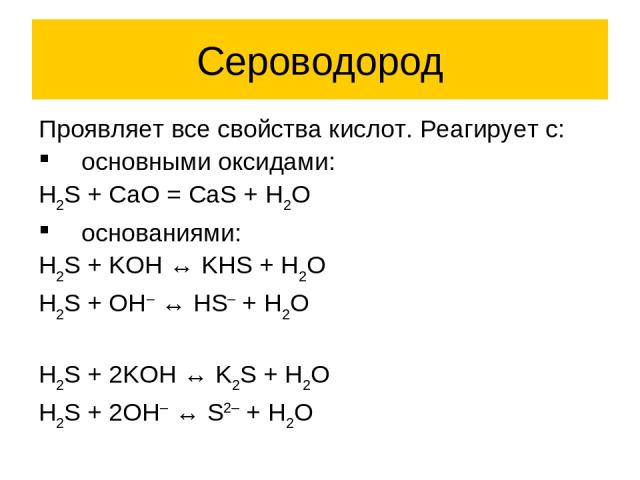
Сероводород Проявляет все свойства кислот. Реагирует с: основными оксидами: H2S + CaO = CaS + H2O основаниями: H2S + KOH ↔ KHS + H2O H2S + OH– ↔ HS– + H2O H2S + 2KOH ↔ K2S + H2O H2S + 2OH– ↔ S2– + H2O

Сероводород солями: CuCO3 + H2S = CuS + H2CO3 металлами: Ca + H2S = CaS + H2↑

Свойства солей Кислые соли сероводородной кислоты – гидросульфиды (KHS, NaHS) хорошо растворимы в воде. Растворимыми также являются сульфиды щелочных и щёлочноземельных металлов. Сульфиды остальных металлов в воде нерастворимы, а сульфиды меди, свинца, серебра, ртути и др. тяжёлых ме нерастворимы даже в кислотах (кроме азотной).

Окисление сероводорода Сероводород легко окисляется кислородом (как при избытке O2 и недостатке?). Бромной водой Br2: H2S + Br2 = 2HBr + S↓ желто- оранжевая бесцветная

Оксид серы (IV) SO2 – сернситый газ. Реагирует с водой с образование H2SO3. Типичный кислотный оксид. Взаимодействует с основаниями (образуется соль (сульфит или гидросульфит) и вода) и основными оксидами (образуется только соль).

Оксид серы (IV) Получают: горением серы обжигом пирита действием кислот на сульфиты взаимодействием конц. серной кислоты и тяжелых ме
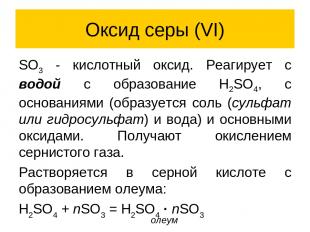
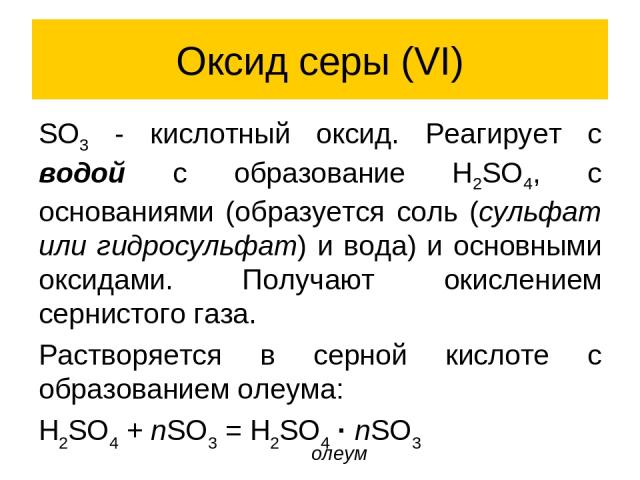
Оксид серы (VI) SO3 - кислотный оксид. Реагирует с водой с образование H2SO4, с основаниями (образуется соль (сульфат или гидросульфат) и вода) и основными оксидами. Получают окислением сернистого газа. Растворяется в серной кислоте с образованием олеума: H2SO4 + nSO3 = H2SO4 · nSO3 олеум

Серная кислота Серная кислота H2SO4 – тяжёлая маслянистая жидкость без запаха и цвета. При концентрации > 70% – серная кислота называется концентрированной, менее 70% - разбавленной. Диссоциация серной кислоты выражается уравнением: H2SO4 ↔ 2H+ + SO42–

Серная кислота Кислота реагирует с амофотерными и основными оксидами и гидроксидами, солями: H2SO4 + BaCl2 = BaSO4↓ + HCl Последняя реакция является качественной на SO42– ион (образуется нерастворимый осадок белого цвета).
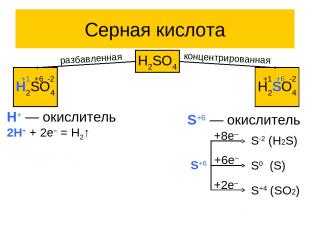
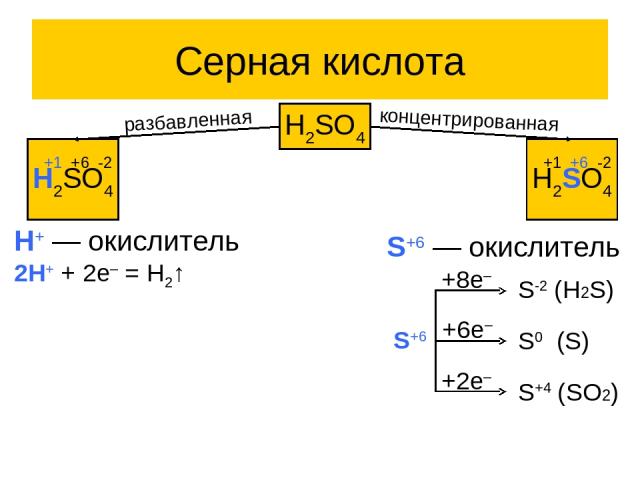
Серная кислота H2SO4 H2SO4 +1 +6 -2 H2SO4 +1 +6 -2 разбавленная концентрированная H+ ― окислитель 2H+ + 2e– = H2↑ S+6 ― окислитель S+6 +8e– +6e– +2e– S-2 (H2S) S0 (S) S+4 (SO2)

Серная кислота C разбавленной серной кислотой реагируют все металлы, стоящие в ряду активности до водорода. При реакции образуется сульфат металла и выделяется водород: H2SO4 + Zn = ZnSO4 + H2↑ Металлы, стоящие после водорода с разбавленной кислотой не реагируют: Cu + H2SO4 ≠

Концентрированная серная кислота Металлы, стоящие в ряду активности после водорода, взаимодействуют с концентрированной серной кислотой по следующей схеме: H2SO4(конц.) + Ме = МеSO4 + SO2↑ + H2O Т.е. образуются: сульфат металла оксид серы(IV) - сернистый газ SO2 вода

Концентрированная серная кислота Более активными ме серная кислота при определённых условиях может восстанавливаться до серы в чистом виде или сероводорода. На холоде конц. серная кислота пассивирует железо и алюминий, поэтому их перевозят в железных цистернах: H2SO4(конц.) + Fe ≠ (на холоде)

Получение серной кислоты получение SO2 (обычно обжигом пирита) окисление SO2 в SO3 в присутсвии катализатора – оксида ванадия(V) растворение SO3 в серной кислоте с получением олеума

Сульфаты Соли серной кислоты имеют все свойства солей. Особенным является их отношение к нагреванию: сульфаты активных ме (Na, K, Ba) не разлагаются даже при t > 1000˚C другие (Cu, Al, Fe) даже при небольшом нагревании распадаются на оксид серы(VI) и оксид металла

Вопросы в каких реакциях сера играет роль окислителя? восстановителя? какие степени она при этом проявляет? чем обусловлено различие свойств концентрированной и разбавленной серной кислоты? напишите уравнения реакции конц. и разбавленной кислот с медью и цинком. как отличить растворы иодида натрия и сульфата натрия? предложите два способа и напишите уравнения реакций в молекулярном и ионном видах.

Задания Какое кол-во сернистого газа можно получить из 10 кг руды, содержащей 48% пирита? Какой объем занимают: а) 4 моль SO2? б) 128 г SO3? Осуществите реакции: O2 → S → SO2 → SO3 → H2SO4 → Na2SO4 → BaSO4