Презентация на тему: Растворение. Растворимость. Типы растворов

Растворение. Растворимость. Типы растворов Презентация Сергеевой Виктории Юрьевны Учитель химии ГОУ №256

ФИЗИЧЕСКАЯ ТЕОРИЯ РАСТВОРОВ Якоб Вант-ГоффСванте АррениусВильгельм Освальд Растворение--результат диффузии, т.е. физический процесс.Диффузия-проникновение частиц растворённого вещества между молекулами растворителя.

Физико-химическая теория растворов. 1906годД.И.МенделеевГидратная теория растворов. При взаимодействии растворённого вещества с водой образуются гидраты.CuSO4-белые кристаллыCuSO4 . 5H2 O-голубые кристаллыКристаллогидрат сульфата меди (II)Медный купорос.

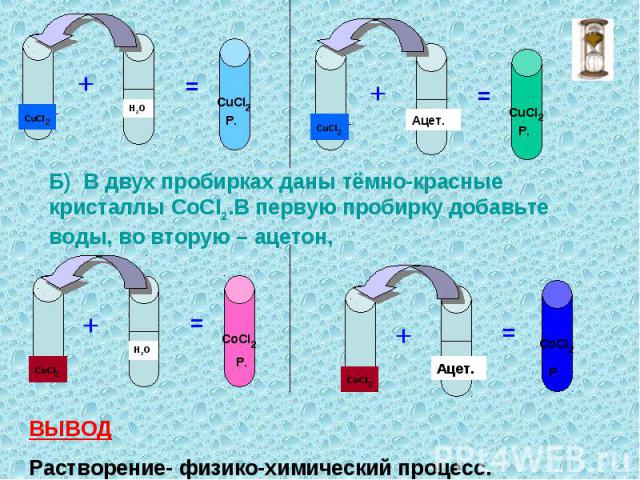
В пробирку поместите белые кристаллы CuSO4, добавьте воды, перемешайте. Определите цвет полученного раствора. а) В двух пробирках даны голубые кристаллы СuCI2. В первую добавьте воды, во вторую- ацетон, перемешайте. Определите цвет полученных растворов.
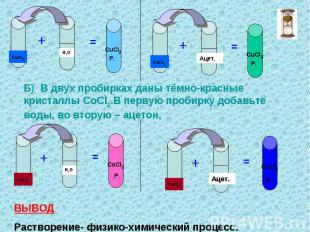
Б) В двух пробирках даны тёмно-красные кристаллы СоСI2.В первую пробирку добавьте воды, во вторую – ацетон, ВЫВОД Растворение- физико-химический процесс.

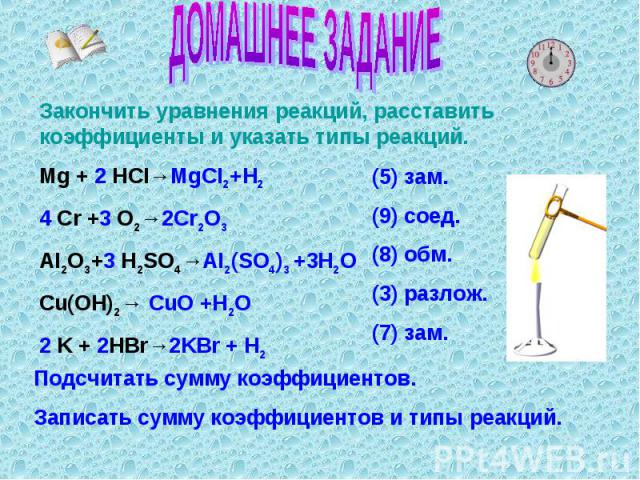
ДОМАШНЕЕ ЗАДАНИЕ Закончить уравнения реакций, расставить коэффициенты и указать типы реакций.Mg + 2 HCI→MgCI2+H24 Cr +3 O2→2Cr2O3AI2O3+3 H2SO4→AI2(SO4)3 +3H2OCu(OH)2→ CuO +H2O2 K + 2HBr→2KBr + H2 (5) зам.(9) соед.(8) обм.(3) разлож.(7) зам. Подсчитать сумму коэффициентов.Записать сумму коэффициентов и типы реакций.

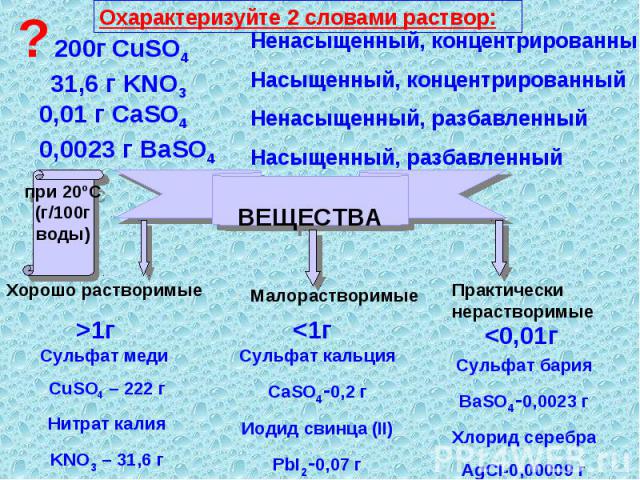
РАСТВОРИМОСТЬ ВЕЩЕСТВ В ВОДЕ при 20ºС (г/100г воды) Хорошо растворимые Сульфат меди CuSO4 – 222 гНитрат калияKNO3 – 31,6 г Сульфат кальцияCaSO4-0,2 гИодид свинца (II)PbI2-0,07 г Сульфат барияBaSO4-0,0023 гХлорид серебраAgCI-0,00009 г

В организме человека в среднем содержится 5 л крови, плотность которой состовляет 1,05 г/мл. Сколько граммов железа и гемоглобина содержится в крови, если массовая доля гемоглобина состовляет 12%, а массовая доля железа в гемоглобине – 5%?
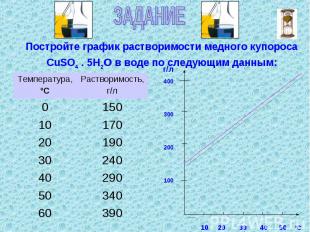
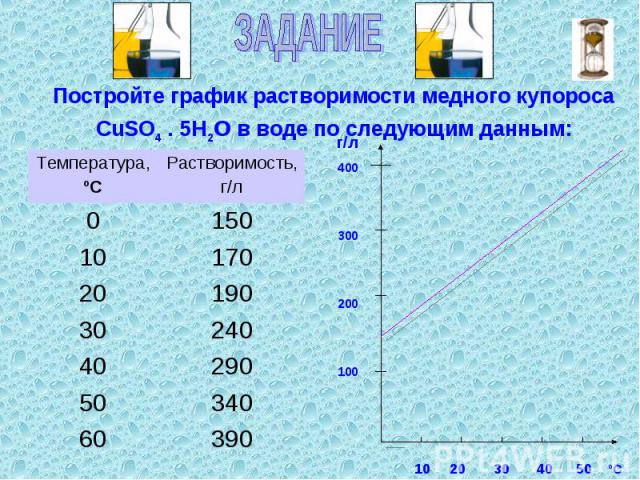
Постройте график растворимости медного купороса CuSO4 . 5H2о в воде по следующим данным:

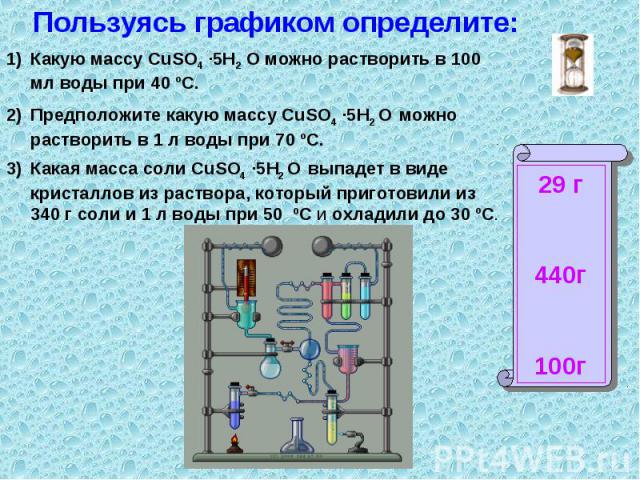
Какую массу CuSO4 ·5H2 O можно растворить в 100 мл воды при 40 ºС.Предположите какую массу CuSO4 ·5H2 O можно растворить в 1 л воды при 70 ºС.Какая масса соли CuSO4 ·5H2 O выпадет в виде кристаллов из раствора, который приготовили из 340 г соли и 1 л воды при 50 ºС и охладили до 30 ºС.

ОТВЕТ: m(гем.) = 630 г m(Fe) = 31,5 г.
ТИПЫ РАСТВОРОВ
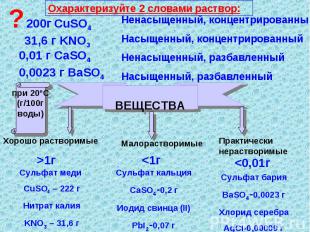
Охарактеризуйте 2 словами раствор: Ненасыщенный, концентрированныйНасыщенный, концентрированныйНенасыщенный, разбавленныйНасыщенный, разбавленный Сульфат меди CuSO4 – 222 гНитрат калияKNO3 – 31,6 г Сульфат кальцияCaSO4-0,2 гИодид свинца (II)PbI2-0,07 г Сульфат барияBaSO4-0,0023 гХлорид серебраAgCI-0,00009 г

Он образуется при растворении вещества в воде.Раствор в котором больше невозможно растворить вещество при данной температуре.Элемент входящий в состав воды.Органический растворитель.Основоположник гидратной теории растворов.Массовая доля растворённого вещества.Основоположник физической теории растворов.Вещество, вызывающее отравление.


ДОМАШНЕЕ ЗАДАНИЕ § 34Упражнения 4, 5, 6.Страница 142

Уже звенит звонок.Спасибо за урок.