Презентация на тему: Основные понятия химии

ОСНОВНЫЕ ПОНЯТИЯ ХИМИИ 1 полугодие 8 класс Л.И.Настина, учитель химии

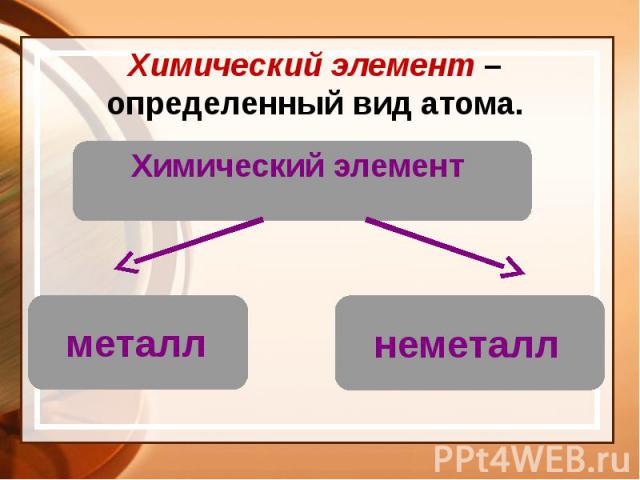
Химия – это наука о веществах, их свойствах и превращениях Химия – это наука о веществах, их свойствах и превращениях Физическое тело вещество Химический элемент - определенный вид атомов


Вещества – это то, из чего состоят тела

План характеристики элемента: 1. Символ и название. 2. Положение в ПСХЭ. 3. Строение атома. 4. Электронная конфигурация. 5. Структурная конфигурация. 6. Формула и характер высшего оксида. 7. Формула гидроксидного соединения.

Ион - Заряженная частица вещества NA+, Cl- , SO4 2-, Al3+

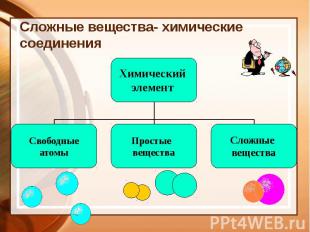
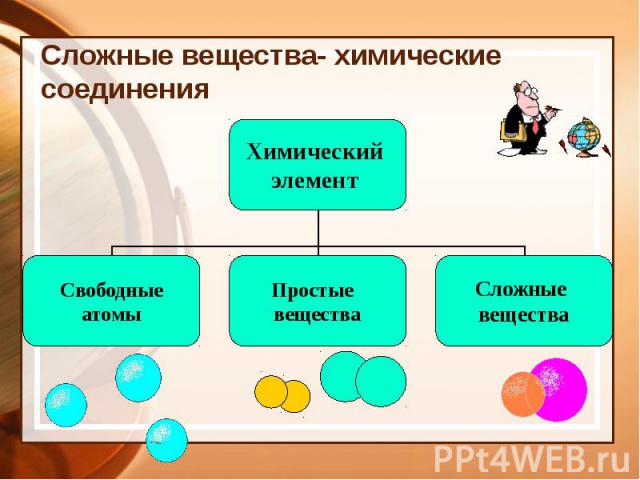
Сложные вещества- химические соединения
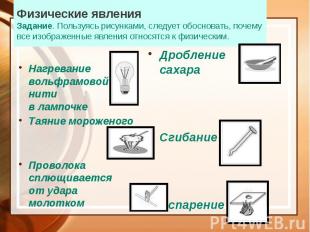
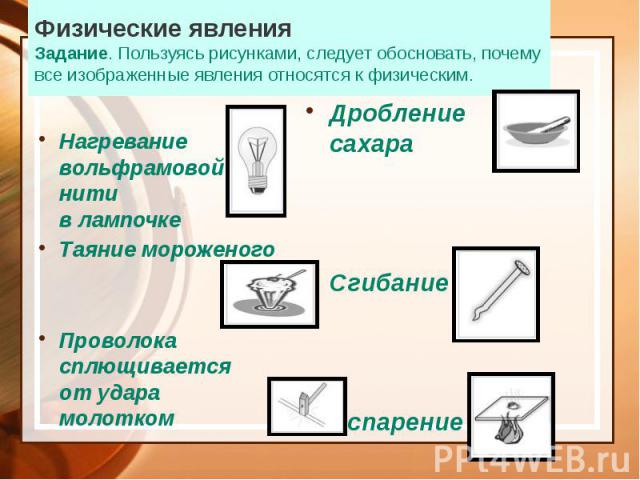
Физические явления Задание. Пользуясь рисунками, следует обосновать, почему все изображенные явления относятся к физическим. Нагревание вольфрамовой нити в лампочке Таяние мороженого Проволока сплющивается от удара молотком
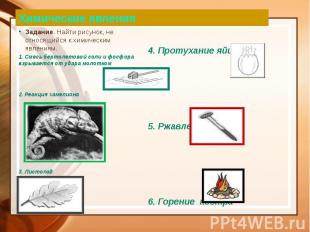
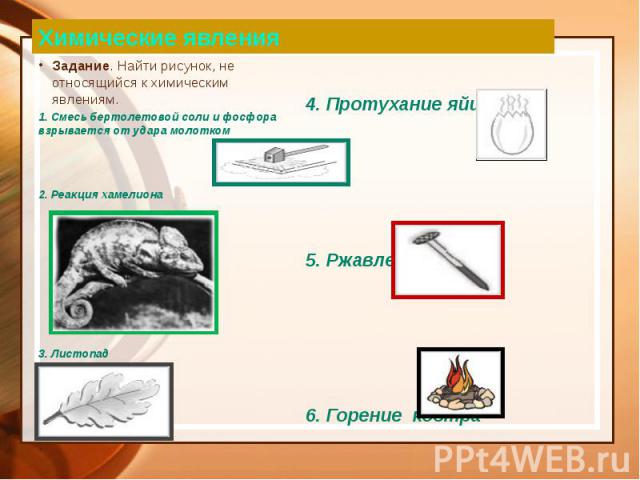
Химические явления Задание. Найти рисунок, не относящийся к химическим явлениям. 1. Смесь бертолетовой соли и фосфора взрывается от удара молотком 2. Реакция хамелиона 3. Листопад

Признаки химической реакции Изменение окраски. Выделение или поглощение теплоты. Появление запаха. Образования осадка. Выделение газа.


Под ВАЛЕНТНОСТЬ (сила) понимают свойства атомов образовывать химические связи с другими атомами, а также число одинарных связей. Под ВАЛЕНТНОСТЬ (сила) понимают свойства атомов образовывать химические связи с другими атомами, а также число одинарных связей. Валентность у элементов бывает: постоянная, переменная. Определять валентность можно также с помощью ПСХЭ.

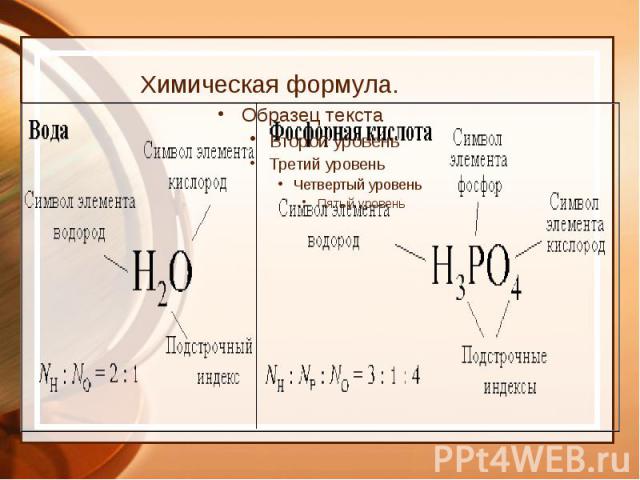
Химические формулы Химическая формула – это условная запись состава вещества посредством химических знаков и индексов.
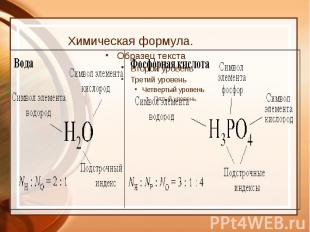
Химическая формула.

Закон постоянства состава вещества или закон Пруста. каждое химически чистое вещество с молекулярным строением независимо от места нахождения и способа получения имеет один и тот же постоянный качественный и количественный состав.

Индекс показывает количество атомов данного элемента в молекуле. Итак, состав веществ выражается химическими формулами с целочисленными индексами, например Н2О, НСl, СН4, HNO3, CuS, Na3PO4, P2O5, Na2SO4
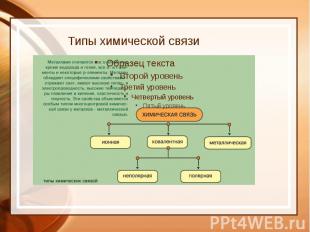
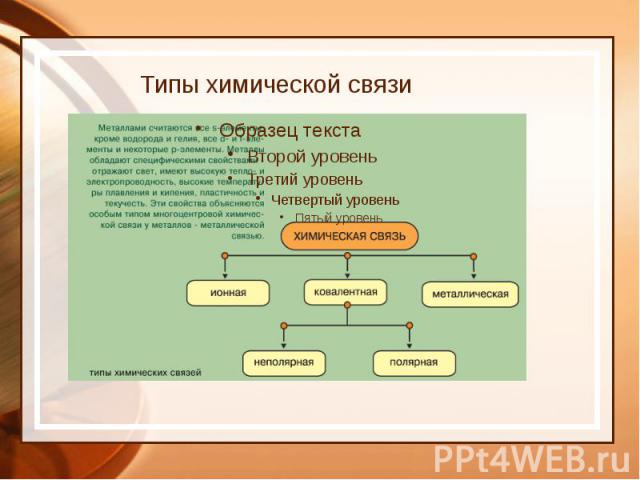
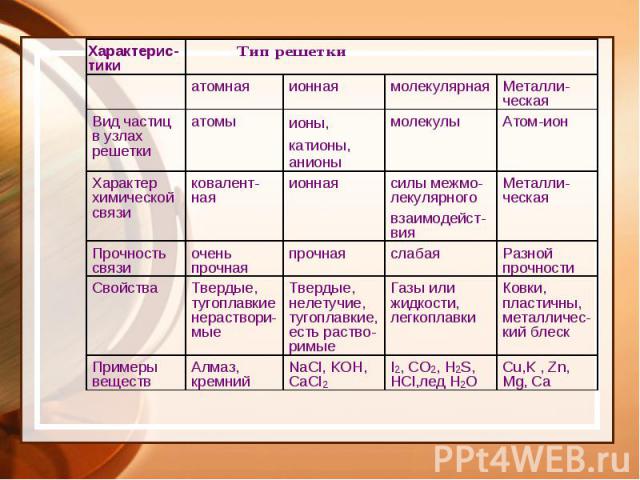
Типы химической связи
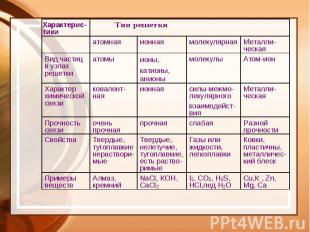

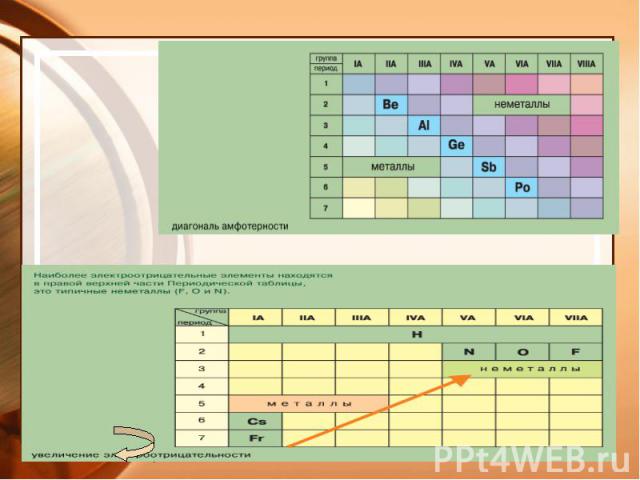
Электроотрицательность - способность атомов оттягивать на себя электроны.
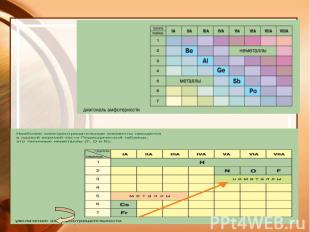




Массовые доли элементов. ФОРМУЛА: Ar (эл.)• n W(эл.) Mr (в-ва) Единицы измерения [доли] или [%], в этом случае умножаем на 100 %.
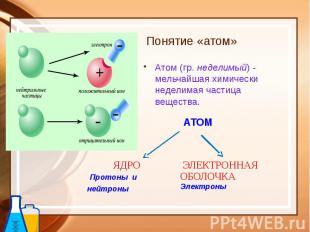
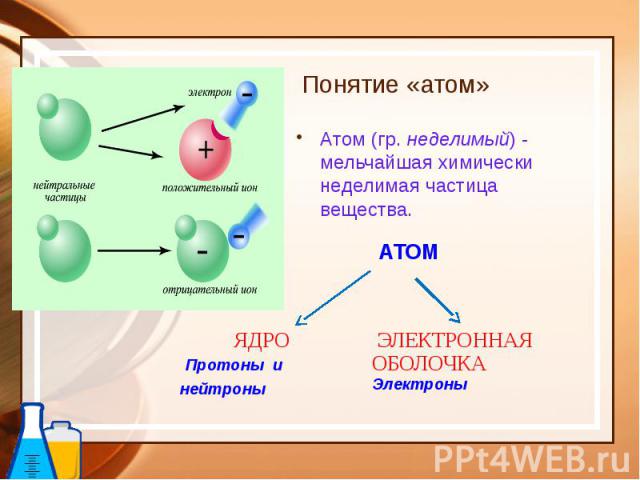
Понятие «атом» Атом (гр. неделимый) - мельчайшая химически неделимая частица вещества.

ОСНОВНЫЕ ПОЛОЖЕНИЯ ПЛАНЕТАРНОЙ МОДЕЛИ: Атом – это микрочастица, которая имеет форму шара. Атом – это сложная система, состоящая из ядра и электронов. Ядра находятся в центре атома и имеют очень маленький размер. Ядро имеет положительный заряд, величина которого определяется числом протонов в нем. Электроны движутся вокруг ядра, имеют ничтожно малую массу и размеры, обладают отрицательным зарядом. Атом электронейтрален, поэтому число протонов и электронов в нем одинаково.

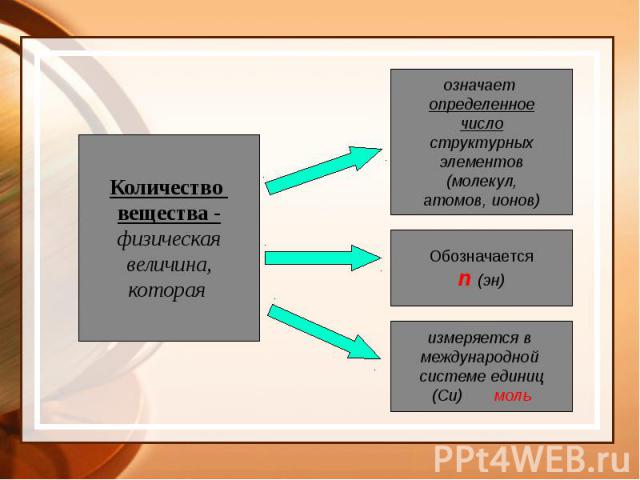
Как измерить вещество?
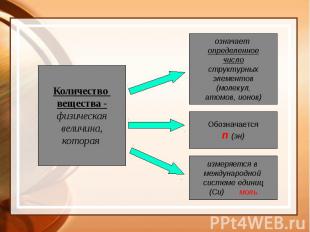
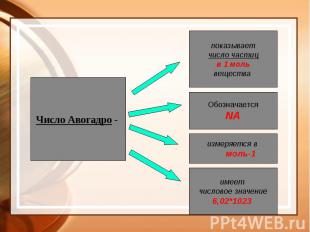
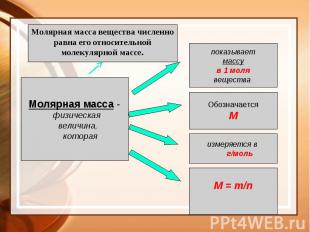

Для расчёта количества

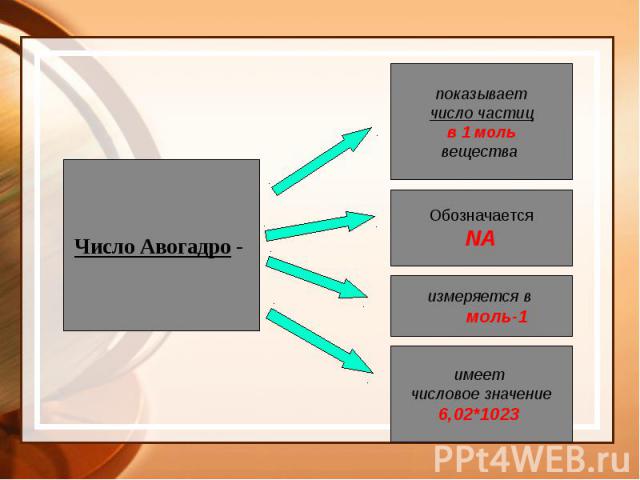
Но если число частиц известно?

Амедео Авогадро высказал предположение в 1811 году, что

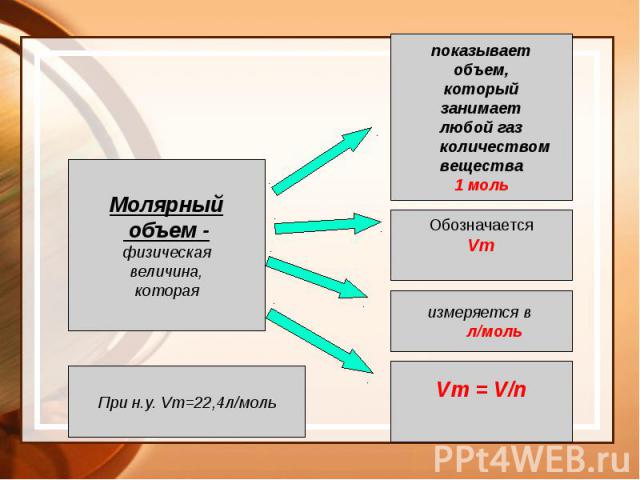
Молярный объем газа Vm Молярный объем газа Vm
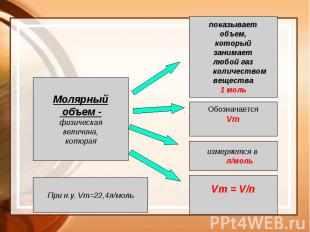

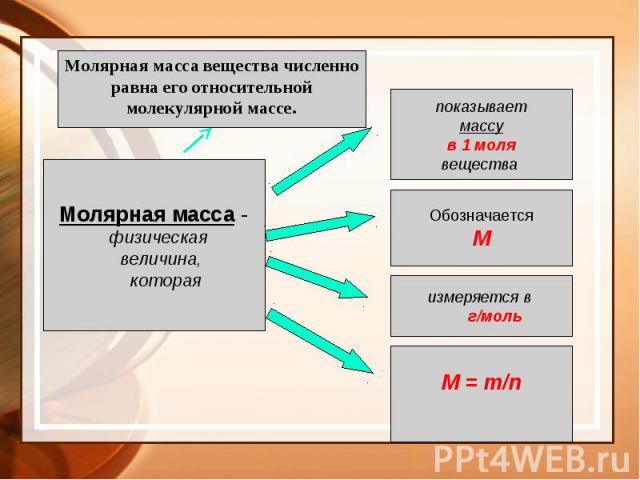
Производные формулы

Отношение массы растворимого вещества к общей массе раствора называют массовой долей растворенного вещества. Отношение массы растворимого вещества к общей массе раствора называют массовой долей растворенного вещества. Массовую долю обозначают греческой буквой W (омега) и выражают в долях единицы или процентах.

Оцените своё состояние после урок

















![Массовые доли элементов. ФОРМУЛА: Ar (эл.)• n W(эл.) Mr (в-ва) Единицы измерения [доли] или [%], в этом случае умножаем на 100 %. Массовые доли элементов. ФОРМУЛА: Ar (эл.)• n W(эл.) Mr (в-ва) Единицы измерения [доли] или [%], в этом случае умножаем на 100 %.](https://fs1.ppt4web.ru/images/95289/123012/640/img25.jpg)