Презентация на тему: Основания, их классификация и свойства в свете теории электролитической диссоциации

Урок-презентация Химия 8 класс

Основания, их классификация и свойства в свете теории электролитической диссоциации

ЦЕЛИ УРОКА: 1) сформировать понятие об основаниях как электролитах;2) рассмотреть классификацию оснований по различным признакам;3) познакомить практически с химическими свойствами оснований в свете теории электролитической диссоциации; 4) развивать умения и навыки работы с химическими реактивами и химическим оборудованием;5) учить сравнивать, анализировать, делать выводы;6) совершенствовать умения и навыки в написании формул веществ и уравнений химических реакций.

ЗАДАЧИ УРОКА:1) учиться проводить химические реакции и записывать уравнения химических реакций в молекулярной, полной и сокращенной ионной формах;2) различать свойства растворимых и нерастворимых оснований.

Основания - это сложные вещества, в которых атом металла связан с одной или несколькими гидроксогруппами (ОН).Названия оснований состоят из двух слов:гидроксид + название металла в родительном падеже.Если металл образует соединения с разными степенями окисления, то степень окисления указывается после названия металла в скобках римской цифрой:Fe(OH)2 ___ гидроксид железа (II).
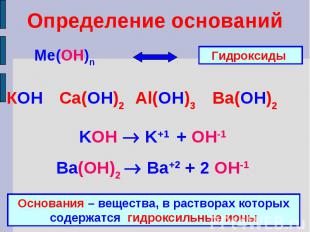
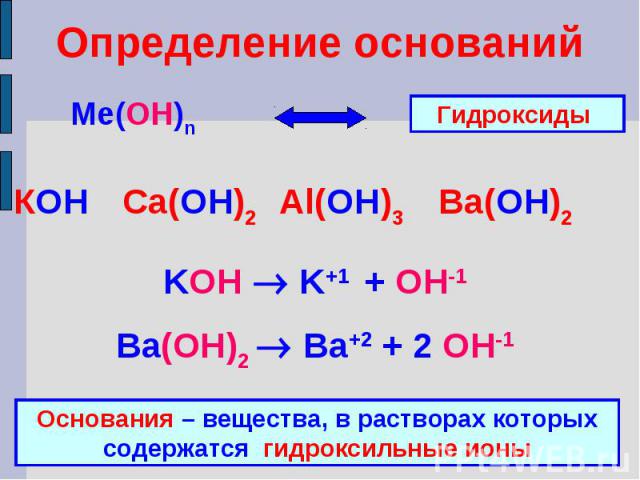
Определение основанийКОН Ca(ОН)2 Al(ОН)3 Ba(ОН)2KOH K+1 + OH-1Ba(ОН)2 Ba+2 + 2 OH-1Основания – вещества, в растворах которых содержатся гидроксильные ионы
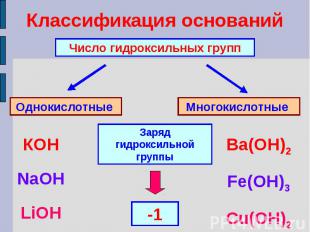
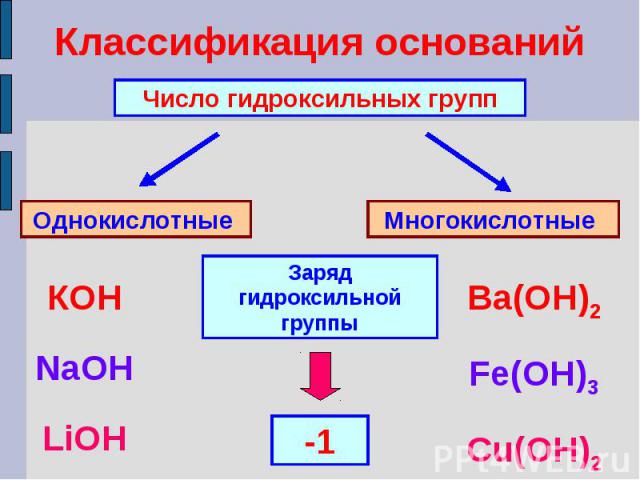
Классификация основанийЧисло гидроксильных группОднокислотные Многокислотные Заряд гидроксильной группыКОНNaOHLiOHBa(ОН)2Fe(OH)3Cu(OH)2
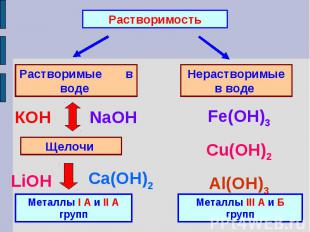
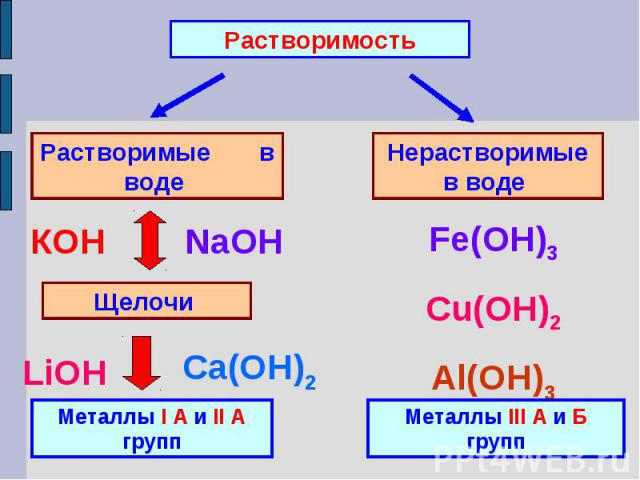
РастворимостьРастворимые в воде Нерастворимые в воде Металлы I А и II А группМеталлы III А и Б групп


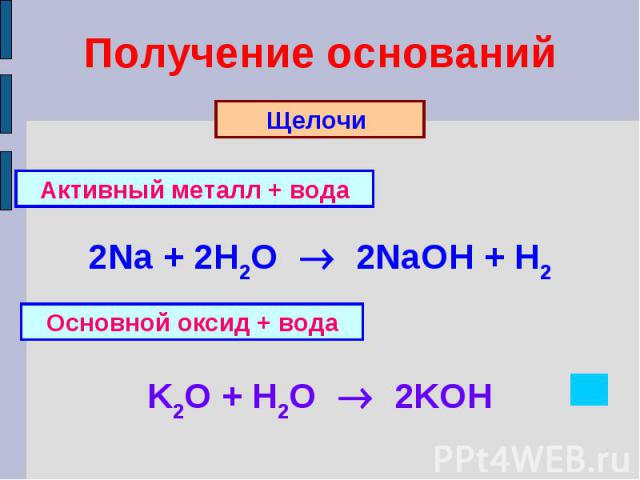
Получение основанийАктивный металл + вода2Na + 2H2O 2NaOH + H2Основной оксид + водаK2O + H2O 2KOH
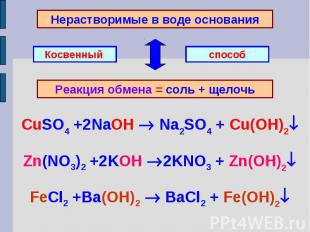
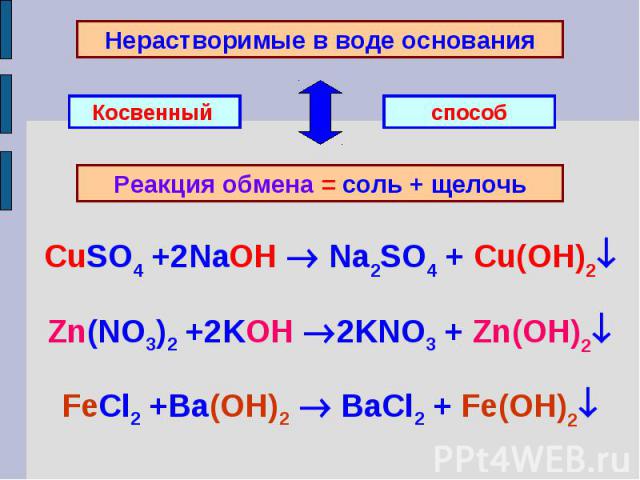
Нерастворимые в воде основанияРеакция обмена = соль + щелочьCuSO4 +2NaOH Na2SO4 + Cu(OH)2Zn(NO3)2 +2KOH 2KNO3 + Zn(OH)2FeCl2 +Ba(OH)2 BaCl2 + Fe(OH)2
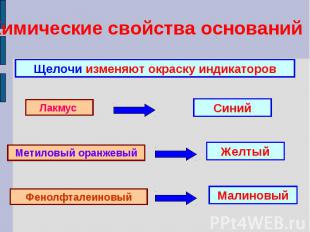
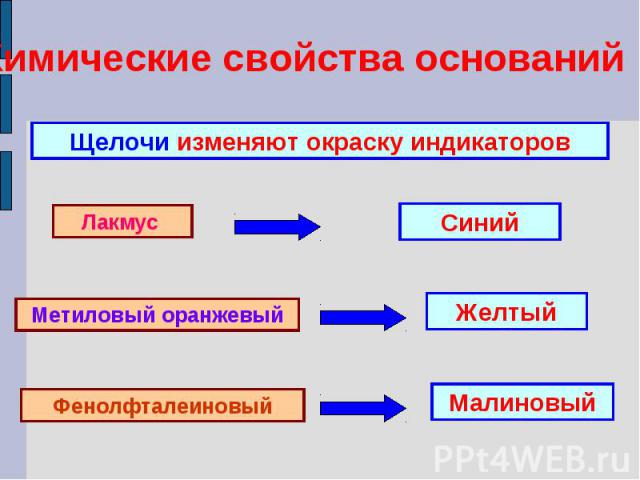
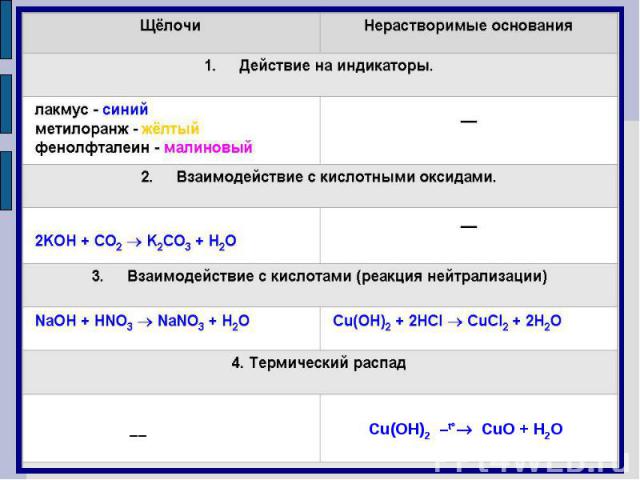
Химические свойства основанийЩелочи изменяют окраску индикаторовЛакмус СинийМетиловый оранжевыйЖелтыйФенолфталеиновыйМалиновый
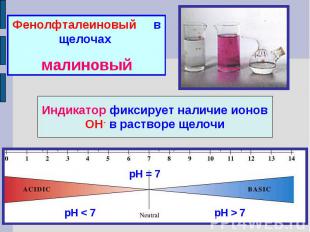
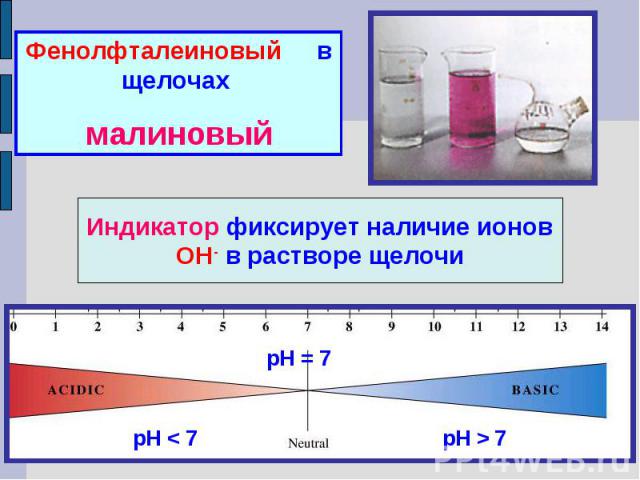
Фенолфталеиновый в щелочах малиновыйИндикатор фиксирует наличие ионов ОН- в растворе щелочи






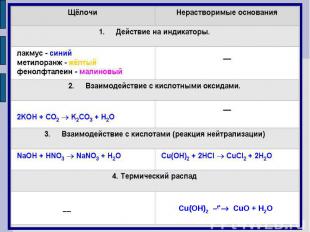

Рефлексия: Вариант 1 Вариант2 1. Данны вещества: CaO, AI(OH)3, HCI, KOH, Na2SO4, MgO, BA(OH)2, H2SO4, N2O5, NaOH, HNO3, Ca(OH)2, MgCO3, Fe(OH)3.Выбрать щелочи. Выбрать нерастворимые основания.2. Выбрать оксиды, с которыми реагирует NaOH KOHa) SO2; CO2 а) Na2O; CaOб) AI2O3; MgO б) CO2; N2O5в) N2O5; P2O5 в) FeO; K2Oг) CaO; Fe2O3 г) P2O5; SO33.Выбрать вещество с которыми реагирует AI(OH)3 Fe(OH)3 а) CO2 а) H3PO4б)NaOH б)Na2Oв)H2SO4 в)KOH4. В растворах щелочей:Фенолфталеин Лакмуса)бесцветный; б)синий; в) малиновый; г) красный5. Соотнесите:Формула оксида: Формула гидроксида:1. Fe2o3; 2. CO2; 3.Ca O; 4. P2O5; 1.KOH; 2. H2SO4;3. Fe (OH)2Формула гидроксида: Формула гидроксида:А.H2CO3 ;Б.Fe(OH)3;В.Fe(OH)2;Г.Ca(OH)2; А.FeO;Б.SO3; В.K2O; Г.Fe2O3 Д. H3PO4 Д.Al2O3

ОТВЕТЫ: 1 вариант: 2 вариант:1.К ОН,Ва (ОН)2, NaOH, Ca(OH)2 1.Al(ОН)3, Fe(OH)32.a,в 2.б,г3.в 3. а4.в 4. б5. Б А Г Д 5. В Б А Д