Презентация на тему: Характеристика алюминия

* Выполнил: Ученик 9”Б” класса Власов Данил 5klass.net
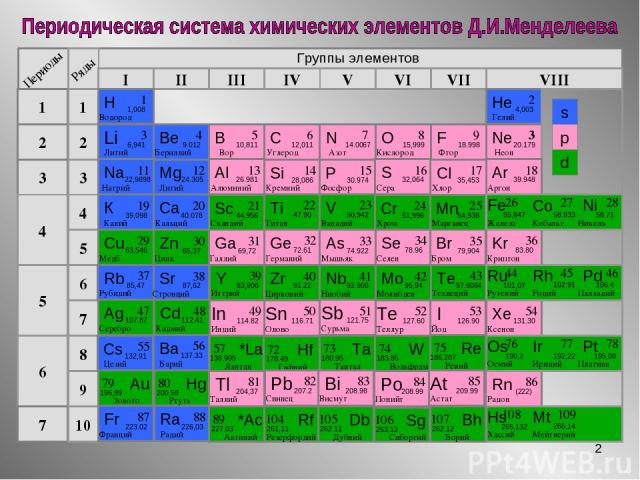
* Группы элементов I II III IV VII VI V VIII 3 2 1 4 5 6 7 1 2 3 4 5 6 7 8 9 10 s d p
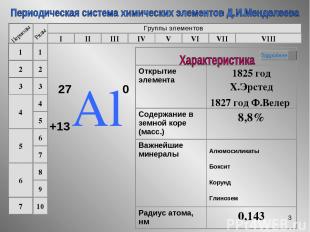
* Группы элементов I II III IV VII VI V VIII 3 2 1 4 5 6 7 1 2 3 4 5 6 7 8 9 10 Подробнее Открытие элемента 1825 год Х.Эрстед 1827 год Ф.Велер Содержание в земной коре (масс.) 8,8% Важнейшие минералы Алюмосиликаты Боксит Корунд Глинозем Радиус атома, нм 0,143

* 2. Электронное строение 5. Свойства атома 3. Строение простого вещества 4. Физические свойства 6. Химические свойства 7. Нахождение в природе 8. Получение 9. Применение 1. Из истории открытия

* 1. Из истории открытия главная Далее Впервые Al был получен датским физиком Эрстедом Х. в 1825 г. Название элемента происходит от лат. алюмен, так в древности называли квасцы, которые использовали для крашения тканей (KAl(SO4)2 . 12H2O). Позже в 1827 г. немецкий химик Фридрих Велер получил алюминий следующим способом:

* 1. Из истории открытия Главная Далее В период открытия алюминия - металл был дороже золота. Англичане хотели почтить богатым подарком великого русского химика Д.И Менделеева, подарили ему химические весы, в которых одна чашка была изготовлена из золота, другая - из алюминия. Чашка из алюминия стала дороже золотой. Полученное «серебро из глины» заинтересовало не только учёных, но и промышленников и даже императора Франции. Далее
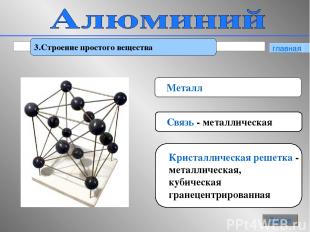
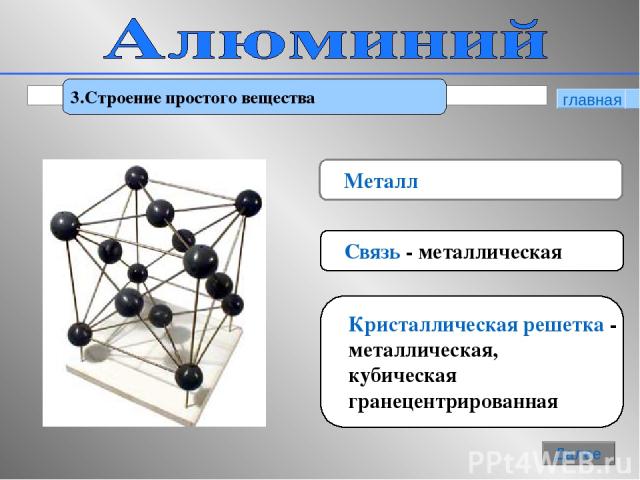
* 3.Строение простого вещества Металл Связь - металлическая Кристаллическая решетка - металлическая, кубическая гранецентрированная главная Далее
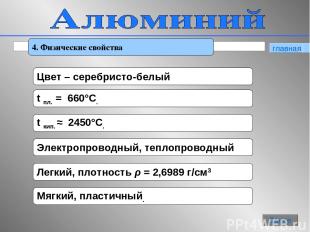
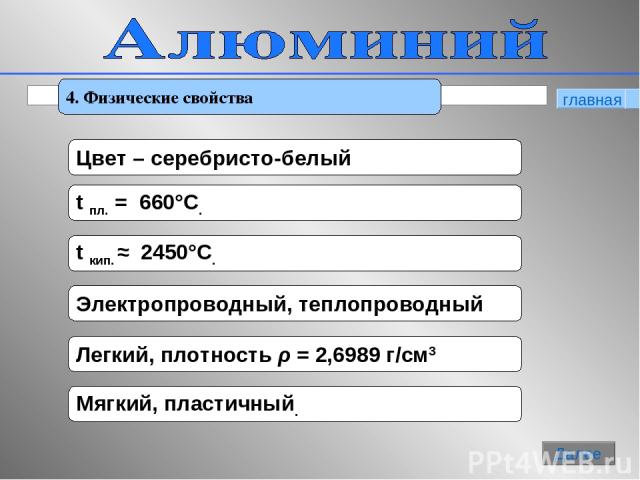
* 4. Физические свойства главная Далее

* 5. Свойства атома 2.1 Степень окисления главная Далее
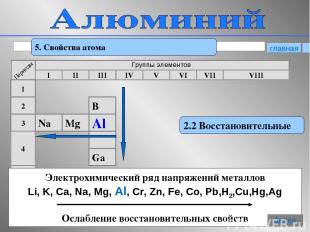
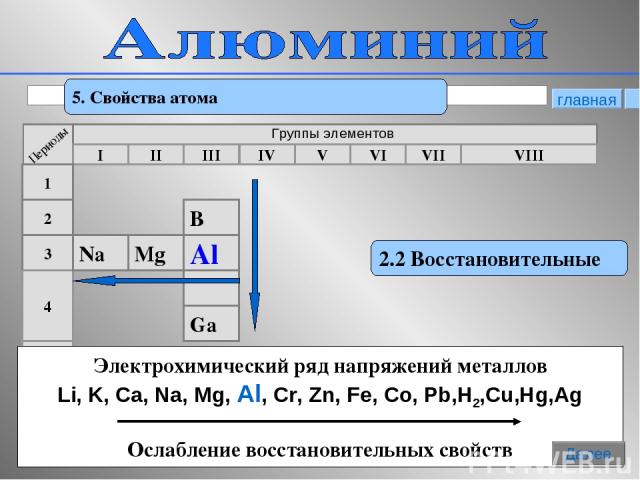
* 5. Свойства атома 2.2 Восстановительные Электрохимический ряд напряжений металлов Li, K, Ca, Na, Mg, Al, Cr, Zn, Fe, Co, Pb,H2,Cu,Hg,Ag Ослабление восстановительных свойств главная Далее

* 6. Химические свойства 4Аl + 3O2 = 2Al2O3 t 2Al + 3S = Al2S3 C н е м е т а л л а м и (c кислородом, с серой) 2Аl + 3Cl2 = 2AlCl3 4Al + 3C = Al4C3 C неметаллами (c галогенами, с углеродом) (Снять оксидную пленку) 2Al + 6H2O = 2Al(OH)2 + H2↑ C в о д о й 2Al + 6HCl = 2AlCl3 + H2↑ 2Al + 3H2SO4 = Al2(SO4)3 + H2↑ C к и с л о т а м и 2Al + 6NaOH + 6H2O = 2Na3[Al(OH)6] + 3H2↑ 2Al + 2NaOH + 2H2O =2NaAlO2 +3H2↑ Cо щ е л о ч а м и 8Al + 3Fe3O4 = 4Al2O3 + 9Fe 2Al + WO3 = Al2O3 + W C о к с и д а м и м е т а л л о в главная Далее
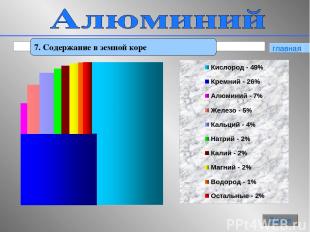
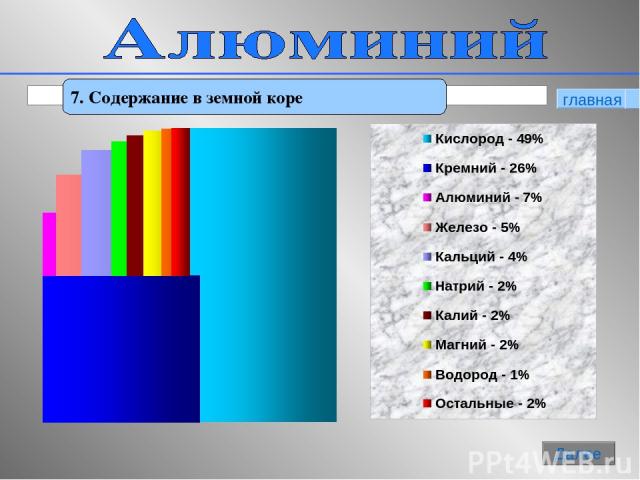
* 7. Содержание в земной коре главная Далее

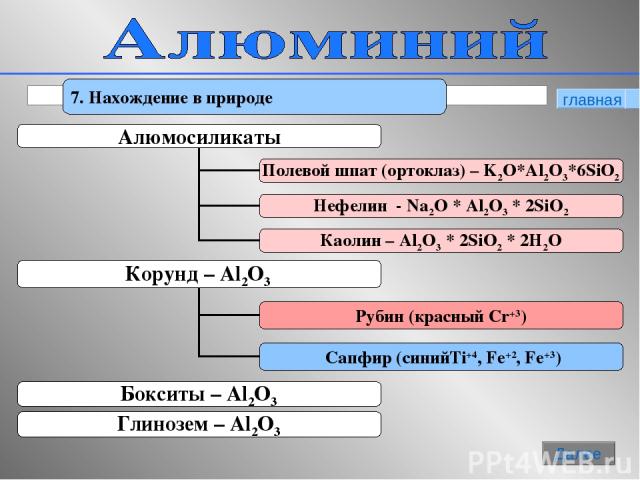
* 7. Нахождение в природе главная Далее

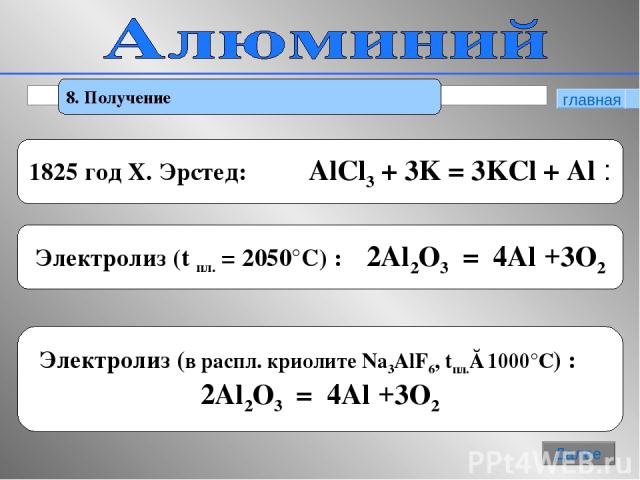
* 8. Получение главная Далее

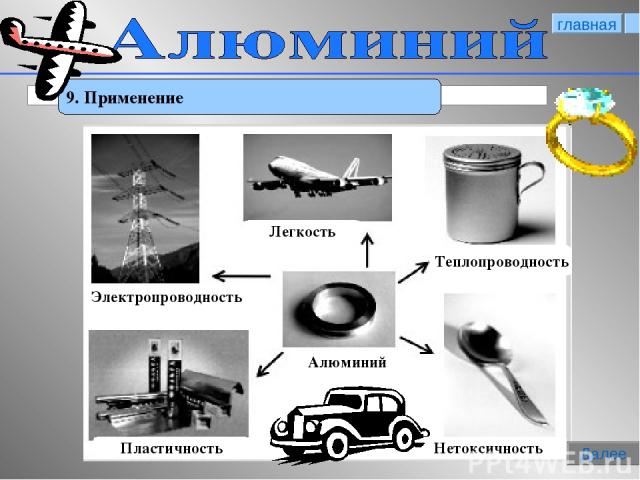
* 9. Применение главная Далее