Презентация на тему: Цветные реакции белков.Качественные реакции на остатки аминокислот.


Биуретовая Биуретовая Уравнение реакции Проведение опыта Нингидриновая Ксантопротеиновая Уравнение реакции Проведение опыта Миллона Гопкинса-Коле Диазореакция Паули

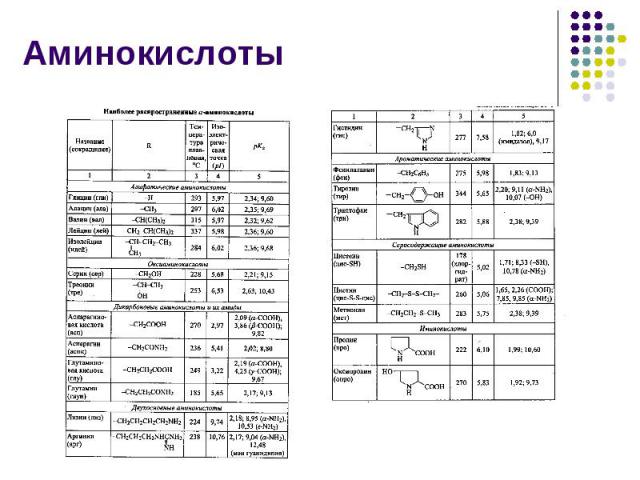
Для аминокислот, постоянно встречающихся в составе белков, разработано множество цветных (в том числе именных) реакций. Многие из них высокоспецифичны, что позволяет определять ничтожные количества той или иной аминокислоты. Для аминокислот, постоянно встречающихся в составе белков, разработано множество цветных (в том числе именных) реакций. Многие из них высокоспецифичны, что позволяет определять ничтожные количества той или иной аминокислоты. Надо помнить, что все качественные реакции – это реакции не собственно на белки, а на определенные аминокислоты, входящие в их состав.
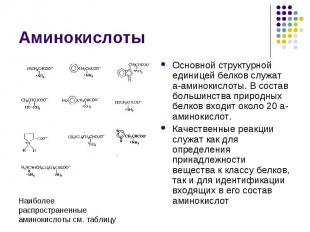
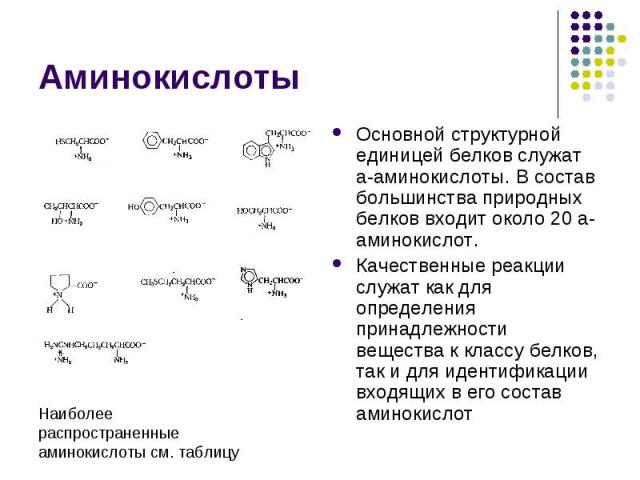
Основной структурной единицей белков служат a-аминокислоты. В состав большинства природных белков входит около 20 a-аминокислот. Основной структурной единицей белков служат a-аминокислоты. В состав большинства природных белков входит около 20 a-аминокислот. Качественные реакции служат как для определения принадлежности вещества к классу белков, так и для идентификации входящих в его состав аминокислот

Определяет наличие пептидной связи в растворе исследуемого соединения. Определяет наличие пептидной связи в растворе исследуемого соединения.

Реакция обусловлена образованием биуретового комплекса в результате соединения меди с пептидной группировкой белка. Реакция обусловлена образованием биуретового комплекса в результате соединения меди с пептидной группировкой белка. В пептидах и белках пептидная связь обычно находится в амидной форме (или кетоформе), но в щелочной среде она переходит в иминольную (енольную):

Биуретовая реакция протекает так: Биуретовая реакция протекает так:
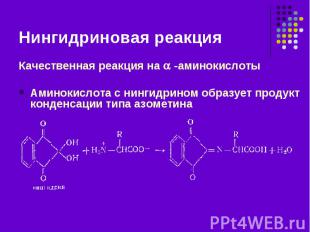
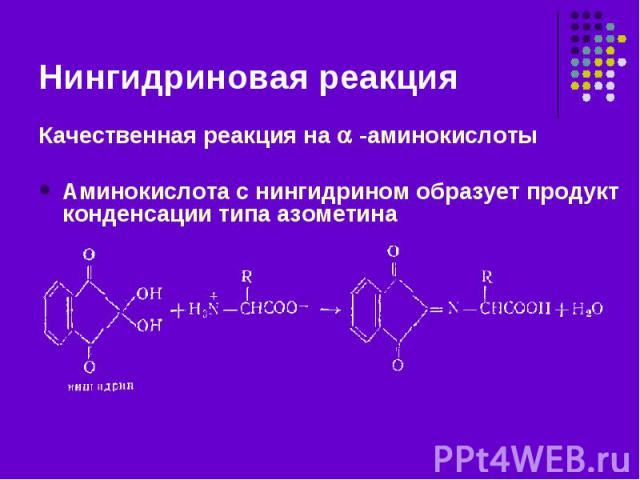
Качественная реакция на -аминокислоты Качественная реакция на -аминокислоты Аминокислота с нингидрином образует продукт конденсации типа азометина
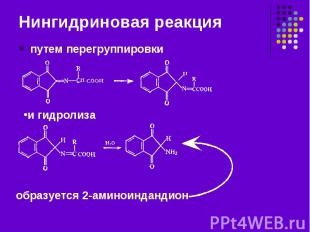
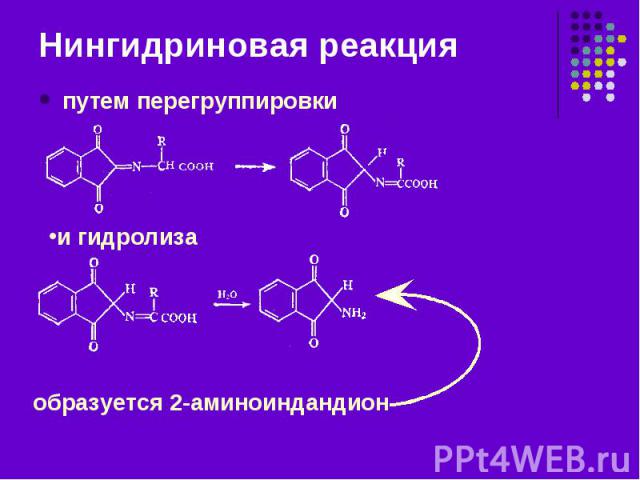
путем перегруппировки путем перегруппировки
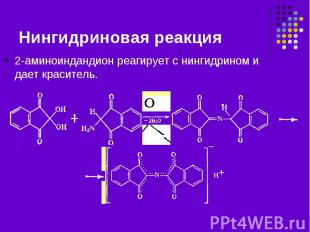
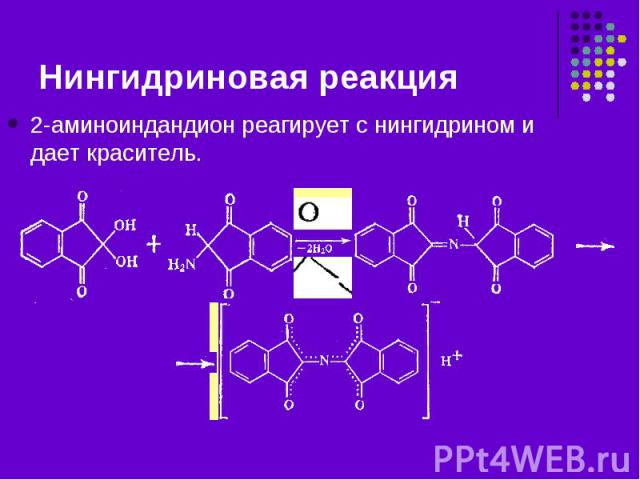
2-аминоиндандион реагирует с нингидрином и дает краситель. 2-аминоиндандион реагирует с нингидрином и дает краситель.

Определяет присутствие в белке ароматических и гетероциклических - аминокислот : Определяет присутствие в белке ароматических и гетероциклических - аминокислот : триптофана, фенилаланина, тирозина, гистидина.
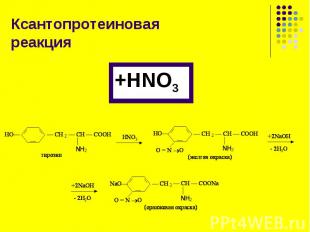

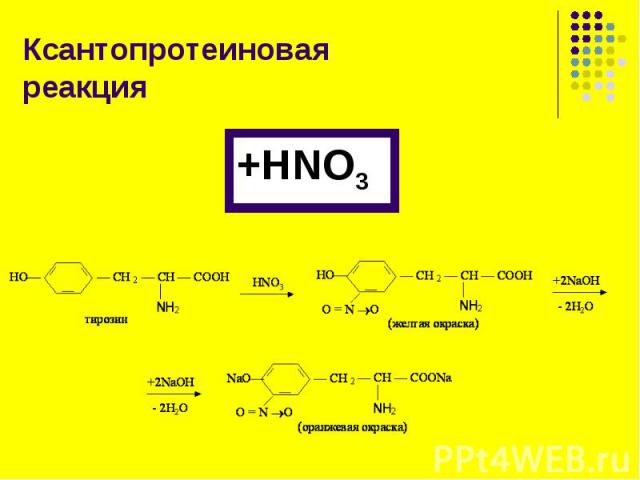
Это реакция на аминокислоту тирозин Это реакция на аминокислоту тирозин

Реактив Миллона (раствор HgNO3 и Hg(NO2)2 в разбавленной HNO3, содержащей примесь HNO2) взаимодействует с тирозином с образованием ртутной соли нитропроизводного тирозина, окрашенной в розовато-красный цвет: Реактив Миллона (раствор HgNO3 и Hg(NO2)2 в разбавленной HNO3, содержащей примесь HNO2) взаимодействует с тирозином с образованием ртутной соли нитропроизводного тирозина, окрашенной в розовато-красный цвет:

К 2 мл концентрированного раствора тирозина прибавляют ~1 мл реактива Миллона К 2 мл концентрированного раствора тирозина прибавляют ~1 мл реактива Миллона встряхивают осторожно нагревают пробирки на пламени спиртовки. Образуется красное окрашивание.

Эта реакция определяет аминокислоту триптофан. Эта реакция определяет аминокислоту триптофан.

Из глиоксиловой кислоты под действием концентрированной серной кислоты сначала получается формальдегид: Из глиоксиловой кислоты под действием концентрированной серной кислоты сначала получается формальдегид:
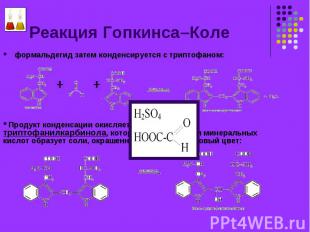
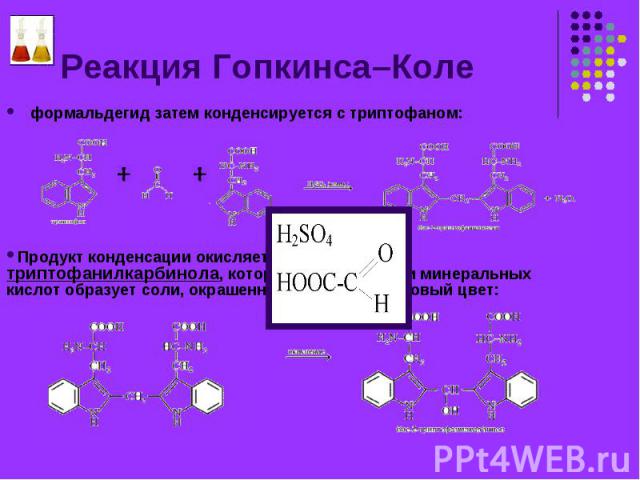
формальдегид затем конденсируется с триптофаном: формальдегид затем конденсируется с триптофаном:

Охладить до 0 °С насыщенного раствора щавелевой кислоты Охладить до 0 °С насыщенного раствора щавелевой кислоты К 2 г порошка магния (слегка увлажненного) добавить щавелевую кислоту Полученный осадок оксалата магния отфильтровать и декантировать небольшим количеством воды. Фильтрат подкислить уксусной кислотой и довести до объема 200 мл (полученный раствор хранить в холодильнике!). Это и есть глиоксиловая кислота. 1 мл 0,005%-го раствора триптофана смешать с равным объемом глиоксиловой кислоты и к смеси прибавляют 10 капель раствора сульфата меди(II). Небольшими порциями добавляют 2–3 мл концентрированной серной кислоты, охлаждая пробирку после приливания очередной порции кислоты током холодной воды (или в ванночке со льдом). Полученную смесь оставляют на 10 мин при комнатной температуре, после чего ставят на 5 мин в кипящую водяную баню. Наблюдается образование сине-фиолетового окрашивания

Эта реакция аминокислоту гистидин. Эта реакция аминокислоту гистидин.

при взаимодействии кислого раствора сульфаниловой кислоты с нитритом натрия образуется диазобензолсульфоновая кислота: при взаимодействии кислого раствора сульфаниловой кислоты с нитритом натрия образуется диазобензолсульфоновая кислота:
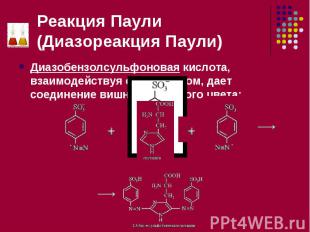
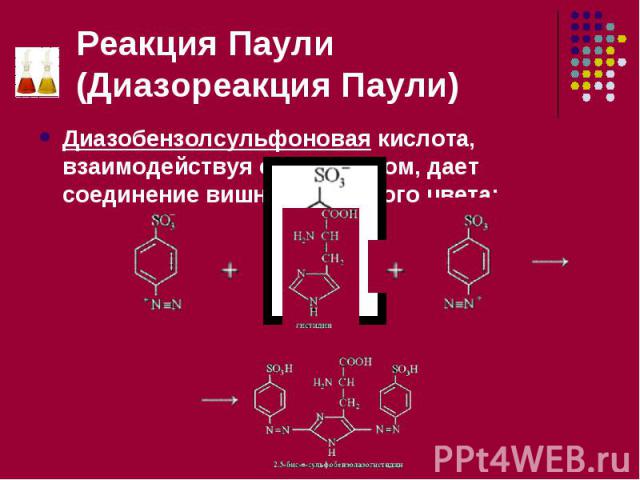
Диазобензолсульфоновая кислота, взаимодействуя с гистидином, дает соединение вишнево-красного цвета: Диазобензолсульфоновая кислота, взаимодействуя с гистидином, дает соединение вишнево-красного цвета:

В пробирку наливают 1 мл 1%-го раствора сульфаниловой кислоты в 5%-м растворе соляной кислоты. В пробирку наливают 1 мл 1%-го раствора сульфаниловой кислоты в 5%-м растворе соляной кислоты. Прибавляют 2 мл 0,5%-го раствора нитрита натрия Сильно встряхивают Немедленно приливают 2 мл 0,01%-го раствора гистидина После перемешивания содержимого пробирки сразу приливают 6 мл 10%-го раствора соды. Появляется интенсивная вишнево-красная окраска.