Презентация на тему: АЗОТ И ФОСФОР

Урок по химии в 10 классе: «Азот и фосфор – p-элементы VA-группы» подготовил учитель химии и биологии ГУО СШ №163 г.Минска Костюкевич Юрий Михайлович

В VA-группе периодической системе расположены неметаллы азот N и фосфор P, полуметалл мышьяк As, а также сурьма Sb и висмут Bi, которые относят к неметаллам.

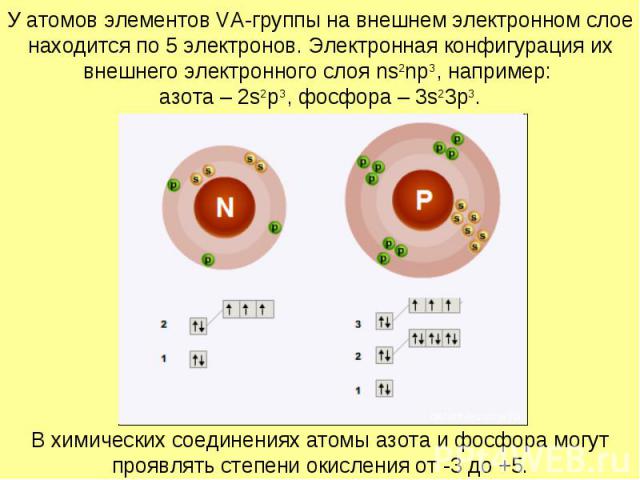
У атомов элементов VA-группы на внешнем электронном слое находится по 5 электронов. Электронная конфигурация их внешнего электронного слоя ns2np3, например: азота – 2s2p3, фосфора – 3s23p3.

Азот в природе Азот обозначается символом N (лат. Nitrogenium, т.е. «рождающий селитру). Простое вещество азот (N2) — достаточно инертный при нормальных условиях газ без цвета, вкуса и запаха. Азот, в форме двухатомных молекул N2 составляет большую часть атмосферы, где его содержание составляет 78,084% по объёму (то есть около 3,87·1015 т).

Азот в космосе Вне пределов Земли азот обнаружен в газовых туманностях, солнечной атмосфере, на Уране, Нептуне, межзвёздном пространстве и др. Азот — 4й по распространённости элемент Солнечной системы (после водорода, гелия и кислорода).

Фосфор в природе Фосфор в природе встречается в основном в виде фосфатов. Так, фосфат кальция Са3(PO4)2 является основным компонентом минерала апатита. Фосфор содержится во всех частях зелёных растений, ещё больше его в плодах и семенах. Содержится в животных тканях, входит в состав белков и других важнейших органических соединений (АТФ, ДНК), является элементом жизни.
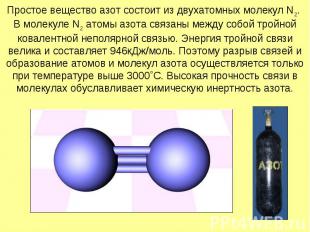
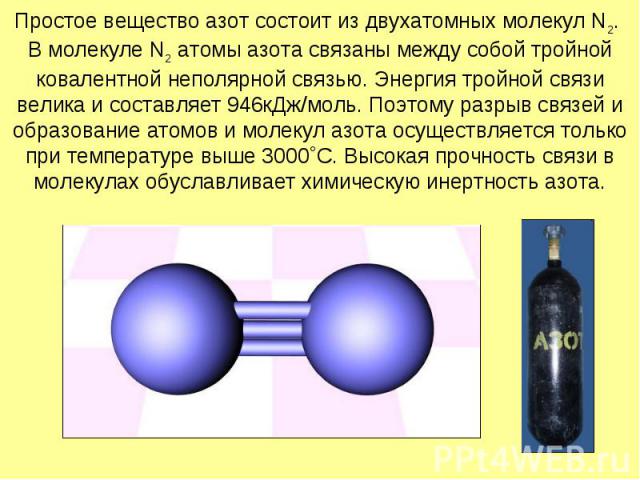
Простое вещество азот состоит из двухатомных молекул N2. В молекуле N2 атомы азота связаны между собой тройной ковалентной неполярной связью. Энергия тройной связи велика и составляет 946кДж/моль. Поэтому разрыв связей и образование атомов и молекул азота осуществляется только при температуре выше 3000˚С. Высокая прочность связи в молекулах обуславливает химическую инертность азота.

В свободном состоянии фосфор образует несколько аллотропных модификаций, которые называются белым, красным и черным фосфором. Фосфор

В простейшей молекуле Р4 каждый из четырех атомов фосфора связан ковалентной связью с тремя остальными. Из таких молекул, имеющих форму тетраэдра, состоит белый фосфор. Отливаемый в инертной атмосфере в виде палочек (слитков), он сохраняется в отсутствие воздуха под слоем очищенной воды или в специальных инертных средах.
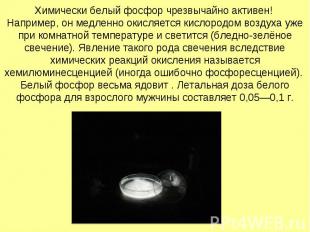
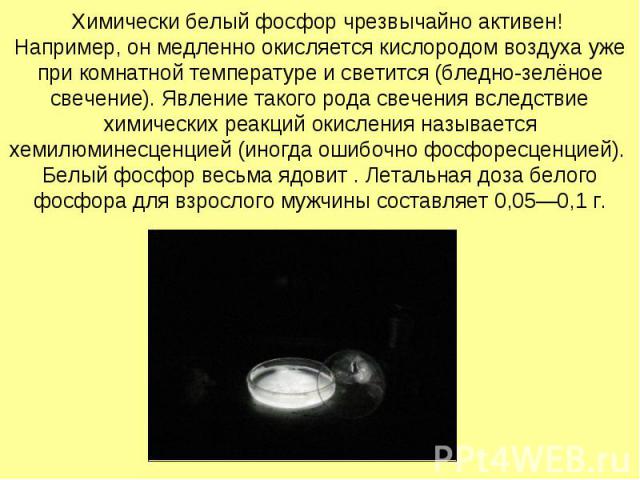
Химически белый фосфор чрезвычайно активен! Например, он медленно окисляется кислородом воздуха уже при комнатной температуре и светится (бледно-зелёное свечение). Явление такого рода свечения вследствие химических реакций окисления называется хемилюминесценцией (иногда ошибочно фосфоресценцией). Белый фосфор весьма ядовит . Летальная доза белого фосфора для взрослого мужчины составляет 0,05—0,1 г.
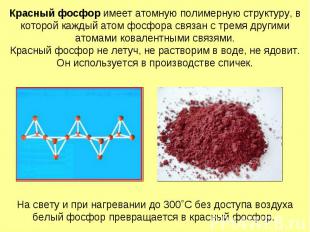
Красный фосфор имеет атомную полимерную структуру, в которой каждый атом фосфора связан с тремя другими атомами ковалентными связями. Красный фосфор не летуч, не растворим в воде, не ядовит. Он используется в производстве спичек.

При нагревании под давлением примерно в 1200 раз большим, чем атмосферное давление, белый фосфор переходит в черный фосфор, который имеет атомную слоистую кристаллическую решетку. Черный фосфор по своим физическим свойствам похож на металл: он проводит электрический ток и блестит. Внешне весьма похож на графит. Чёрный фосфор — это химически наименее активная форма фосфора.

В 1830 году французский химик Шарль Сориа изобрёл фосфорные спички, состоявшие из смеси бертолетовой соли, белого фосфора и клея. Эти спички были весьма огнеопасны, поскольку загорались даже от взаимного трения в коробке и при трении о любую твёрдую поверхность, например, подошву сапога. Из-за белого фосфора они были ядовиты. В 1855 году шведский химик Йохан Лундстрем нанёс красный фосфор на поверхность наждачной бумаги и заменил им же белый фосфор в составе головки спички. Такие спички уже не приносили вреда здоровью, легко зажигались о заранее приготовленную поверхность и практически не самовоспламенялись. Йохан Лундстрем патентует первую «шведскую спичку», дошедшую практически до наших дней. В 1855 году спички Лундстрема были удостоены медали на Всемирной выставке в Париже. Позднее фосфор был полностью выведен из состава головок спичек и оставался только в составе намазки (тёрки). С развитием производства «шведских» спичек, производство спичек с использованием белого фосфора было запрещено почти во всех странах.

Простейшее вещество азот N2 химически малоактивно и, как правило, вступает в химические реакции только при высоких температурах. Окислительные свойства азота проявляются в реакции с водородом и активными металлами. Так, водород с азотом соединяется в присутствии катализатора при высокой температуре и большом давлении, образуя аммиак: Из металлов при обычных условиях азот реагирует только с литием, образуя нитрид лития:

Окислительные свойства фосфора проявляются при его взаимодействии с наиболее активными металлами: Восстановительные свойства азота и фосфора проявляются при их взаимодействии с кислородом. Так, азот реагирует с кислородом при температуре около 3000˚С, образуя оксид азота (II):

Фосфор также окисляется кислородом, проявляя при этом восстановительные свойства. Но у разных модификаций фосфора химическая активность различна. Например, белый фосфор легко окисляется на воздухе при комнатной температуре с образованием оксида фосфора(III): Окисление белого фосфора сопровождается свечением. Белый и красный фосфор загораются при поджигании и горят ослепительно ярким пламенем с образованием белого дыма оксида фосфора(IV):

Горение белого фосфора

Наиболее активен химически, токсичен и горюч белый фосфор. Потому он очень часто применяется в зажигательных бомбах. К сожалению, фосфорные боеприпасы применяются и в XXI веке! - во время осады Сараево фосфорные снаряды применялись артиллерией боснийских сербов. В 1992 году такими снарядами было сожжено здание Института востоковедения, в результате чего погибло множество исторических документов. - в 2003-2004 годах применялись британскими спецслужбами в окрестностях Басры в Ираке. - в 2004 году применялись США против партизанского подполья в Ираке в сражении за Фаллуджу. летом 2006 года, в ходе Второй Ливанской войны артиллерийские снаряды с белым фосфором применяла израильская армия. в 2009 году в ходе операции «Литой свинец» в секторе Газа израильская армия применяла боеприпасы, содержащие белый фосфор, допускаемые международным законодательством. - с 2009 палестинские террористы заряжали свои ракеты белым фосфором.
Появление блуждающих огней на старых кладбищах и болотах вызвано воспламенением на воздухе фосфина PH3 и других соединений, содержащих фосфор. На воздухе продукты соединения фосфора с водородом самовоспламеняются с образованием светящегося пламени и капелек фосфорной кислоты – продукта взаимодействия оксида фосфора(V) с водой. Эти капельки создают размытый контур «привидения».

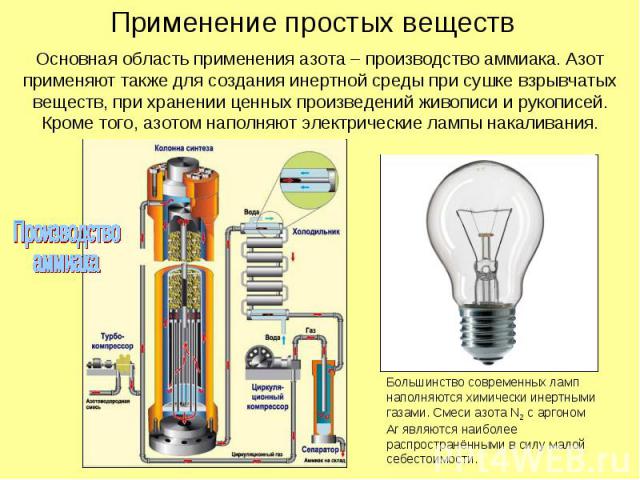
Основная область применения азота – производство аммиака. Азот применяют также для создания инертной среды при сушке взрывчатых веществ, при хранении ценных произведений живописи и рукописей. Кроме того, азотом наполняют электрические лампы накаливания. Применение простых веществ

Красный фосфор используют для производства спичек, фосфорной кислоты, которая, в свою очередь, идет на производство фосфорных удобрений и кормовых добавок для животноводства. Кроме того, фосфор применяют для производства ядохимикатов.

Домашнее задание: Параграф §49.

Список используемых источников http://ru.wikipedia.org/wiki/Азот http://ru.wikipedia.org/wiki/Фосфор http://distant-lessons.ru/ximiya/podgruppa-azota http://www.vredno.com.ua/2011/10/05/ http://21region.org/sections/book/41869-istoriya-spichek.html http://x-ufo.ru/2008/08/19/fotografii_pjejjnobektov_s_kladbishha.html http://www.varson.ru/images/Himia_jpeg_big/7-04.jpg http://lols.ru/2010/11/09/