Презентация на тему: Законы газов

Физические законы, важные для анестезиолога К.М. Лебединский, СПб МАПО 900igr.net

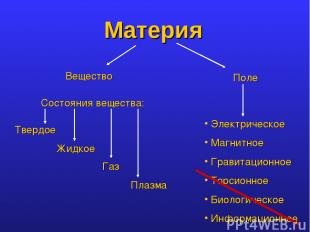
Материя Вещество Поле Состояния вещества: Твердое Жидкое Газ Плазма Электрическое Магнитное Гравитационное Торсионное Биологическое Информационное

«Первичные» физические величины Масса М кг Длина L м Время t с

Производные физические величины Скорость v Lt-1 м/с Ускорение a Lt-2 м/с2 Сила F MLt-2 Н = кг м/с2 Давление P ML-1t-2 Па = Н/м2

Единицы давления Па = Н/м2 см Н2О 100 Па = 0,1 кПа = 1 гПа ат, атм, ата, ати - ? ата 10 м Н2О 100.000 Па = бар мбар = 100 Па 1 см Н2О ати = ата - 1 мм Hg = torr = 133,3 Па
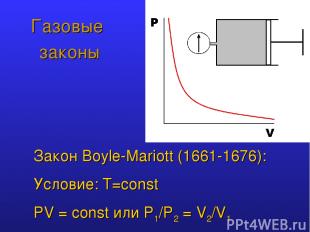
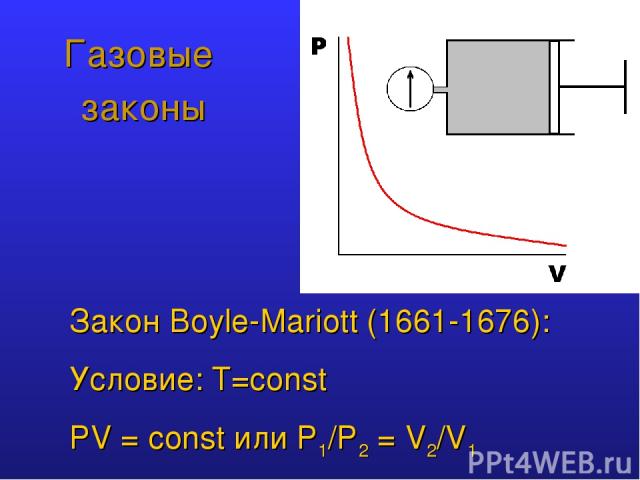
Газовые законы Закон Boyle-Mariott (1661-1676): Условие: T=const PV = const или P1/P2 = V2/V1
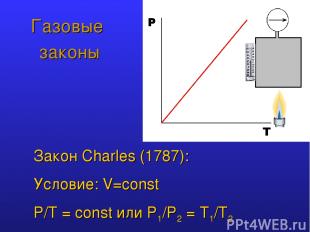
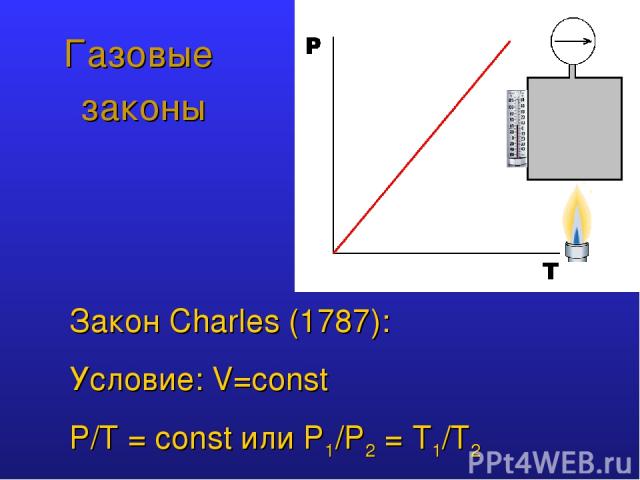
Газовые законы Закон Charles (1787): Условие: V=const P/T = const или P1/Р2 = T1/Т2
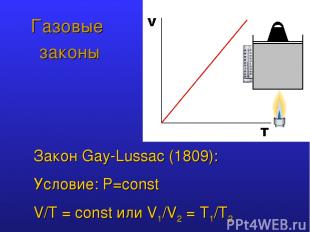
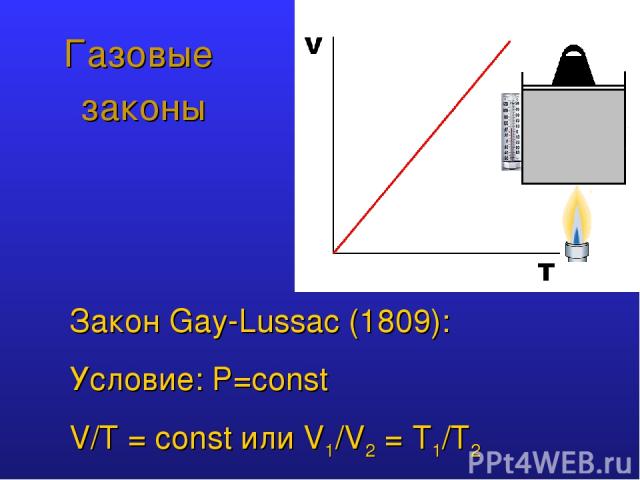
Газовые законы Закон Gay-Lussac (1809): Условие: P=const V/T = const или V1/V2 = T1/Т2
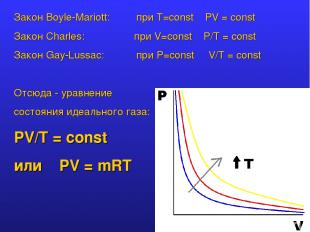
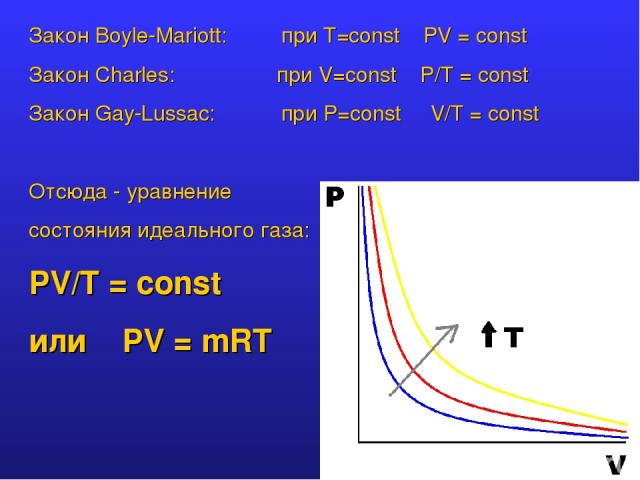
Закон Boyle-Mariott: при T=const PV = const Закон Charles: при V=const P/Т = const Закон Gay-Lussac: при P=const V/T = const Отсюда - уравнение состояния идеального газа: PV/T = const или PV = mRT

Критическая температура: Газ можно перевести в жидкое состояние путем сжатия только при температуре ниже критической (точка перегиба изотермы на диаграмме объем-давление). Критической температуре соответствуют критическое давление, выше которого жидкость и газ сосуществуют в равновесии, и критический объем. Значения tкрит, С: Гелий -268 Углекислый газ 31 Кислород -118 Закись азота 36 Азот -147 Ксенон 17
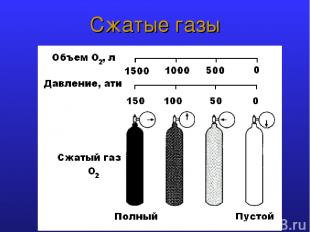
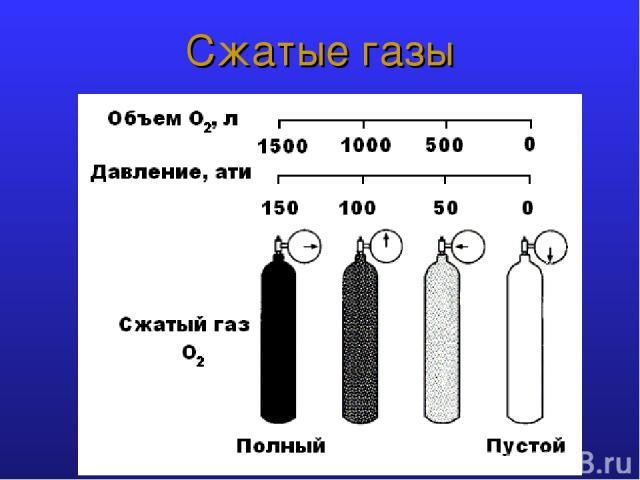
Сжатые газы

Сжиженные газы

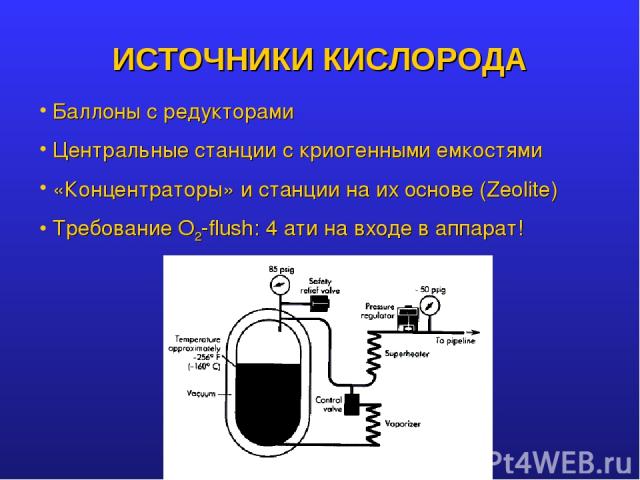
ИСТОЧНИКИ КИСЛОРОДА Баллоны с редукторами Центральные станции с криогенными емкостями «Концентраторы» и станции на их основе (Zeolite) Требование O2-flush: 4 ати на входе в аппарат!

Парциальное (частичное) давление - давление, которое оказывал бы каждый газ в отдельности в том случае, если бы он целиком занимал весь объем, предоставленный смеси газов. Отражая количество молекул газа в объеме и их кинетическую энергию, зависит от доли газа (%) в смеси и от давления смеси как целого: PX = %X Pсмеси Закон Dalton (1801): давление смеси газов равно сумме парциальных давлений компонентов

Закон Avogadro (1811, «молекулярная гипотеза»): 1 моль (6 1023 молекул) любого газа при одинаковых t и Р занимает одинаковый объем – 22,4 л Молярная масса (г/моль) численно равна ОММ (у.е.): Гелий 4 Углекислый газ 44 Кислород 32 Закись азота 44 Азот 28 Ксенон 131

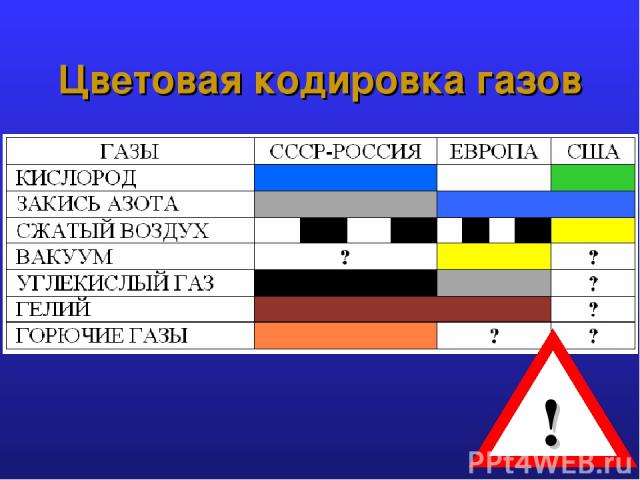
Цветовая кодировка газов !

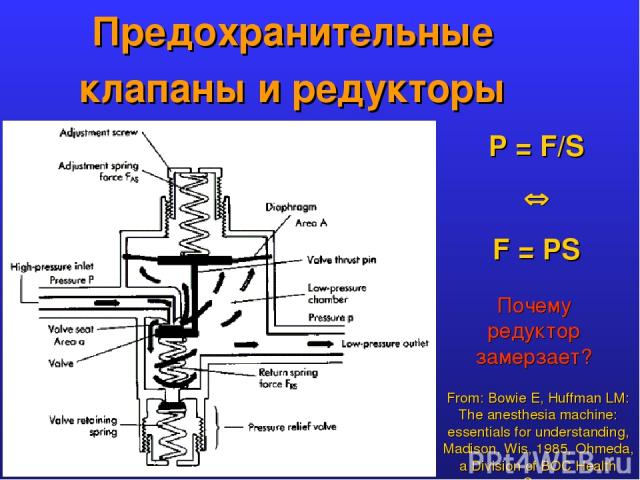
Предохранительные клапаны и редукторы From: Bowie E, Huffman LM: The anesthesia machine: essentials for understanding, Madison, Wis, 1985, Ohmeda, a Division of BOC Health Care P = F/S F = PS Почему редуктор замерзает?
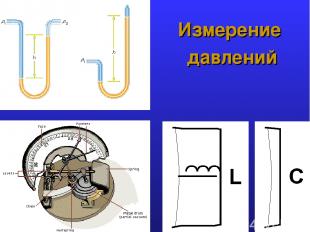
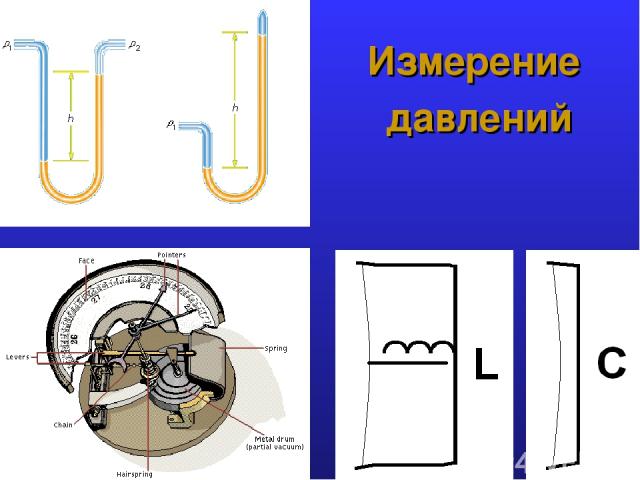
Измерение давлений
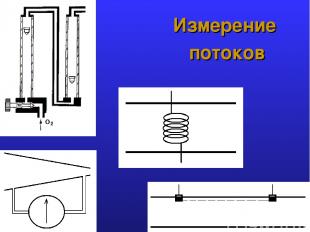
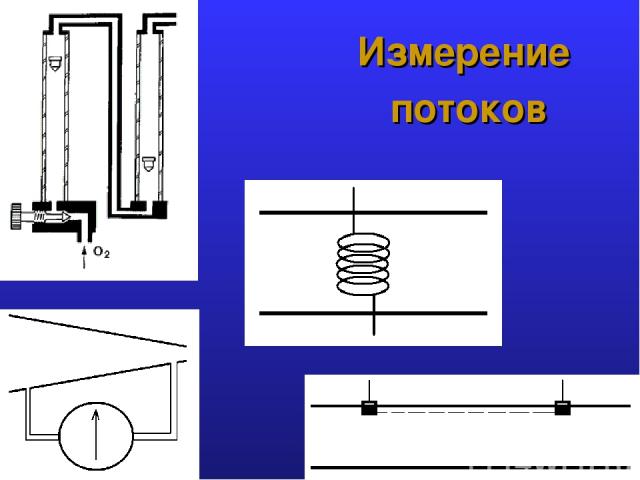
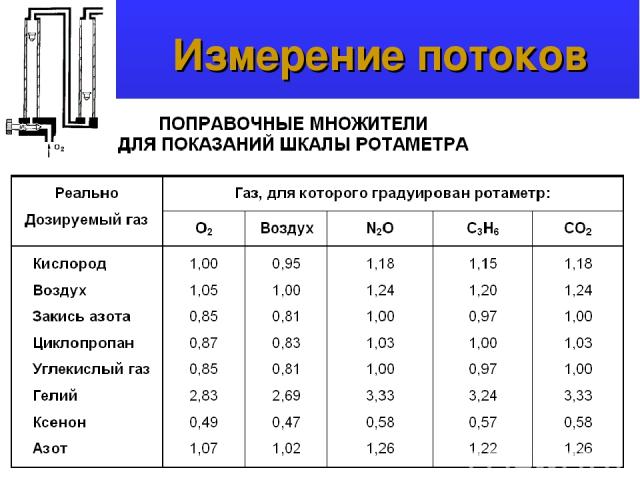
Измерение потоков
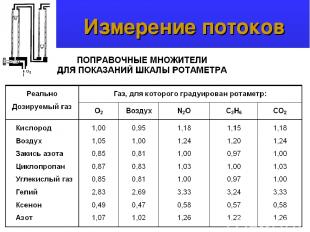
Измерение потоков

Измерение объемов V = Q(t)dt
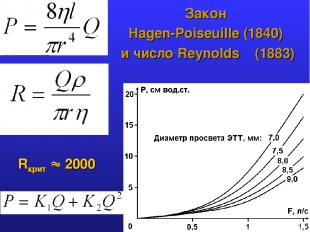
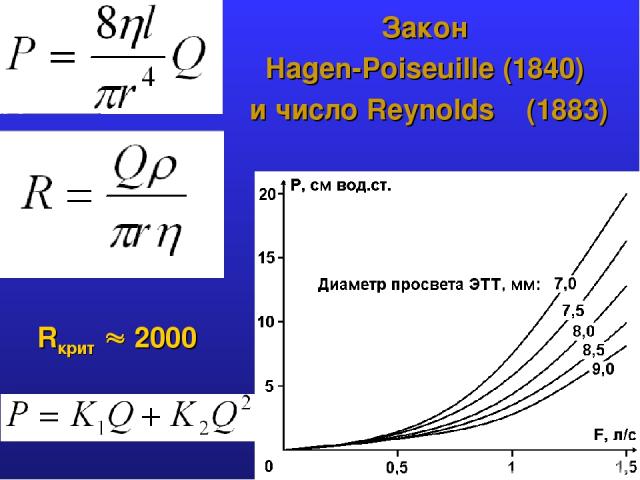
Закон Hagen-Poiseuille (1840) и число Reynolds (1883) Rкрит 2000
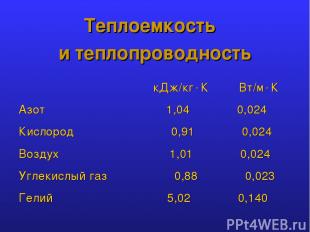
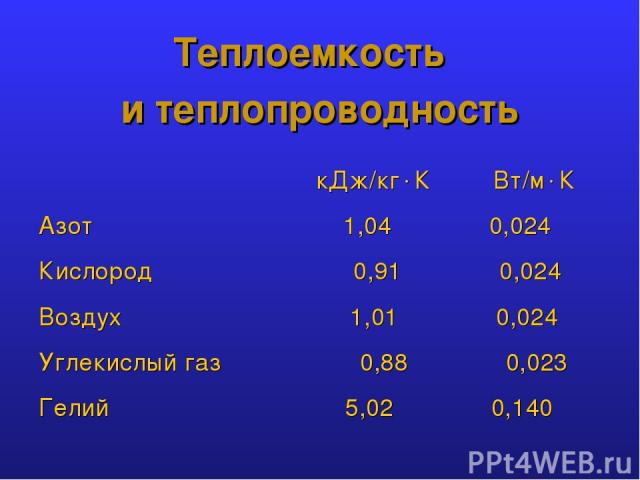
Теплоемкость и теплопроводность кДж/кг К Вт/м К Азот 1,04 0,024 Кислород 0,91 0,024 Воздух 1,01 0,024 Углекислый газ 0,88 0,023 Гелий 5,02 0,140

ВОПРОСЫ ?