Презентация на тему: Теория гибридизации

Теоретические основы органической химии Теория гибридизации Лекция 3 (электронно-лекционный курс) Проф. Бородкин Г.И.

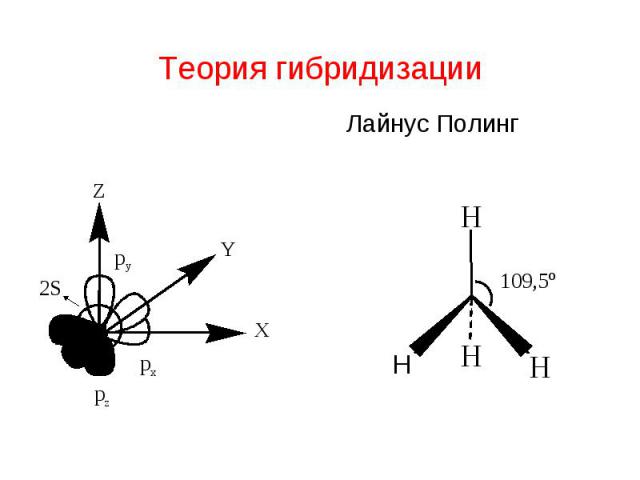
Лаунус Полинг – американский химик, физик (1901-94 гг) Первые исследования по применению квантовой механики к теории химической связи Метод валентных связей, теория резонанса Теория гибридизации Электроотрицательность атомов Биохимические исследования
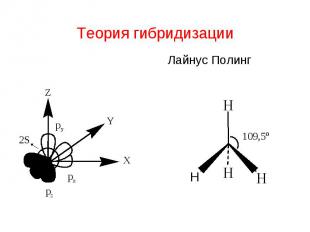
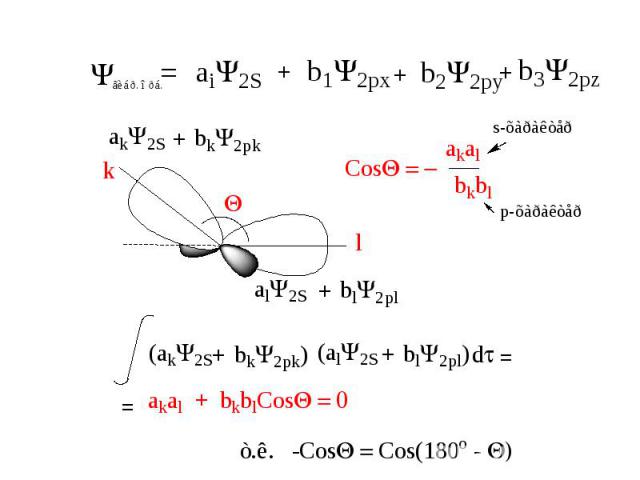
Теория гибридизации

Графан

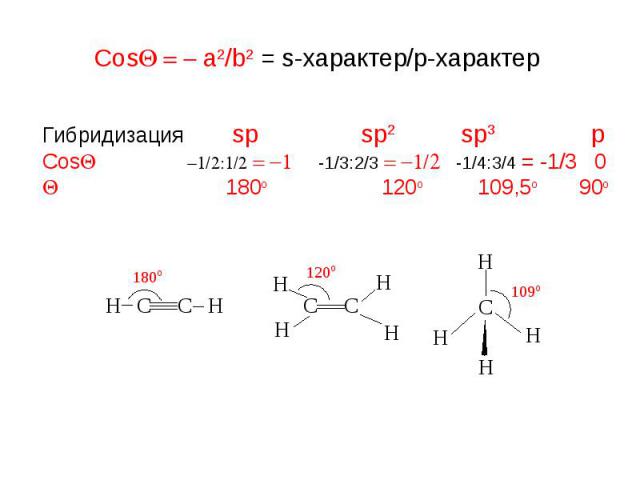
Гибридизация sp sp2 sp3 p CosQ -1/2:1/2 = -1 -1/3:2/3 = -1/2 -1/4:3/4 = -1/3 0 Q 180o 120o 109,5o 90o
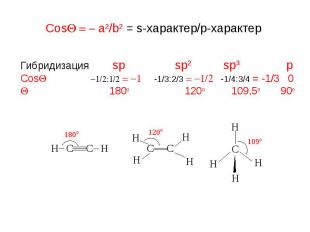
Гибридизация sp sp2 sp3 p CosQ -1/2:1/2 = -1 -1/3:2/3 = -1/2 -1/4:3/4 = -1/3 0 Q 180o 120o 109,5o 90o
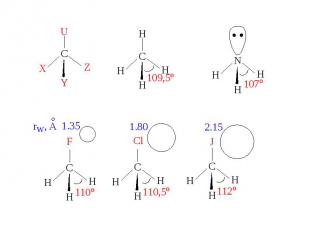
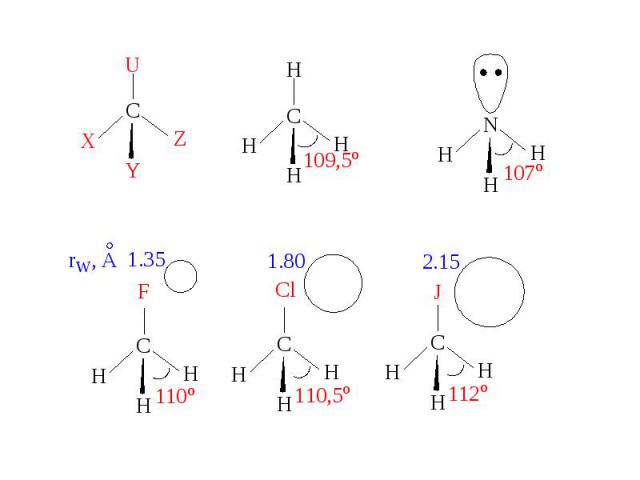
Правило Бента: В соединениях углерода и некоторых других элементов 2-ого периода s-характер концентрируется преимущественно в направлении электроположительного заместителя, а р-характер – электроотрицительного заместителя.

Правило Бента: В соединениях углерода и некоторых других элементов 2-ого периода s-характер концентрируется преимущественно в направлении электроположительного заместителя, а р-характер – электроотрицительного заместителя.
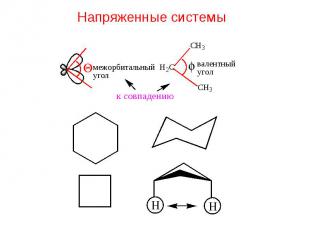
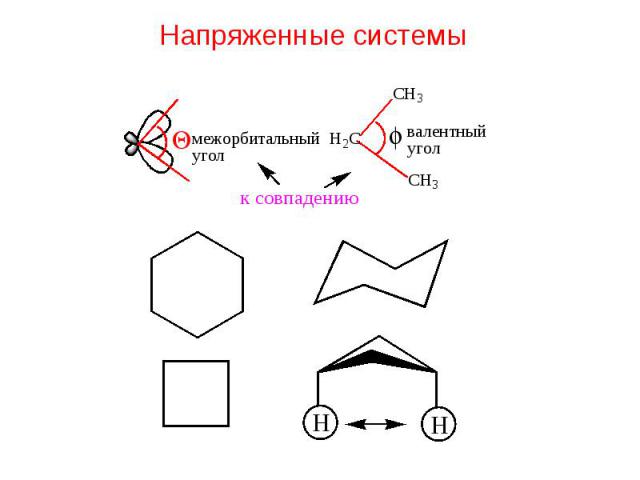
Напряженные системы
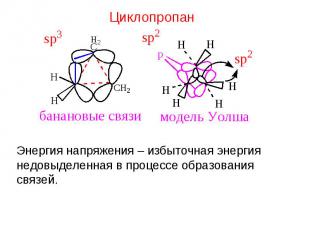
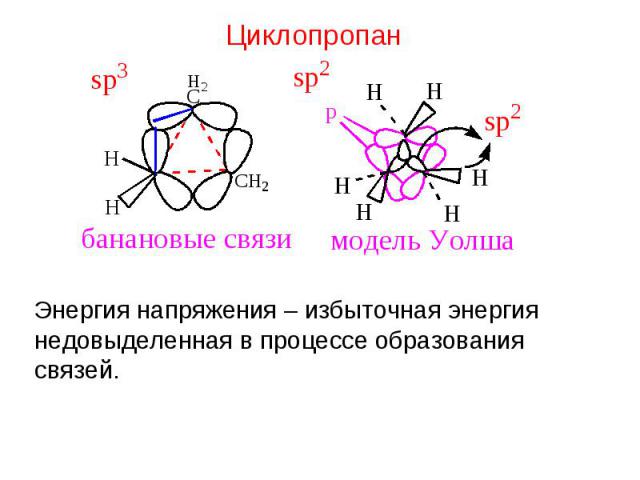
Энергия напряжения – избыточная энергия недовыделенная в процессе образования связей.
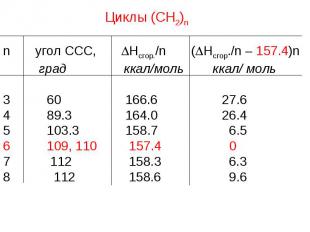
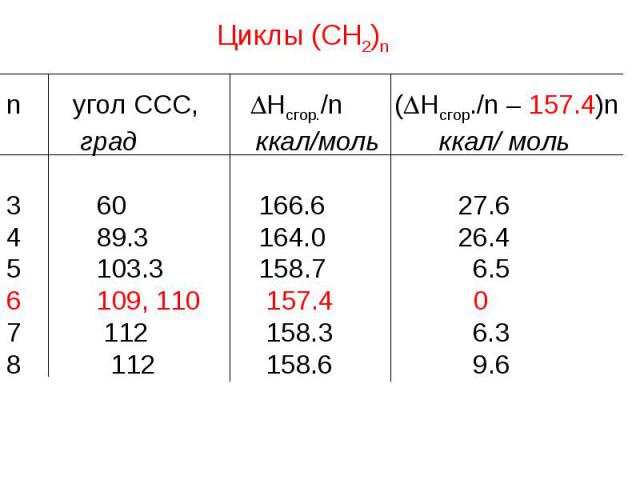
Циклы (СН2)n

h2 - полярность связи С-Н DE - энергия возбуждения связи С-Н до триплетного состояния а2 – s-характер связи С-Н
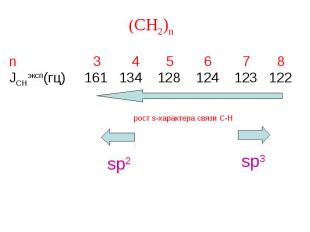
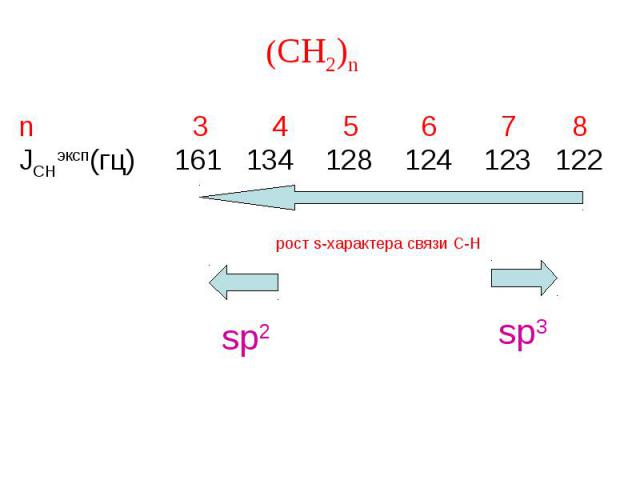
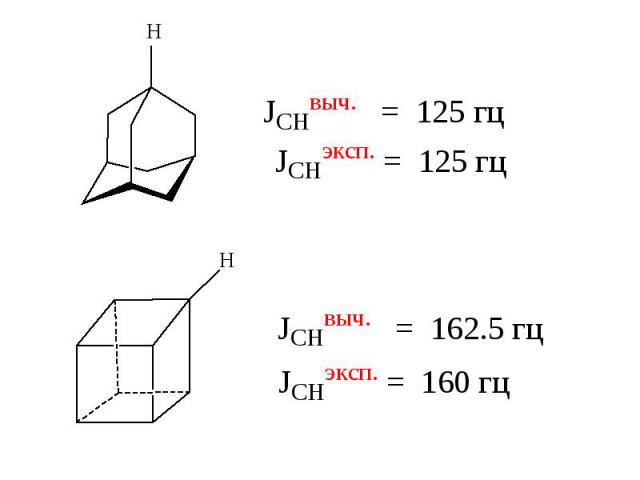
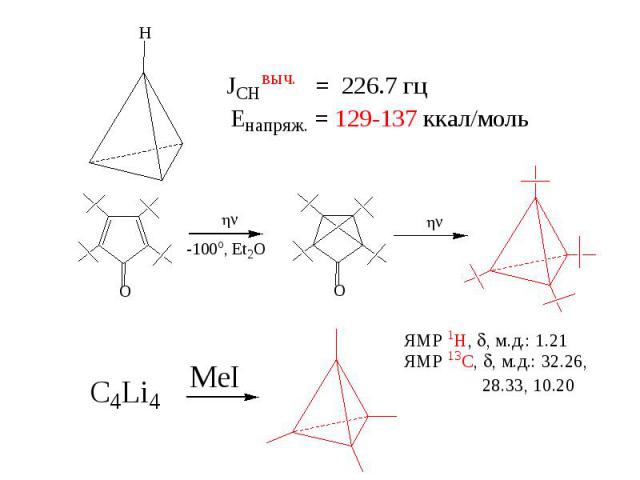
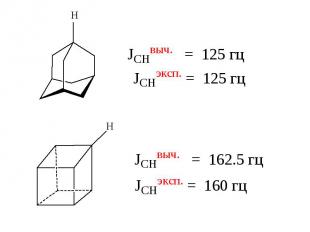
n 3 4 5 6 7 8 JCHэксп(гц) 161 134 128 124 123 122
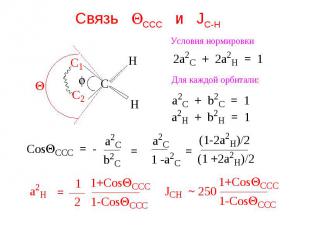
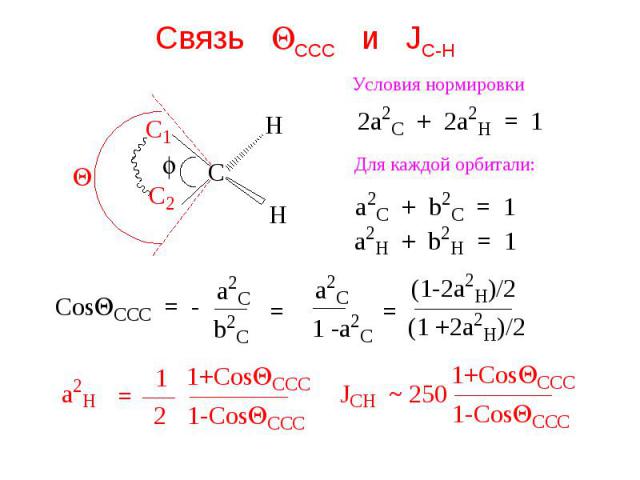
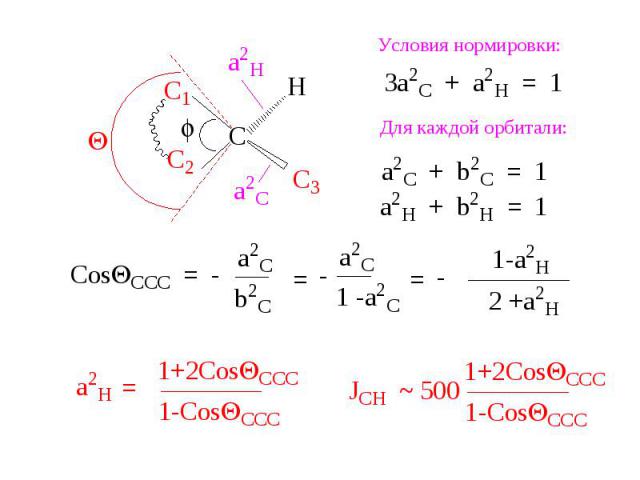
Связь QCCC и JC-H

Принимаем:
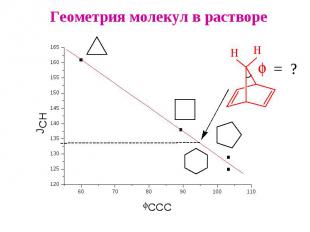
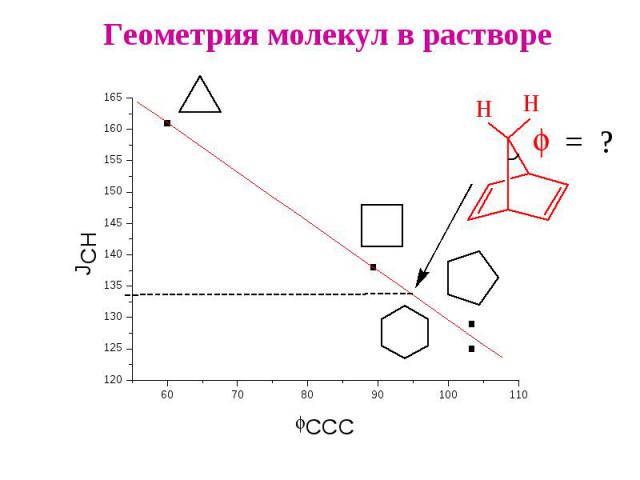
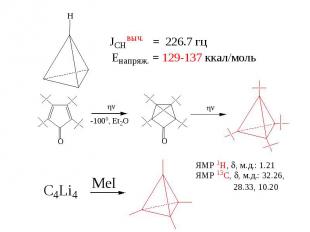
Геометрия молекул в растворе

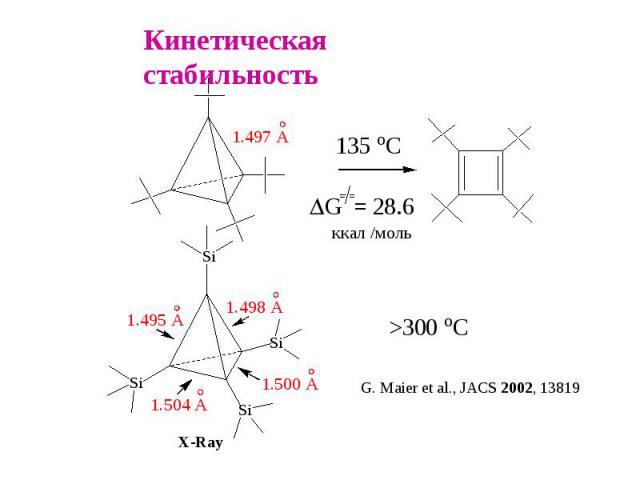
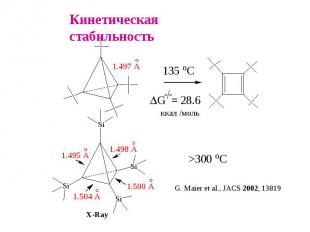
Кинетическая стабильность
Кинетическая стабильность
Кинетическая стабильность
Кинетическая стабильность
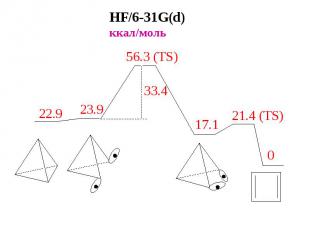
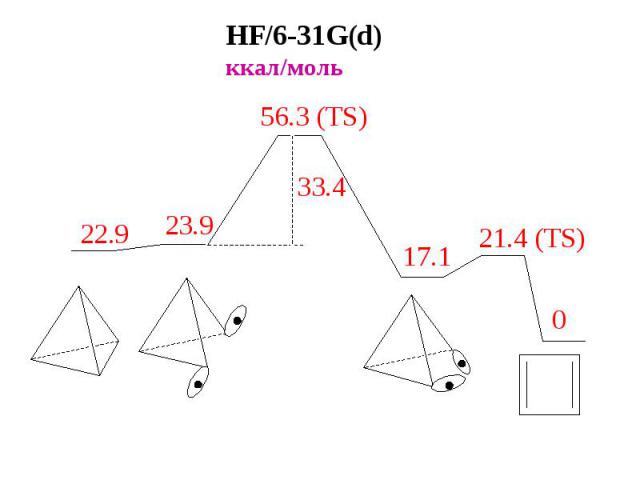
HF/6-31G(d) ккал/моль