Презентация на тему: Строение атома. Опыт Резерфорда

Строение атомаОпыт Резерфорда

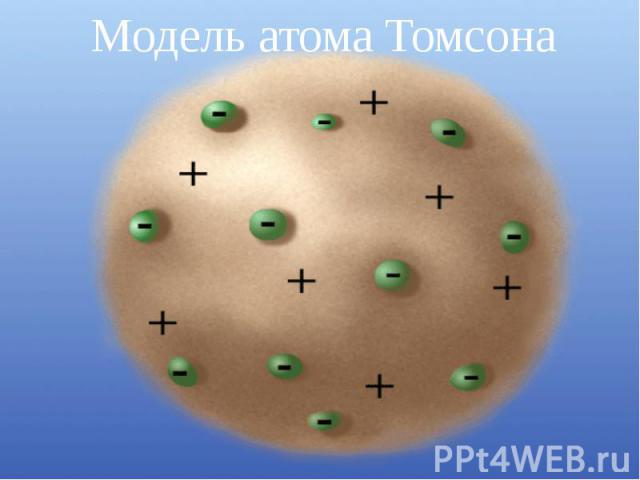
Дж.Дж.Томсон 1896г. -Дж.Дж.Томсон - выдающийся ученый, директор знаменитой Кавендишской лаборатории, лауреат Нобелевской премии. открыл электрон. 1903г. - Дж.Дж.Томсон выдвинул гипотезу о том, что электрон находится внутри атома. Но атом в целом нейтральный, поэтому ученый предположил, что отрицательные электроны окружены в атоме положительно заряженным веществом. Атом, по мысли Дж. Томсона, очень похож на "пудинг с изюмом", где "каша" - положительно заряженное вещество атома., а электроны- " изюм" в ней.
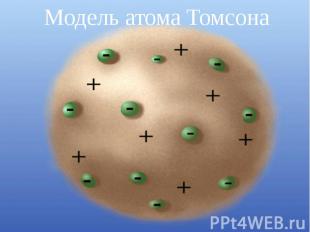
Модель атома Томсона

Через несколько лет в опытах великого английского физика Э. Резерфорда было доказано, что модель Томсона неверна. Эрнест Резерфорд Первые прямые эксперименты по исследованию внутренней структуры атомов были выполнены Э. Резерфордом и его сотрудниками Э. Марсденом и Х. Гейгером в 1909–1911 годах. Резерфорд предложил применить зондирование атома с помощью α-частиц, которые возникают при радиоактивном распаде радия и некоторых других элементов.

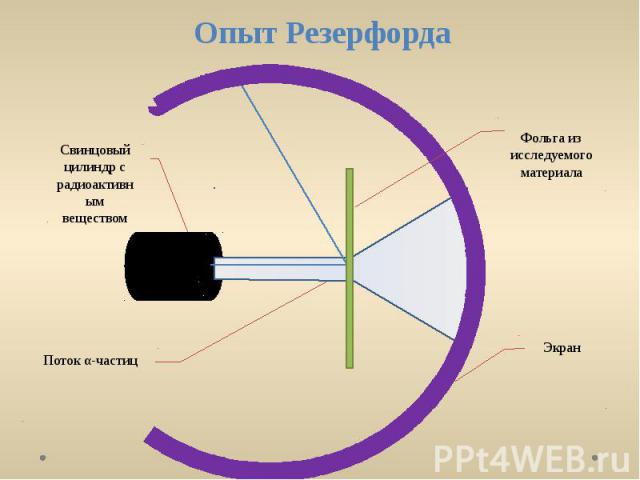
Резерфорд бомбардировал атомы тяжелых элементов (золото, серебро, медь и др.) α-частицами. Электроны, входящие в состав атомов, вследствие малой массы не могут заметно изменить траекторию α-частицы. Рассеяние, то есть изменение направления движения α-частиц, может вызвать только тяжелая положительно заряженная часть атома. От радиоактивного источника, заключенного в свинцовый контейнер, α-частицы направлялись на тонкую металлическую фольгу. Рассеянные частицы попадали на экран, покрытый слоем кристаллов сульфида цинка, способных светиться под ударами быстрых заряженных частиц. Сцинтилляции (вспышки) на экране наблюдались глазом с помощью микроскопа. Наблюдения рассеянных α-частиц в опыте Резерфорда можно было проводить под различными углами φ к первоначальному направлению пучка.
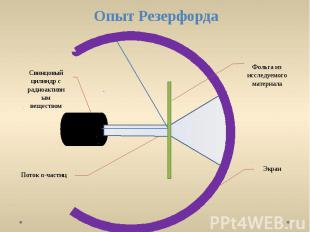
Опыт Резерфорда Свинцовый цилиндр с радиоактивным веществом Поток α-частиц Фольга из исследуемого материала Экран

Было обнаружено, что большинство α-частиц проходит через тонкий слой металла, практически не испытывая отклонения. Однако небольшая часть частиц отклоняется на значительные углы, превышающие 30°. Очень редкие α-частицы (приблизительно одна на десять тысяч) испытывали отклонение на углы, близкие к 180.Этот результат был совершенно неожиданным даже для Резерфорда. Его представления находились в резком противоречии с моделью атома Томсона, согласно которой положительный заряд распределен по всему объему атома. При таком распределении положительный заряд не может создать сильное электрическое поле, способное отбросить α-частицы назад.

Эти соображения привели Резерфорда к выводу, что атом почти пустой, и весь его положительный заряд сосредоточен в малом объеме. Эту часть атома Резерфорд назвал атомным ядром. Так возникла ядерная модель атома. В центре атома находится плотное положительно заряженное ядро, диаметр которого не превышает 10–14–10–15 м. Это ядро занимает только 10–12 часть полного объема атома, но содержит весь положительный заряд и не менее 99,95 % его массы. Веществу, составляющему ядро атома, следовало приписать колоссальную плотность порядка ρ ≈ 1015 г/см3. Заряд ядра должен быть равен суммарному заряду всех электронов, входящих в состав атома. Впоследствии удалось установить, что если заряд электрона принять за единицу, то заряд ядра в точности равен номеру данного элемента в таблице Менделеева.

ПЛАНЕТАРНАЯ МОДЕЛЬ АТОМА

Планетарная модель атома, предложенная Резерфордом, несомненно явилась крупным шагом вперед в развитии знаний о строении атома. Она была совершенно необходимой для объяснения опытов по рассеянию α-частиц, однако оказалась неспособной объяснить сам факт длительного существования атома, т. е. его устойчивость. По законам классической электродинамики, движущийся с ускорением заряд должен излучать электромагнитные волны, уносящие энергию. За короткое время (порядка 10–8 с) все электроны в атоме Резерфорда должны растратить всю свою энергию и упасть на ядро. То, что этого не происходит в устойчивых состояниях атома, показывает, что внутренние процессы в атоме не подчиняются классическим законам.