Презентация на тему: Опыт Резерфорда, модель атома

Модели атомов. Опыт Резерфорда. Презентация урока физики в 9 классе. Учитель Васильева Е.Д. 5klass.net

Проверка домашнего материала: Как назвали способность атомов некоторых химических элементов к самопроизвольному излучению? Как были названы частицы, входящие в состав радиоактивного излучения? Что представляют собой эти частицы? О чём свидетельствовало явление радиоактивности? Расскажите, как проводился опыт Резерфорда, схема которого изображена на рис.136, стр181. Что выяснилось в результате этого опыта?
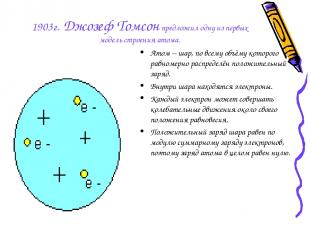
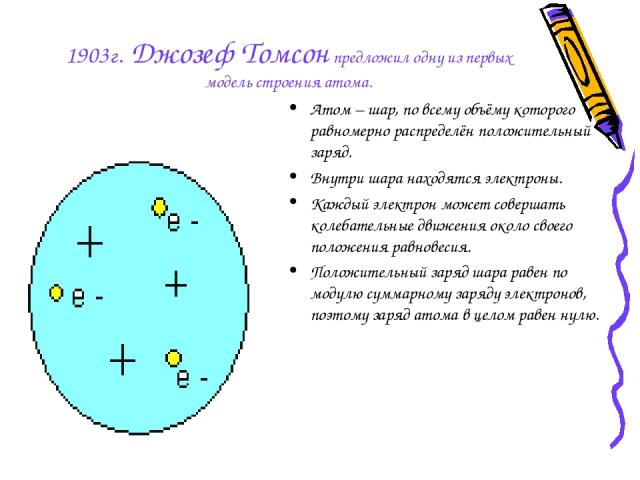
1903г. Джозеф Томсон предложил одну из первых модель строения атома. Атом – шар, по всему объёму которого равномерно распределён положительный заряд. Внутри шара находятся электроны. Каждый электрон может совершать колебательные движения около своего положения равновесия. Положительный заряд шара равен по модулю суммарному заряду электронов, поэтому заряд атома в целом равен нулю.

Модель Томсона нуждалась в экспериментальной проверке. Важно было проверить, действительно ли положительный заряд распределён по всему объёму атома с постоянной плотностью. В 1911г. Эрнест Резерфорд совместно со своими сотрудниками провёл ряд опытов по исследованию состава и строения атомов.

Идея опыта Резерфорда: Зондировать атом альфа–частицами. Альфа-частицы возникают при распаде радия. Масса альфа-частицы в 8000 раз больше массы электрона. Электрический заряд альфа-частицы в 2 раза больше заряда электрона. Скорость альфа-частицы около 15 000 км/с. Альфа-частицы является ядром атома гелия.
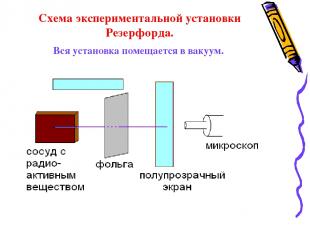
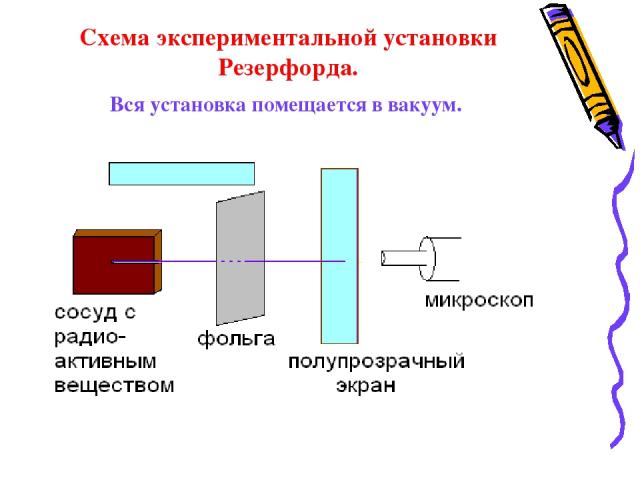
Схема экспериментальной установки Резерфорда. Вся установка помещается в вакуум.

В ходе эксперимента обнаружили: 1. В отсутствии фольги – на экране появлялся светлый кружок напротив канала с радиоактивным веществом. 2. Когда на пути пучка альфа-частиц поместили фольгу, площадь пятна на экране увеличилась. 3. Помещая экран сверху и снизу установки, Резерфорд обнаружил, что небольшое число альфа-частиц отклонилось на углы около 900. 4. Единичные частицы были отброшены назад.

Противоречие модели Томсона с экспериментом: 1. Так как масса электронов мала, они не могут заметно изменить траекторию движения альфа-частиц. 2. Заметное рассеивание альфа-частиц может вызвать только положительная часть атома и лишь в том случае, если она сконцентрирована в очень малом объёме.

Выводы из опыта по рассеиванию альфа-частиц Резерфорда: 1. Существует атомное ядро, т.е. тело малых размеров, в котором сконцентрирована почти вся масса атома и весь положительный заряд. 2. В ядре сконцентрирована почти вся масса атома. 3. Вокруг ядра по замкнутым орбитам вращаются отрицательные частицы- электроны. 4. отрицательный заряд всех электронов распределён по всему объёму атома. Ядерная модель атома:

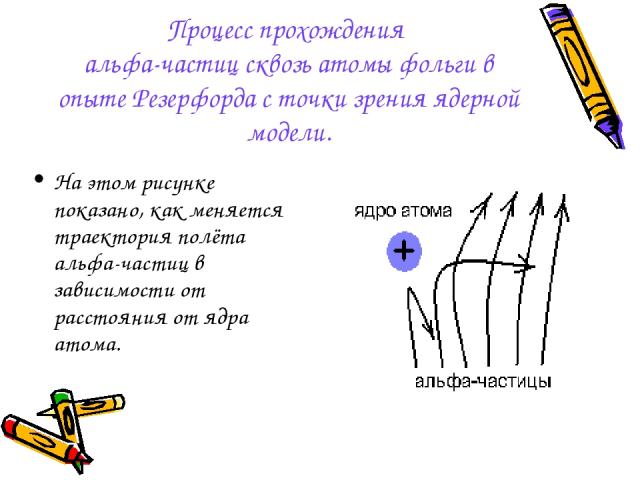
Процесс прохождения альфа-частиц сквозь атомы фольги в опыте Резерфорда с точки зрения ядерной модели. На этом рисунке показано, как меняется траектория полёта альфа-частиц в зависимости от расстояния от ядра атома.

Недостаток планетарной модели атома: Нельзя объяснить факт существования атома; Нельзя объяснить устойчивость атома.

Вопросы на закрепление: 1. В чём заключается сущность модели Томсона? 2. В чём заключалась идея опыта Резерфорда? 3. Объясните по схеме опыт Резерфорда по рассеиванию альфа-частиц. (Схема экспериментальной установки Резерфорда.) 4. Объясните причину рассеивания альфа-частиц атомами вещества. 5. В чём сущность планетарной модели атома?