Презентация на тему: Молекулярная физика

МОЛЕКУЛЯРНАЯ ФИЗИКА 900igr.net

Основные положения МКТ Все вещества состоят из молекул, которые разделены промежутками. Молекулы беспорядочно движутся. Между молекулами есть силы взаимодействия.

Качественный анализ МКТ 1 положение МКТ доказывается наблюдением за молекулами с помощью ионного проектора или электронного микроскопа и явлением диффузии – перемешиванием газов, жидкостей и твердых тел при непосредственном контакте. 2 положение МКТ доказывается с помощью диффузии и броуновского движения – теплового движения взвешенных в жидкости или в газе частиц. 3 положение МКТ доказывается с помощью давления на стенки сосуда, силы упругости.

Количественный анализ МКТ NА = 6,02 * 1023 – постоянная Авогадро. M = m0 · NA. Основное уравнение МКТ для газов где n – концентрация вещества, – среднеквадратичная скорость молекул, Eср – средняя кинетическая энергия поступательного движения молекул, k = 1,38·10–23 Дж/К – постоянная Больцмана

ТЕМПЕРАТУРА Температура – мера средней кинетической энергии молекул. В физике общепринятой является абсолютная температура T. Ее точка отсчета смещена относительно шкалы Цельсия на 273,15 ºC, а единица шкалы – кельвин – совпадает с градусом Цельсия. Таким образом, p = nkT. k – постоянная Больцмана = 1,38*10-23 Дж/К 1000 373К 00 273К -2730 0К Шкалы Цельсия кельвина T = t0c + 273,15 .

Уравнение состояния идеального газа Уравнение Менделеева - Клапейрона Здесь ν – количество вещества, R = 8,31 Дж/(моль·К) – универсальная газовая постоянная.

ГАЗОВЫЕ ЗАКОНЫ Количественные зависимости между двумя параметрами газа при фиксированном значении третьего называют газовыми законами. T=const; Изотермический процесс. P=const; Изобарный процесс. V=const; Изохорный процесс.
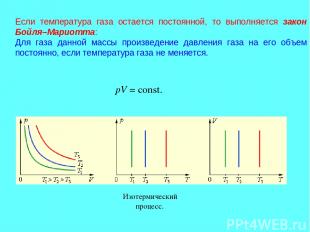
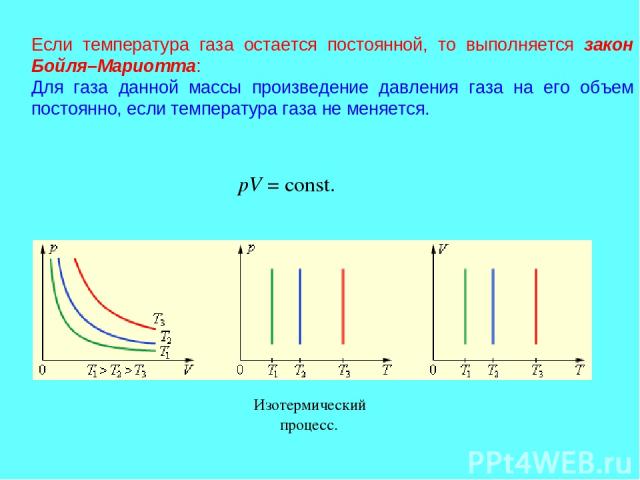
Если температура газа остается постоянной, то выполняется закон Бойля–Мариотта: Для газа данной массы произведение давления газа на его объем постоянно, если температура газа не меняется. pV = const. Изотермический процесс.
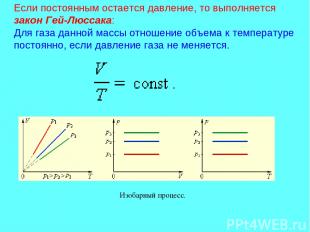
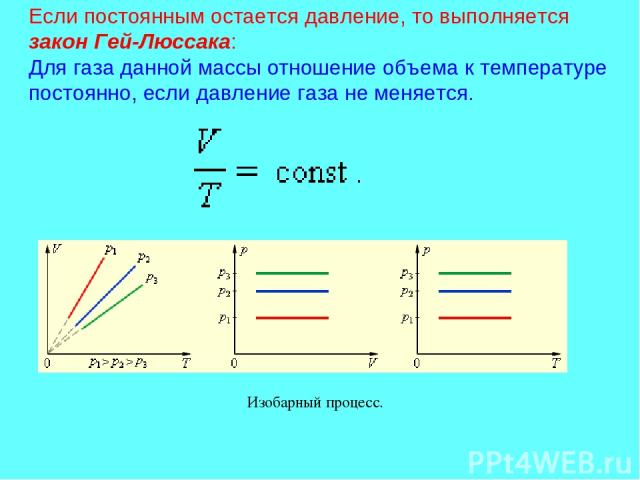
Если постоянным остается давление, то выполняется закон Гей-Люссака: Для газа данной массы отношение объема к температуре постоянно, если давление газа не меняется. Изобарный процесс.
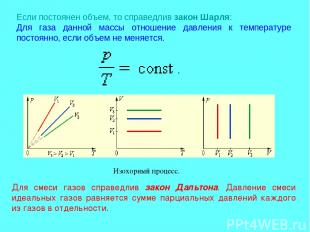
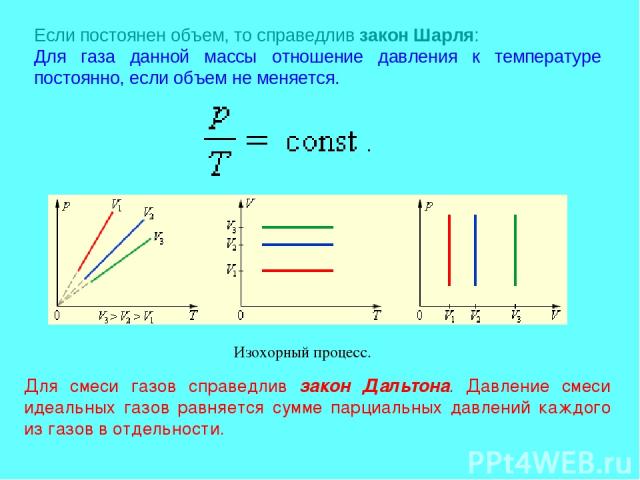
Если постоянен объем, то справедлив закон Шарля: Для газа данной массы отношение давления к температуре постоянно, если объем не меняется. Для смеси газов справедлив закон Дальтона. Давление смеси идеальных газов равняется сумме парциальных давлений каждого из газов в отдельности. Изохорный процесс.

Найди соответствие величины и формулы Величина 1. Масса молекулы 2. молярная масса 3. количество вещества 4. число Авогадро 5. постоянная Больцмана 6. универсальная газовая постоянная 7. уравнение состояния идеал. Газа 8. основное уравнение МКТ 9. число молекул 10.уравнение Клапейрона 11.закон Шарля 12.закон Гей-Люссака 13.энергия движения молекул 14.закон Бойля-Мариотта формула 1. NA=6,02*1023 2. k=1,38*10-23Дж/К 3. R=8,3 Дж/моль.К 4. M=Mr*10-3кг/моль 5. m0=M/NA 6. υ=m/M 7. E=1,5kT 8. p=nkT 9. p=m0nv2/3 10. V1/T1=V2/T2 11. pV=mRT/M 12. pV/T=R 13. p1V1=p2V2 14. p1/T1=p2/T2