Презентация на тему: Модели строения атома

Модель строения атома. Опыты Резерфорда Выполнила: Готманова Елена Анатольевна, учитель физики МОУ «СОШ № 15» р.п. Первомайский Щекинского района 14.02.2009 г. 900igr.net

Цели и задачи Познакомить учащихся с моделями строения атома; Выяснить принципиальные отличия в строении этих моделей; Показать с помощью экспериментальных проверок состоятельность этих моделей; Научить использовать знания о строении атома в химии и астрономии
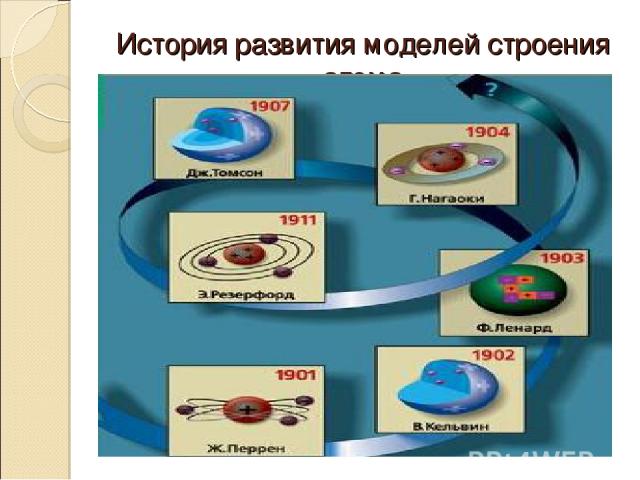
История развития моделей строения атома

Модель атома Томсона Атом выступал в виде положительно заряженной «капли», внутри которой «плавали» отрицательно заряженные шарики - электроны, так что атом подобен кексу, в котором роль изюминок играют электроны. Каждый электрон может совершать колебательные движения около своего положения равновесия. Положительный заряд шара равен по модулю суммарному отрицательному заряду электронов, поэтому электрический заряд атома в целом равен нулю.

Историческая справка ТОМСОН Джозеф Джон (1856-1940), английский физик, основатель научной школы, член (1884) и президент (1915- 1920) Лондонского Королевского общества, иностранный член- корреспондент Петербургской АН (1913) и иностранный почетный член (1925) АН СССР. Директор Кавендишской лаборатории (1884- 1919). Исследовал прохождение электрического тока через разреженные газы. Открыл (1897) электрон и определил (1898) его заряд. Предложил (1903) одну из первых моделей атома. Один из создателей электронной теории металлов. Нобелевская премия (1906).

Модель атома Резерфорда В центре расположено положительно заряженное атомное ядро, в котором сосредоточена почти вся масса атома. В целом атом нейтрален. Поэтому число внутриатомных электронов, как и заряд ядра, равно порядковому номеру элемента в периодической системе. Покоиться электроны внутри атома не могут, т.к. они упали бы на ядро. Они движутся вокруг ядра. Такой характер движения электронов определяется действием кулоновских сил со стороны ядра (одноименные заряды притягиваются).

Историческая справка РЕЗЕРФОРД Эрнест (1871-1937), английский физик, один из создателей учения о радиоактивности и строении атома, основатель научной школы, иностранный член-корреспондент РАН (1922) и почетный член АН СССР (1925). Директор Кавендишской лаборатории (с 1919). Открыл (1899) альфа- и бета-лучи и установил их природу. Создал (1903, совместно с Ф. Содди) теорию радиоактивности. Предложил (1911) планетарную модель атома. Осуществил (1919) первую искусственную ядерную реакцию. Предсказал (1921) существование нейтрона. Нобелевская премия (1908).

Сравните фотографии. В чем сходство и различие этих фотографий?

Строения атома с точки зрения химии В центре атома находится ядро, состоящее из протонов и нейтронов, а вокруг ядра движутся электроны. Так как атом в целом электронейтрален, то, следовательно, число электронов, движущихся вокруг ядра атома, должно быть равно заряду ядра, который в свою очередь равен порядковому номеру элемента.

Методы, подтверждающие правильность гипотезы Резерфорда Метод рассеивания α - частиц Пропуская пучок α-частиц через тонкую фольгу, Э.Резерфорд обнаружил, что какая-то часть частиц отклоняется на довольно значительный угол от своего первоначального направления, а небольшая часть частиц отражается от фольги. Доказывает, что атом имеет ядро, в котором сконцентрирована почти все масса атома.

Метод сцинтилляции. Средством регистрации излучений был экран, покрытый люминесцирующим веществом . Это вещество светится при ударе о него заряженной частицы, если энергии этой частицы достаточно для возбуждения атомов вещества. В том месте, куда частица попадает, возникает вспышка – сцинтилляция. Вспышки на экране наблюдаются с помощью микроскопа.
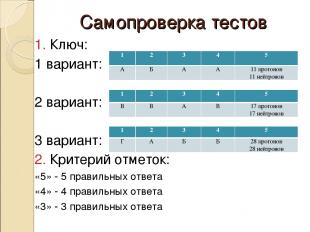
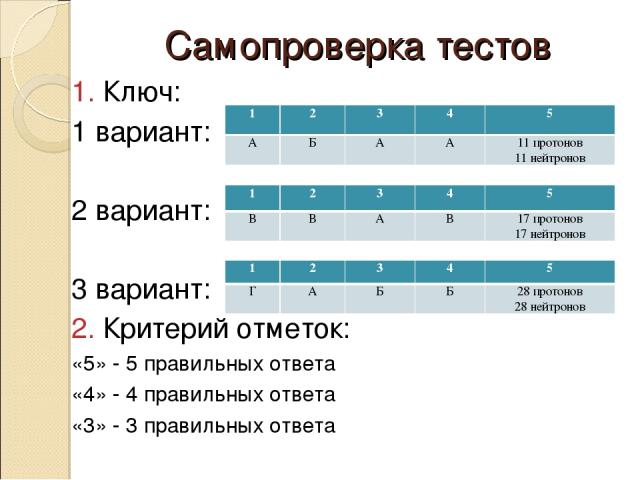
Самопроверка тестов 1. Ключ: 1 вариант: 2 вариант: 3 вариант: 2. Критерий отметок: «5» - 5 правильных ответа «4» - 4 правильных ответа «3» - 3 правильных ответа 1 2 3 4 5 А Б А А 11 протонов 11 нейтронов 1 2 3 4 5 В В А В 17 протонов 17 нейтронов 1 2 3 4 5 Г А Б Б 28 протонов 28 нейтронов

Домашнее задание 1. § 56, написать минисочинение (не менее 10 предложений) о том, что было бы на Земле, если бы вещество не могло делиться на атомы