Презентация на тему: Газы, газовые законы

Приключения в Школе приведений Урок решения задач в 10 классе Элективный курс 5klass.net

Цели урока: 1. Закрепление знаний об идеальном газе, изопроцессах. 2. Формирование умений решения задач на применение уравнения состояния идеального газа и построение графиков изопроцессов. 3. Прививать интерес к решению задач по физике.

Газовые законы Учебная презентация для 10 класса
Проверка P давление V объем T температура

Макроскопические параметры Параметры, характеризующие состояние газа без учета его молекулярного строения, называются макроскопическими. ? Назовите эти параметры.

Изопроцессы Процессы, протекающие в термодинамической системе при одном неизменном макроскопическом параметре когда два других изменяются, называются изопроцессами. Вопрос: какие параметры называются макроскопическими? Нажми для проверки
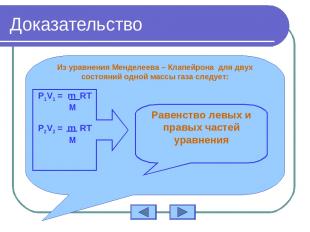
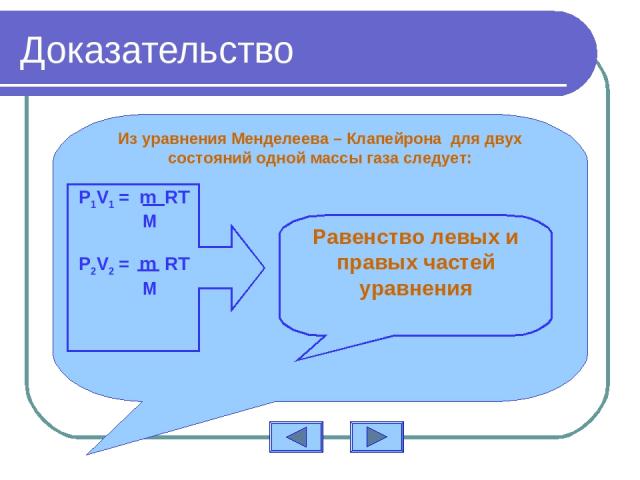
Доказательство Из уравнения Менделеева – Клапейрона для двух состояний одной массы газа следует: P1V1 = m RT M P2V2 = m RT M Равенство левых и правых частей уравнения
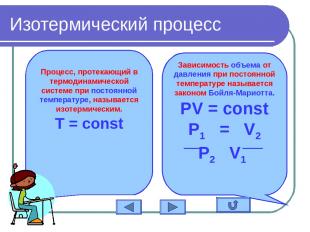
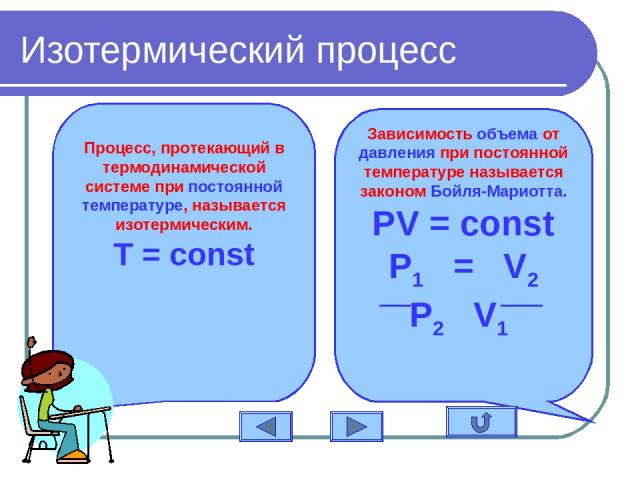
Изотермический процесс Процесс, протекающий в термодинамической системе при постоянной температуре, называется изотермическим. T = const Зависимость объема от давления при постоянной температуре называется законом Бойля-Мариотта. PV = const P1 = V2 P2 V1
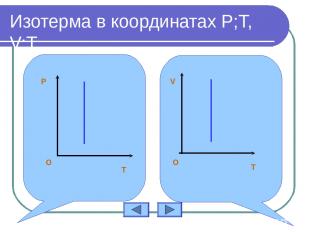
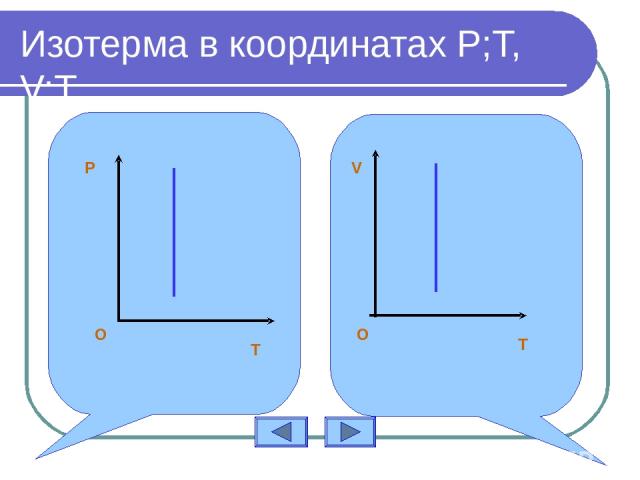
Изотерма в координатах P;T, V;T P T O T V O
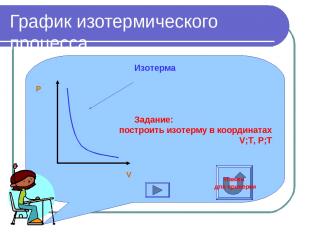
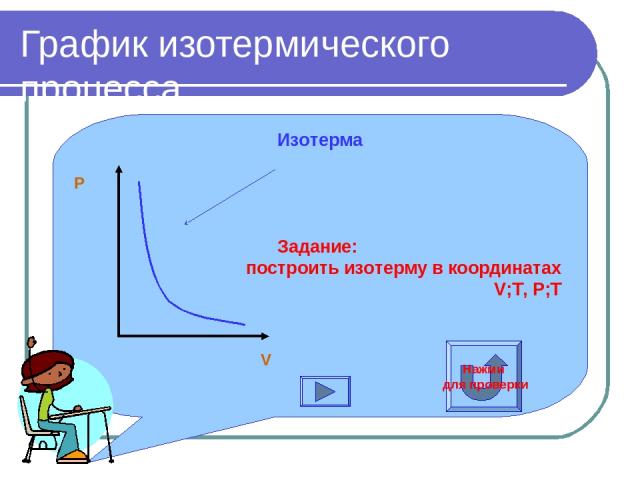
График изотермического процесса Изотерма Задание: построить изотерму в координатах V;T, P;T V P Нажми для проверки
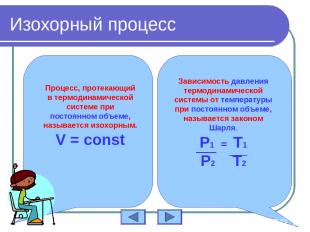
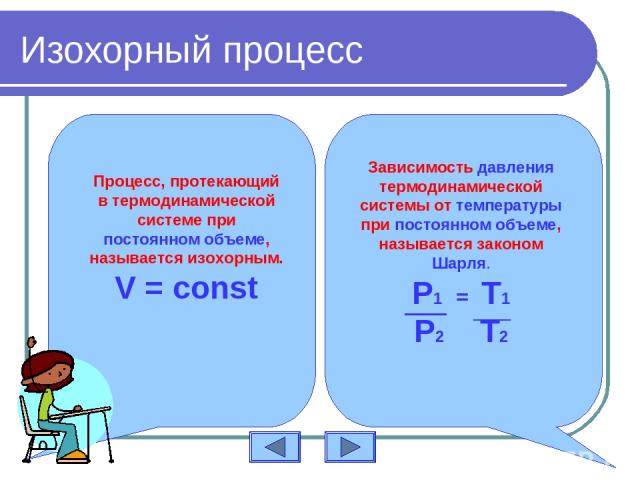
Изохорный процесс Процесс, протекающий в термодинамической системе при постоянном объеме, называется изохорным. V = const Зависимость давления термодинамической системы от температуры при постоянном объеме, называется законом Шарля. P1 = T1 P2 T2
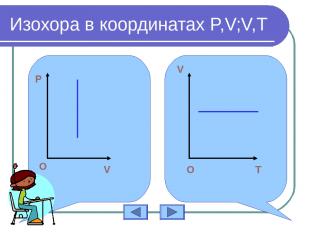
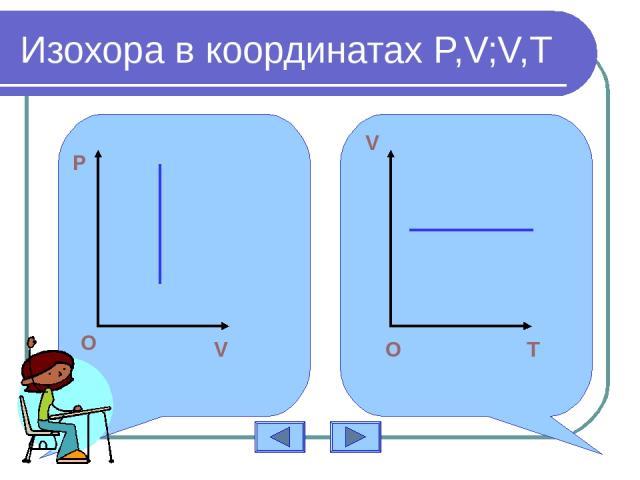
Изохора в координатах P,V;V,T О T V O O O
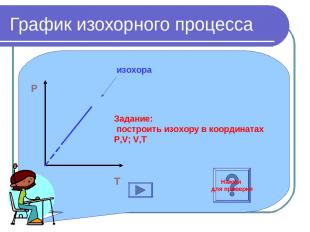
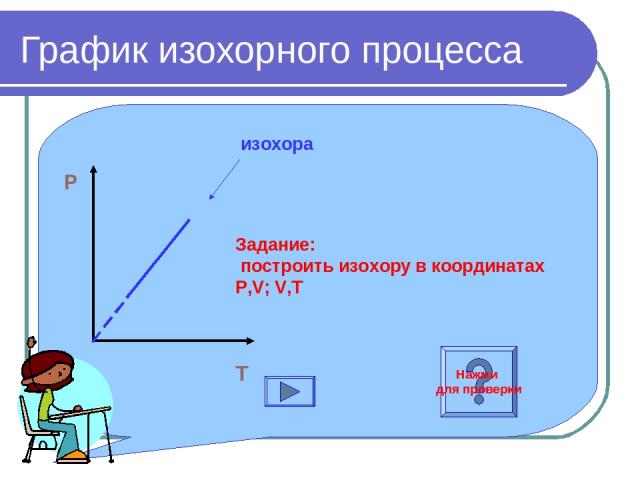
График изохорного процесса P O T изохора Задание: построить изохору в координатах P,V; V,T Нажми для проверки
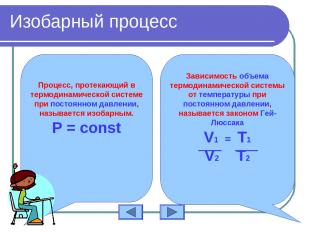
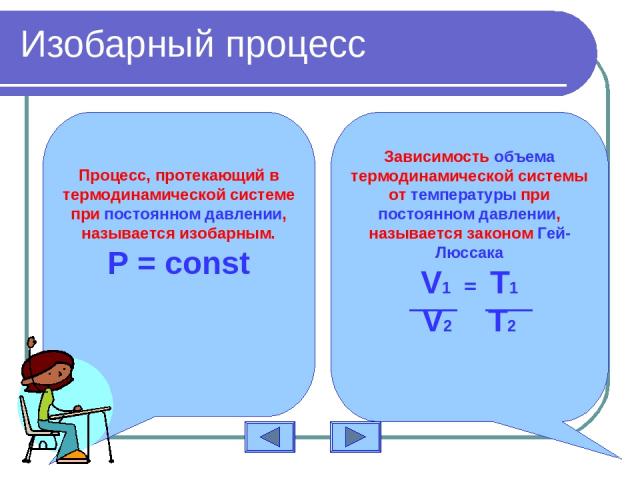
Изобарный процесс Процесс, протекающий в термодинамической системе при постоянном давлении, называется изобарным. Р = const Зависимость объема термодинамической системы от температуры при постоянном давлении, называется законом Гей-Люссака V1 = T1 V2 T2
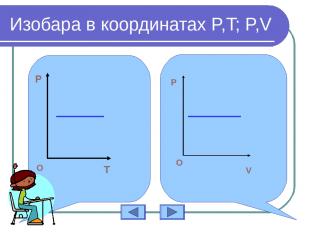
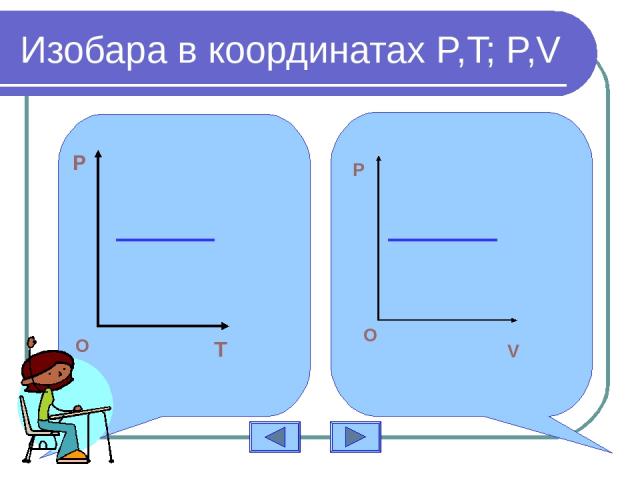
Изобара в координатах P,T; P,V P T O P O V
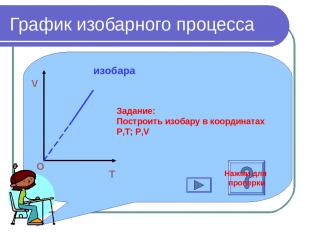
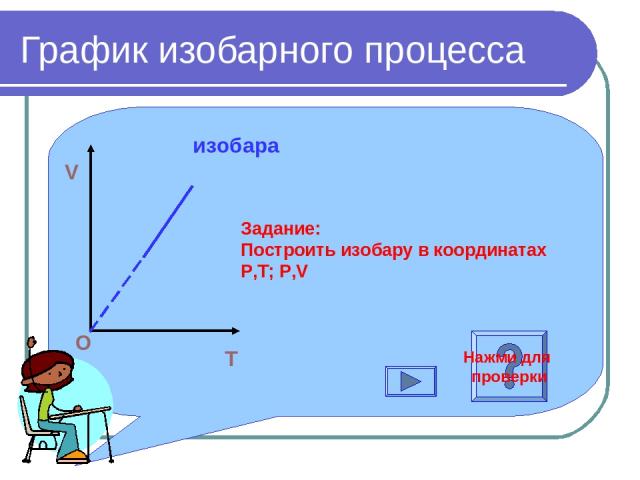
График изобарного процесса T V O изобара Задание: Построить изобару в координатах Р,Т; Р,V Нажми для проверки
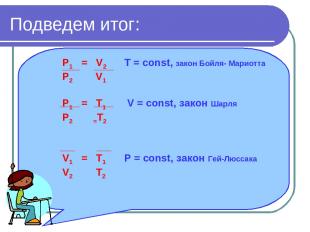
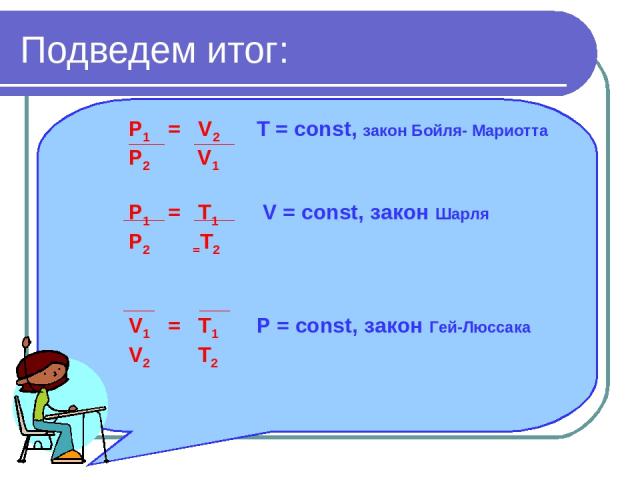
Подведем итог: P1 = V2 T = const, закон Бойля- Мариотта P2 V1 P1 = T1 V = const, закон Шарля P2 =T2 V1 = T1 Р = const, закон Гей-Люссака V2 T2
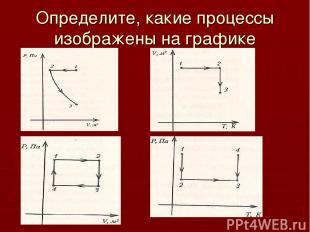
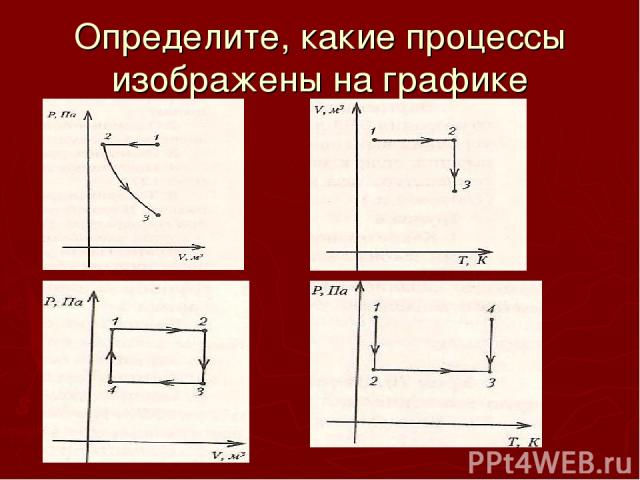
Определите, какие процессы изображены на графике
Графическое представление газовых процессов Базовый уровень 10 класс
Графики газовых процессов изображают в координатах p,V; p,T; V,T. Перед построением графика следует получить аналитическое выражение функции процесса из уравнения Менделеева-Клапейрона или уравнений газовых законов. Введение
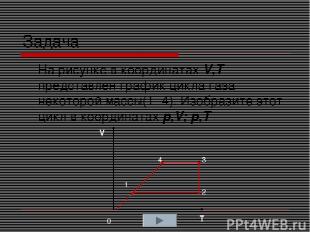
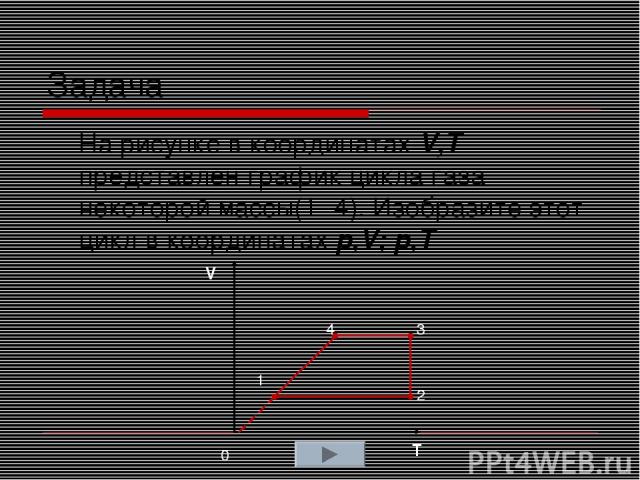
Задача На рисунке в координатах V,T представлен график цикла газа некоторой массы(1 -4). Изобразите этот цикл в координатах p,V; p,T V T 1 4 3 2 0
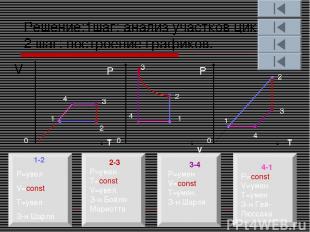
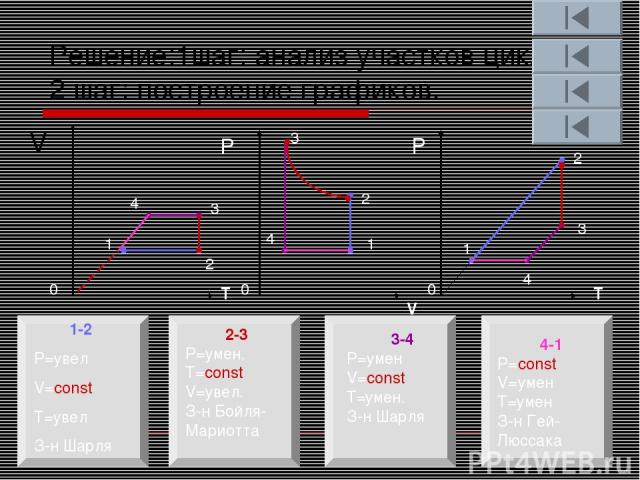
Решение:1шаг: анализ участков цикла. 2 шаг: построение графиков. V T V T Р Р 0 0 0 1 2 3 4 1-2 P=увел V=const T=увел З-н Шарля 2-3 P=умен. T=const V=увел. З-н Бойля-Мариотта 3-4 P=умен V=const T=умен. З-н Шарля 4-1 P=const V=умен T=умен З-н Гей-Люссака 1 2 3 4 1 2 3 4
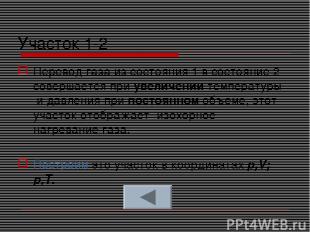
Участок 1-2 Перевод газа из состояния 1 в состояние 2 совершается при увеличении температуры и давления при постоянном объеме, этот участок отображает изохорное нагревание газа. Построим это участок в координатах p,V; p,T.
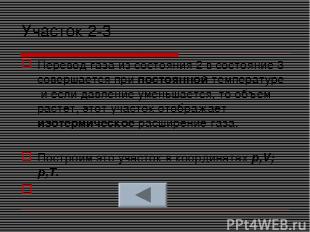
Участок 2-3 Перевод газа из состояния 2 в состояние 3 совершается при постоянной температуре и если давление уменьшается, то объем растет, этот участок отображает изотермическое расширение газа. Построим это участок в координатах p,V; p,T.
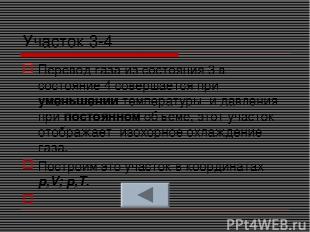
Участок 3-4 Перевод газа из состояния 3 в состояние 4 совершается при уменьшении температуры и давления при постоянном объеме, этот участок отображает изохорное охлаждение газа. Построим это участок в координатах p,V; p,T.
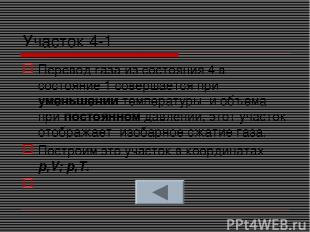
Участок 4-1 Перевод газа из состояния 4 в состояние 1 совершается при уменьшении температуры и объема при постоянном давлении, этот участок отображает изобарное сжатие газа. Построим это участок в координатах p,V; p,T.

Ученики школы Привидений: Каспер – водород, Микки – воздух, Олес – углекислый газ, Лулу – идеальный газ, Лоло – гелий, Лили – аргон, Марго и Янек – просто газы, Ольгерд – азот, Рышард – инертный газ.

Задача 1 Каспер решил отдохнуть и залез в банку объемом 20 л. Найдите давление Каспера, если его масса 4 г и температура 270С.

СИ: m= 4·10 -3 кг V= 2 ·10 -2 м3 T= 300 К M= 2·10 -3 кг/моль р - ? Решение: Ответ:

Задача 2 Лулу, идеальную во всех отношениях, в темном коридоре подкараулили завидующие её фигуре Лоло и Лили. После того как Лулу как следует разозлили, её абсолютная температура увеличилась в 2 раза, а давление подскочило на 25 %. Нанесло ли все это урон фигуре Лулу и во сколько раз изменился её объем?

Дано: Т1= Т Т2= 2Т р1= р Р2= 1,25р Решение:

Решение:

Задачи Задача Ивлевой Юли Задача о Марго Задача про трубку с ртутью Задача о Янеке Задача

Проверь свои знания по теме «Уравнение состояния идеального газа» Тренировочный тест

1.Назови макроскопические параметры: Масса, давление, объем, температура давление, объем, температура

К макроскопическим параметрам идеального газа относятся: давление, объем и температура! P, V, T

2.Из предложенных формул выбери уравнение состояния идеального газа P = 1/3 mov2n PV = m/MRT P = 2/3nE PV = 3/2kT

Неправильно! Повтори теорию!
Молодец! Переходи к следующему вопросу

Неправильно! Повтори теорию!

Уравнением состояния идеального газа называется зависимость между макроскопическими параметрами: давлением, объемом и температурой! pv = m/MRT

Молодец! Переходи к следующему вопросу
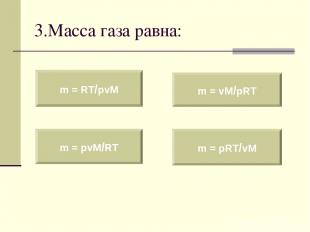
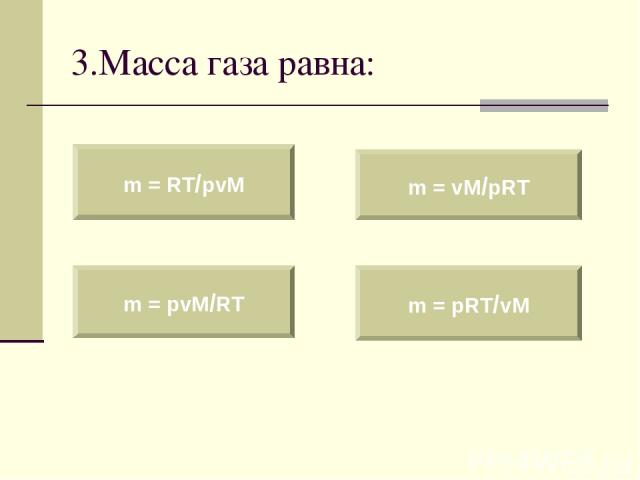
3.Масса газа равна: m = RT/pvM m = pvM/RT m = vM/pRT m = pRT/vM
Молодец! Переходи к следующему вопросу

Неправильно! Повтори теорию!

Чтобы выразить неизвестную величину из уравнения Менделеева – Клапейрона, умножь левую и правую часть уравнения на знаменатель (М), получишь: рvM = mRT, найди неизвестный множитель, разделив произведение на известные множители. pv = m/MRT

4.Универсальная газовая постоянная равна: 6,022 *10 23 моль-1 1,38 * 10 – 23Дж/К 8,31 Дж/ (моль*К)

Неправильно! Повтори теорию!

Молодец! Переходи к следующему вопросу

Универсальной газовой постоянной называется произведение числа Авогадро и постоянной Больцмана: 6,02 * 1023 * 1,38 * 10 -23 k NA = R
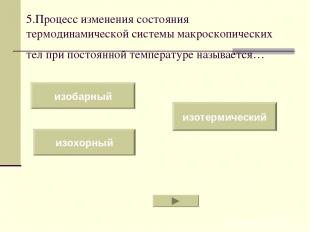
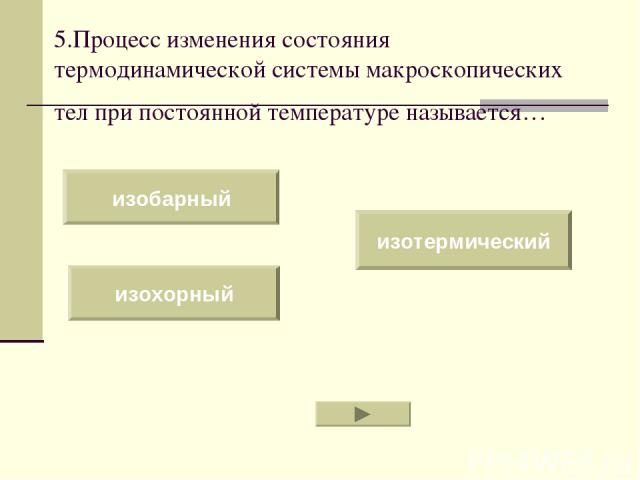
5.Процесс изменения состояния термодинамической системы макроскопических тел при постоянной температуре называется… изобарный изохорный изотермический

Согласно уравнению состояния газа в любом состоянии с неизменной температурой произведение давления газа на его объем остается постоянным. Процесс изотермический. T = const Закон Бойля-Мариотта pv = const

Молодец! Переходи к следующему вопросу

Неправильно! Повтори теорию!
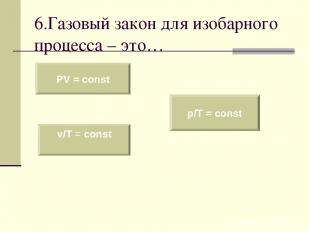
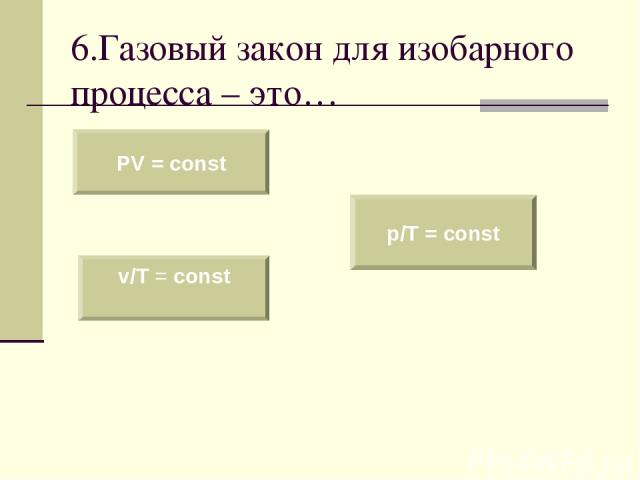
6.Газовый закон для изобарного процесса – это… PV = const v/T = const p/T = const

Неправильно! Повтори теорию!

Молодец! Переходи к следующему вопросу

Для данной массы газа отношение объема к температуре постоянно, если давление газа не меняется. v/T = const Закон Гей-Люссака. P = const
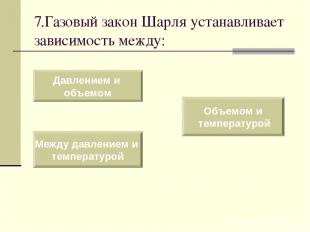
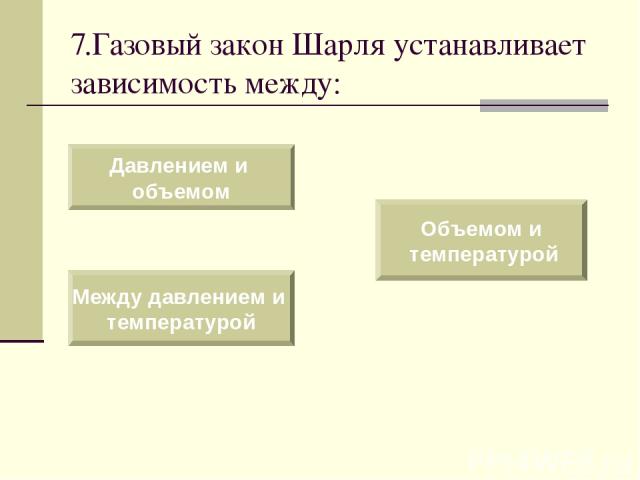
7.Газовый закон Шарля устанавливает зависимость между: Давлением и объемом Между давлением и температурой Объемом и температурой

Повтори теорию! Неправильно!
Поздравляю! Переходи к следующему вопросу

Процесс изменения состояния термодинамической системы при постоянном объеме называют изохорным. Газовый закон Шарля. V = const. p/T = const
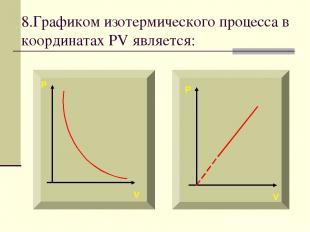
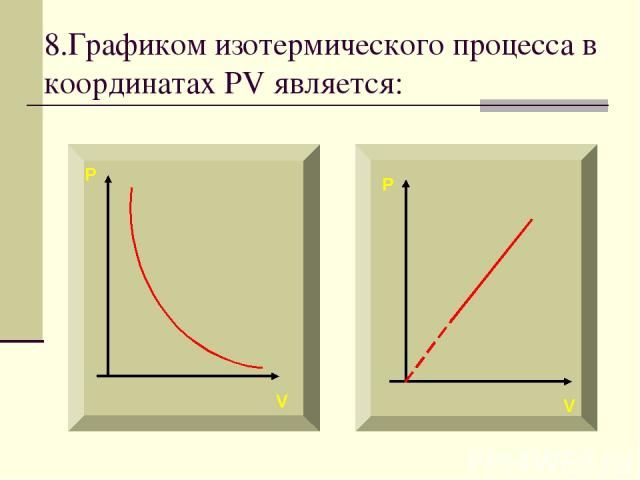
8.Графиком изотермического процесса в координатах PV является: P P V V
Поздравляю! Переходи к следующему вопросу

Неправильно! Повтори теорию!

Зависимость между давлением и объемом в изотермическом процессе обратно пропорциональная. Графиком в координатах PV является изотерма – гипербола.
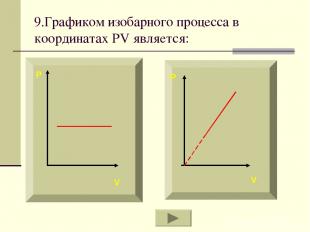
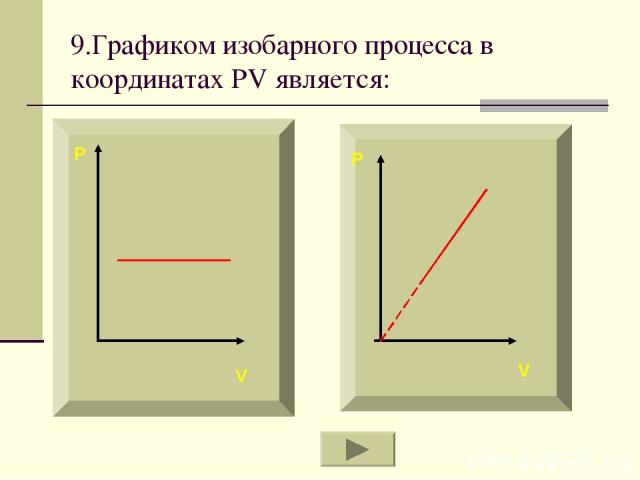
9.Графиком изобарного процесса в координатах PV является: P V P V
Поздравляю! Переходи к следующему вопросу

Неправильно! Повтори теорию!

Если процесс изобарный давление постоянно, в координатах PV график прямая линия параллельная оси объема.
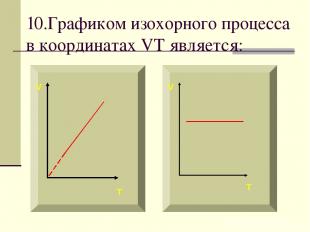
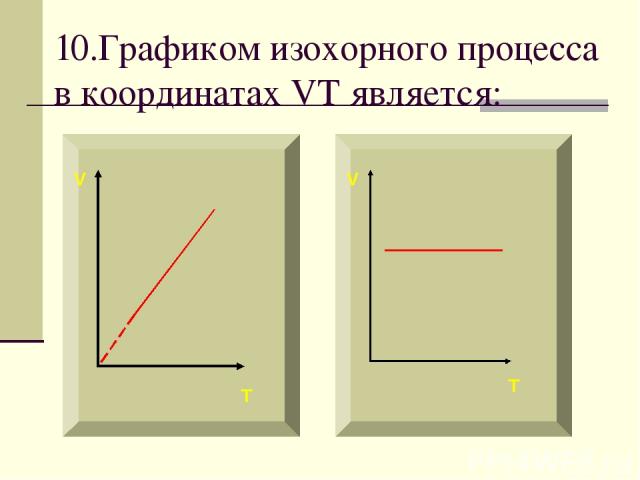
10.Графиком изохорного процесса в координатах VT является: V V T T
Поздравляю! Переходи к следующему вопросу

Неправильно! Повтори теорию!

Если процесс изохорный объем постоянный, в координатах VT график - прямая линия параллельная оси температуры.

Реши задачу: Найди давление газа бутана (С4Н8) в баллоне для портативных газовых плит объемом 0,5 л и массой 250г при температуре 20 0С 21,7 МПа 12кПа
Поздравляю! Переходи к следующей задаче

Неправильно! Посмотри решение

Решение: Переведи единицы измерения объема, массы, температуры в СИ. Найди молярную массу бутана: M=(4*12 + 1*8) * 10-3 = 56 10-3 кг/моль Из уравнения М-К вырази давление: p = mRT / VM, выполни вычисления.
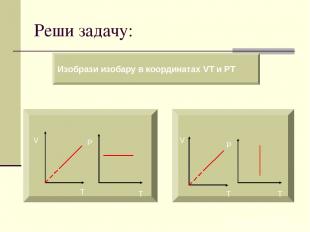
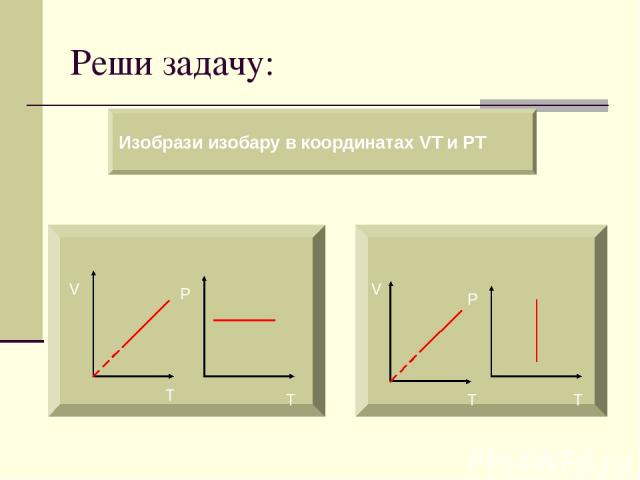
Реши задачу: Изобрази изобару в координатах VT и PT V T P T V T P T
Поздравляю! Переходи к контрольному тесту

Неправильно! Повтори теорию