Презентация на тему: Электролиз растворов и расплавов

Тема у рока: «Электролиз расплавов и растворов бескислородных солей. Окислительно – восстановительные реакции» Задачи урока: 1. рассмотреть электропроводность разных веществ с точки зрения физики и химии 2. выполнить эксперимент 3. описать процессы, сопровождающие электропроводность. ГБОУ СОШ № 2046 г. Москва 900igr.net
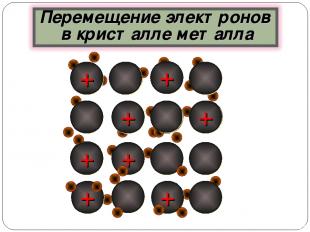
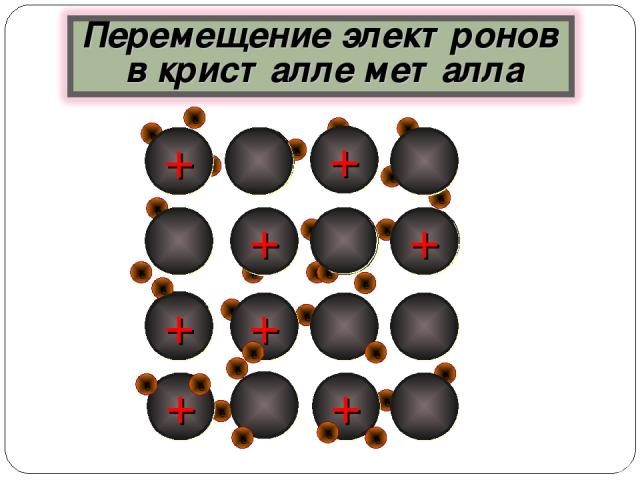
ē ē ē ē ē ē ē ē ē ē ē ē ē ē + + + + + + + + + ē ē ē ē ē ē ē ē ē ē ē ē ē ē ē ē ē ē ē ē ē + + + + + ē
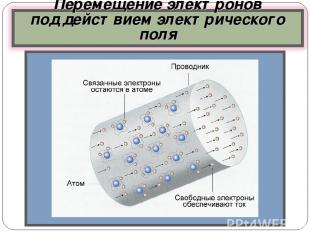

Соли, щелочи, кислоты Нерастворимые, простые, органические вещества, оксиды

Майкл Фарадей (1791 – 1867) Английский физик, ввел термины: электрод, анод – для положительного электрода катод - для отрицательного электрода ион, а так же катион и анион разделил вещества на электролиты и не электролиты. основоположник современной концепции поля в электродинамике
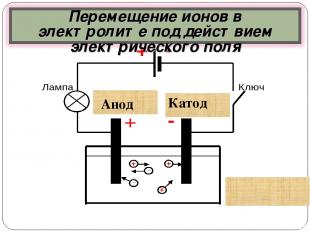
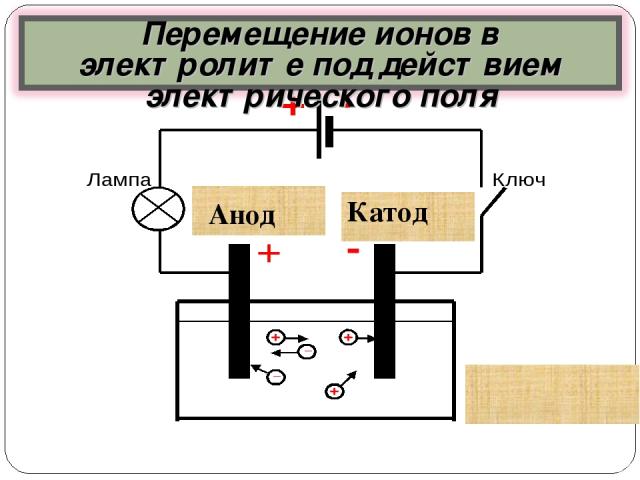
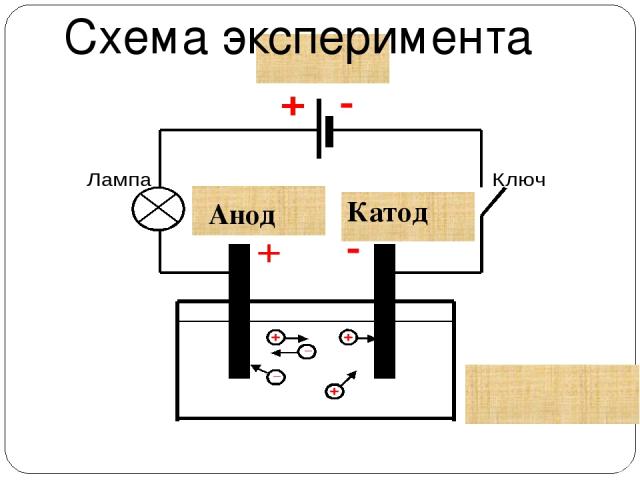
Схема эксперимента Анод Катод

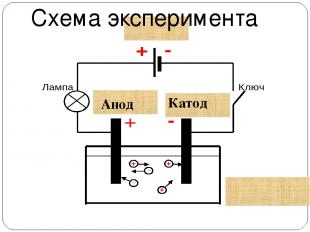
Схема эксперимента Анод Катод
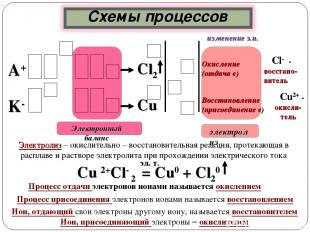
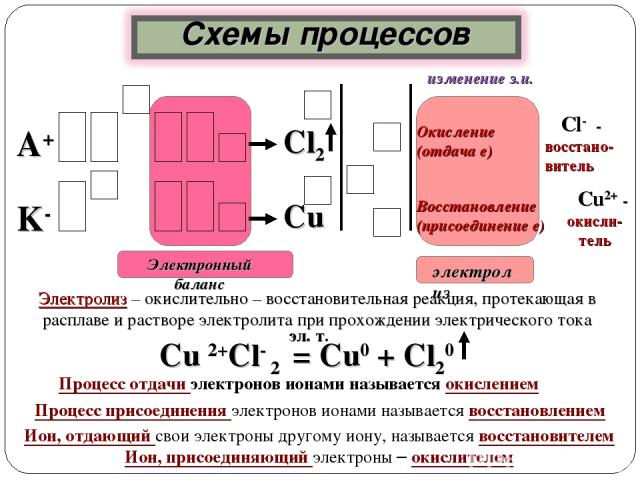
Cl- - восстано- витель Окисление (отдача е) А+ Восстановление (присоединение е) Сu2+ - окисли-тель Cu Сl2 K- Процесс отдачи электронов ионами называется окислением Процесс присоединения электронов ионами называется восстановлением Ион, отдающий свои электроны другому иону, называется восстановителем Ион, присоединяющий электроны – окислителем Электролиз – окислительно – восстановительная реакция, протекающая в расплаве и растворе электролита при прохождении электрического тока изменение з.и.

CuSO4 + Fe = Cu + FeSO4 +2 +2 +6 +6 −2 −2 0 0 Изменились степени окисления Cu и Fe Химические реакции, в результате которых происходит изменение степеней окисления атомов химических элементов или зарядов ионов, образующих реагирующие вещества, называют окислительно-восстановительными процессами (реакциями) (ОВР).


Домашнее задание: Учебник химии: п. 42, упр. 1,3 (с. 109) Задание в тетради по физике (расчетные задачи)

Информационная поддержка и методическая основа разработки урока: Единая коллекция цифровых образовательных ресурсов ГИС «Интернет» – интерактивные задания «Уравнения процессов, происходящих при электролизе» - №1,2 к учебнику Ивановой Р. Г. ООО «Телекомпания СГУ ТВ Современная гуманитарная академия», Видеоиллюстрация. Химия. Электролиз. Часть 5 - видеосюжет «Электролиз воды» Картинки и схемы для слайд - презентации - поисковая система и интернет-портал «Яндекс» картинки Габриелян О.С. Химия. 8 класс : учеб. для общеобразоват. учреждений / О.С. Габриелян. - 11-е изд., испр. - М. : Дрофа, 2005. - 267 с. : ил.