Презентация на тему: Электрический ток в жидкостях

Электрический ток в жидкостях Урок изучения и первичного закрепления знаний

Цели урока Формирование и закрепление знаний об особенностях электропроводности электролитов.Изучение процесса электролиза и его технического примененияФормирование научного мировоззрения и навыков исследовательской деятельностиДемонстрация связи науки и практикиФормирование умений использования сети Интернет для поиска информации и совершенствования знанийВоспитание творческого мышления, учебно-познавательной активности, умений сотрудничать в коллективе

Методы урока Проблемно-диалогический с применением информационно-коммуникационных технологий, элементов мозгового штурма, демонстрационных опытов и составление опорного конспекта

Межпредметная связь Химия - электролитическая диссоциация, электролиз. Математика - построение графиков, преобразование формул, расчёты.

Структура урока Организационный моментАктуализация знаний. Мозговой штурмМотивация. Демонстрационный опыт Постановка проблемыПобуждающий диалог. Поиск и решение проблемыДемонстрационный эксперимент. Интеграция в область химии. Подводящий диалогСистематизация и обобщение знанийПоиск информации в сети ИнтернетЗакрепление знанийДомашнее задание

Ответьте на вопросы: На какие группы делят все вещества по проводимости электрического тока?Приведите примеры самых лучших проводников электрического тока.Какими частицами обусловлен ток в металлах?Изменится ли электропроводность металла, если его нагреть? Изменится ли электропроводность металла, если его расплавить?Какие вам известны жидкости, проводящие электрический ток, кроме расплавленных металлов?
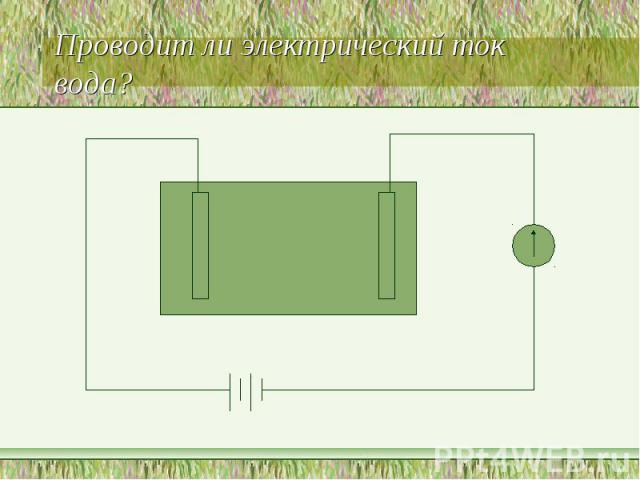
Проводит ли электрический ток вода?
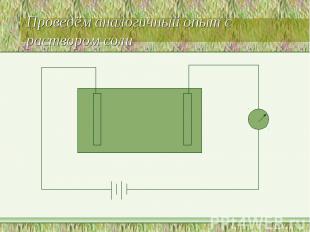
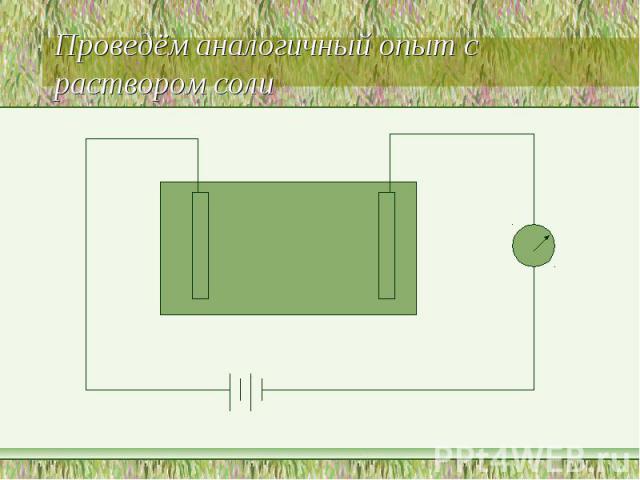
Проведём аналогичный опыт с раствором соли
Почему чистая вода не проводит, а раствор соли проводит электрический ток?Чем обусловлен электрический ток в растворе соли?
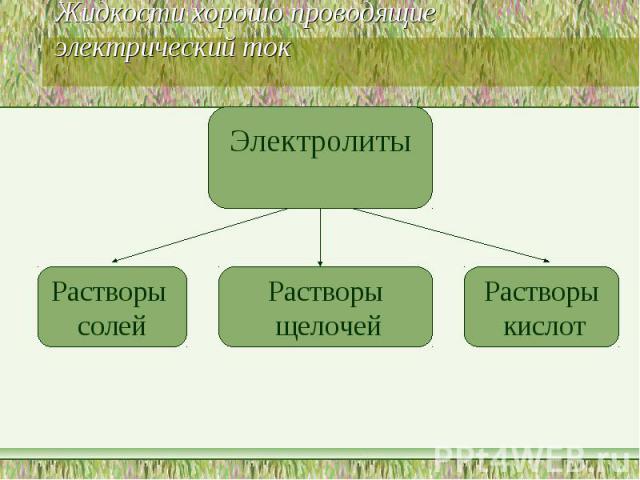
Жидкости хорошо проводящие электрический ток

При опускании в раствор хлорида меди CuCl2 разноимённо заряжённых электродов возникает направленное движение ионов. Хлорид меди в водном растворе диссоциирует на ионы меди и хлора: CuCl2 — Cu2+ + 2Cl-

Электролитическая диссоциация - расщепление молекул на положительные и отрицательные ионы под действием растворителя. При сближении ионов разных знаков возможна их рекомбинация (объединение) в одну молекулу

При прохождении электрического тока через электролит происходит перенос вещества

Процесс выделения на электродах веществ, входящих в состав электролита, при протекании через его раствор (или расплав) электрического тока, называют электролизом Электролиз имеет широкое техническое применение.Где применяют электролиз?На этот вопрос надо подготовить ответ, используя Интернет.

От чего зависит масса, выделенного на электроде вещества? Масса вещества m, выделившегося на электроде за время t при прохождении электрического тока, пропорциональна силе тока I и времени tk -электрохимический эквивалент вещества

Майкл Фарадей - великий английский учёный, творец общего учения об электромагнитных явлениях Майкл Фарадей в 1833 году экспериментально установил закон электролиза. Им были введены общепринятые теперь термины: электрод, катод, анод, электролит, электролиз.

Выполните тест I. Укажите неверный ответ 1. Жидкости могут быть диэлектриками, проводниками, полупроводниками. 2. Все жидкости являются электролитами. 3. Растворы солей, щелочей, кислот и расплавленные соли, обладающие электрической проводимостью, называются электролитами. II. Электролитической диссоциацией называется ...III. Рекомбинацией называется …IV. Электролизом называется … 1. процесс выделения на электродах веществ, входящих в состав электролита. 2. объединение ионов разных знаков в нейтральные молекулы. 3. образование положительных и отрицательных ионов при растворении веществ в жидкости.V. С увеличением температуры электролита его электропроводность … 1. увеличивается. 2. уменьшается. 3. не изменяется.