Презентация на тему: Проблемы выбора лекарственных средств

ПРОБЛЕМЫ ВЫБОРА ЛЕКАРСТВЕННЫХ СРЕДСТВ (ОРИГИНАЛЬНЫЕ И ВОСПРОИЗВЕДЕННЫЕ ПРЕПАРАТЫ) Б.В. АндреевСанкт-Петербургский государственный университетСанкт-Петербургская психиатрическая больница №1 им.П.П. Кащенко

www.rspor.ru ► МОО «Общество фармакоэкономический исследований» Стандарты оказания медицинской помощи (КЭС): база данных всех стандартов медицинской помощи, утвержденных Министерством здравоохранения и социального развития РФ в период с 2004 по 2007 годы Стандарты (Протоколы ведения больных): база данных всех протоколов ведения больных, утвержденных Министерством здравоохранения и социального развития РФ в период с 2002 по 2007 годы. Некоторые версии протоколов ведения больных не являются окончательными – возможны незначительные изменения, которые в данный момент исправляются.

Стандарт 1. Модель пациента Категория возрастная:Нозологическая форма: Код по МКБ-10:Фаза:Стадия:Осложнение:Условие оказания:

Стандарт 1.1. Лечение из расчета … днейА. Стандартизированный объем обследования пациента Б. Стандартизированный объем немеди- каментозного лечения В. Стандартизированный объем сестрин- ской помощиГ. Стандартизированный объем медикаментозного лечения

Стандартизированный объем медикаментозного лечения Фармакотерапевтическая группаМННЧастота назначенияОДД - ориентировочная дневная дозаЭКД - эквивалентная курсовая доза Стоимость курсовая (руб)Проблема выбора ЛС в рамках финансового обеспечения ЛПУ В идеале – соответствие формуляру

ПРОТОКОЛ Область примененияНормативные ссылки (например, постановления Правительства РФ..)Общие положения (решение определенных задач, в том числе, определение алгоритмов диагностики и фармакотерапии конкретного заболевания)План обследования больногоПринципы рационального ведения больныхПринципы медикаментозной терапии

Оригинальный препарат - впервые синтезированное, прошедшее полный цикл доклинических и клинических исследований лекарственное средство, защищённое патентом на срок до 20 летТолько по истечении срока действия патента возможно воспроизведение ЛС любой компанией: создаётся генерик

Evidence-based medicine «медицина, основанная на доказательствах» Согласно этой концепции наиболее ценным источником информации являются крупномасштабные рандомизированные слепые контролируемые исследования (РКИ)Результаты РКИ определенного лекарственного препарата нельзя переносить на «аналоговые» препараты

Генерик: ЛС, обладающего доказанной терапевти-ческой взаимозаменяемостью с оригинальным ЛС аналогичного состава, выпускаемый иным, нежели разработчик оригинального, производителем без лицензии разработчика.Допускается в обращение после истечения срока патентной защиты оригинального ЛС на основании регистрационного досье сокращенного объема.
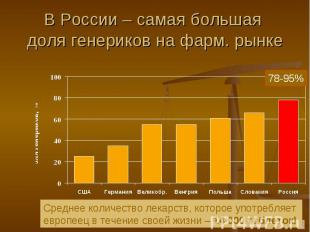
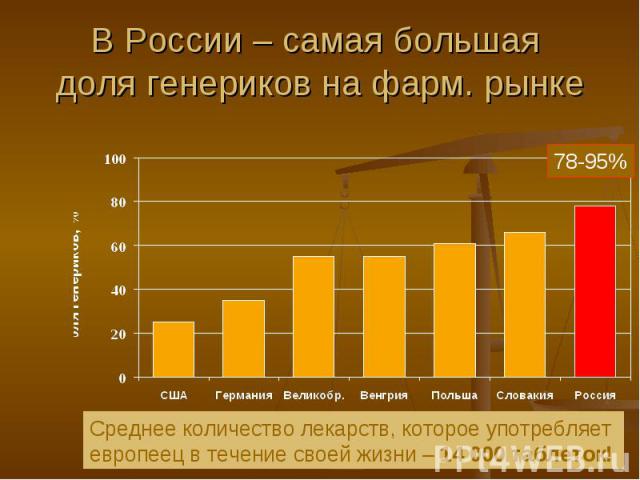
В России – самая большая доля генериков на фарм. рынке Среднее количество лекарств, которое употребляет европеец в течение своей жизни – 14 000 таблеток!

Эналаприл: оригинал и 33 копии*

ФАРМАКОЭПИДЕМИОЛОГИЧЕСКИЕ ПОКАЗАТЕЛИ “Критерии для ЛП (для торговых наименований)”:1. является ли ЛП оригинальным лекарством;2. является ли ЛП супердженериком, то есть ЛП имеющем лицензию на производство от разработчика оригинального ЛП;3. является ли ЛП дженериком, которое на международном рынке ЛП более 3 лет;4. обладает ли генерик данными по биоэквивалентности; 5. обладает ли генерик данными по терапевтической эквивалентности;6. производятся ли генерик по требованиям GMP; 7. обладает ли ЛП “стационарными” формами выпуска (наибольшее количество таблеток, капсул, ампул, флаконов и тд);8. является ли торговая марка ЛП наиболее широко используемой в ЛПУ города (более 70% ЛПУ заказывают именно эту торговую форм).

Преимущества качественных (добросовестных) генериков Сравнительно небольшая стоимость при высоком качестве и хорошем терапевтическом эффекте Прошли исследования на эквивалентностьС 1 января 2007 года в года в РФ обязательная сертификация ЛС заменена декларированием соответствия

Виды эквивалентности Фармацевтическая эквивалентность -равное количество (отличия не более чем на 5%) действующего начала и соответствуют стандартам производства. Максимальная ФЭ при использовании GMP Биоэквивалентность (фармакокинетическая) – идентичность оригинального и воспроизведенного ЛС по основным фармакокинетическим параметрам. Изучается in vivo. Терапевтическая эквивалентность ( позиционируется при биоэквивалентности, НО НЕ ИЗУЧАЕТСЯ)

ФАРМАЦЕВТИЧЕСКАЯ ЭКВИВАЛЕНТНОСТЬ Какие-либо исследования чрезвычайно редкиАктивные лекарственные субстанции, нередко закупаются в странах, мало доступных для действенного контроля (Китай, Индия, Вьетнам и т.д.) Качество этих субстанций в силу несовершенных методов синтеза невысокое (примеси, продукты деградации и т.д.). Производство вспомогательных веществ (наполнителей) также может производиться с определенными нарушениями

Качество наполнителей имеет значение! Любое изменение в составе вспомогательных веществ или оболочки могут существенно изменить качество препарата, его биодоступность, привести к токсическим или аллергическим явлениям

Оценка состава генерика затруднена! Фармакопейные статьи не отражают тонкостей в изменении синтезаХимико-аналитическая экспертиза субстанции, необходимая для выявления технологических примесей, при регистрации генериков в РФ не проводится

Биоэквивалентность: Реальность РФ Если генерик разрешен к применению в других странах, он регистрируется в РФ по упрощенной схеме (без определения биоэквивалентности) Только генерики новых производителей исследуются на биоэквивалентность Из 1256 зарегистрированных в 2001 г. зарубежных препаратов только 22 прошли экспертизу на биоэквивалентность при регистрации в РФ

КАК ОПРЕДЕЛЯЕТСЯ БИОЭКВИВАЛЕНТНОСТЬ Проводится на небольших гомогенных группах здоровых некурящих испытуемых, мужского пола в возрасте 18 - 55 лет, не получающих каких-либо медикаментозных средств, обладающих нормальным ростом и весом, придерживающихся стабильной диеты Генерик и оригинальный препарат назначается в течение одного дня в одной и той же суточной дозе Если концентрация генерика укладывается в пределы от -20%, до +25% брендового препарата, то считается, что биоэквивалентность подтверждена

Критерии биоэквивалентности для РФ
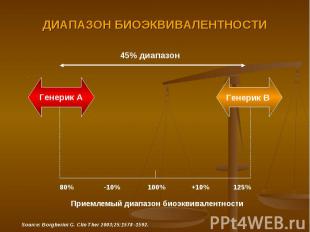
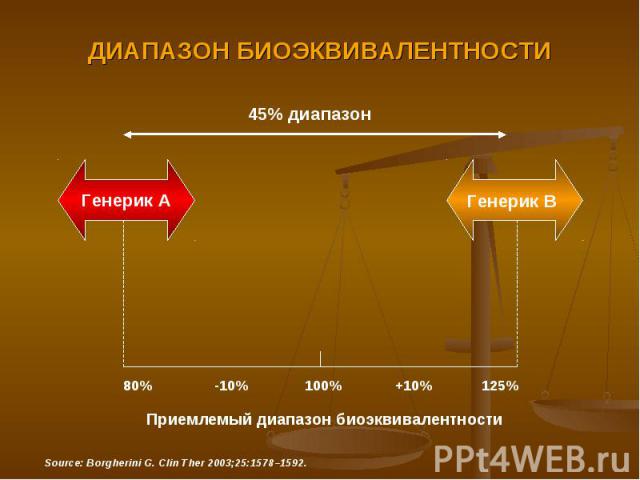
ДИАПАЗОН БИОЭКВИВАЛЕНТНОСТИ

КАК ЧАСТО НАРУШАЕТСЯ БИОЭКВИВАЛЕНТНОСТЬ? Проведенный в Великобритании в 1995-1996 анализ 2427 воспроизведенных ЛС обнаружил 228 существенных отличий. Причем в 84 случаях пришлось провести качественное улучшение препаратов. Ведущее ведомство США, контролирующее качество пищевых продуктов и лекарственных препаратов (Food and Drug Administration) в конце 80-х признало, что до 20% имеющихся там брендовых и дженериковых препаратов не являются биоэквивалентными, и соответственно не могут подменять друг друга

Как решается проблема генериков в развитых странах ? Отрицательное отношение к биоэквивалентности как к единственному способу оценки равнозначности лекарствОбязательность клинических испытаний по правилам GCPКлассификация генериков: коды "А" и "В"

Как решается проблема генериков в развитых странах ? В США присваивается код «А» генерикам, прошедшим клинические испытания на терапевтическую эквивалентность и имеющий отличия фармакокинетики от оригинального препарата на 3-4%На генерики с кодом «А» можно экстраполировать данные исследований оригинального препаратаГенерики с кодом «А» могут являться заменой оригинальному препарату по финансовым соображениям

Как решается проблема генериков в развитых странах ? В США присваивается код «В» генерикам, не прошедшим клинические испытания на терапевтическую эквивалентностьГенерик с кодом «В» не может быть автоматической заменой оригинальному препарату или другому генерику с кодом «А»

Результаты отсутствия исследований терапевтической эквивалентности Биоэквивалентные Ренитеку генерики значительно отличаются от него по терапевтической эффективности

Требования к сравнительным исследованиям: независимоемногоцентровоерандомизированноеконтролируемоедлительное (ср. продолжительность приема)с жесткими конечными точкамиВыполнены только для единичных генериков, применяемых в РФ

СХОДСТВО ПАКСИЛА И РЕКСЕТИНА (фармакологическое действие) Паксил генерализованное тревожное расстройство (эффективность препарата сохраняется при длительном лечении этого расстройства)Рексетин

СХОДСТВО ПАКСИЛА И РЕКСЕТИНА (побочные действия) Паксил Судороги в структуре серотонинового синдрома-РексетинЭпилептиформные припадкиПовышение внутричерепного давления

Что делать ? Создавать информационную базу для закупок КАЧЕСТВЕННЫХ препаратов: оригиналов и генериков!Доказательная медицинская база (РКИ)Фармакоэкономическая и фармакоэпидемиологическая экспертизаКонтроль качества по международным стандартам (доступный для экспертной оценки)