Презентация на тему: Препараты

ПРОБЛЕМЫ ВЫБОРА ЛЕКАРСТВЕННЫХ СРЕДСТВ (ОРИГИНАЛЬНЫЕ И ВОСПРОИЗВЕДЕННЫЕ ПРЕПАРАТЫ) Б.В. Андреев Санкт-Петербургский государственный университет Санкт-Петербургская психиатрическая больница №1 им.П.П. Кащенко 900igr.net

www.rspor.ru ► МОО «Общество фармакоэкономический исследований» Стандарты оказания медицинской помощи (КЭС): база данных всех стандартов медицинской помощи, утвержденных Министерством здравоохранения и социального развития РФ в период с 2004 по 2007 годы Стандарты (Протоколы ведения больных): база данных всех протоколов ведения больных, утвержденных Министерством здравоохранения и социального развития РФ в период с 2002 по 2007 годы. Некоторые версии протоколов ведения больных не являются окончательными – возможны незначительные изменения, которые в данный момент исправляются.

Стандарт 1. Модель пациента Категория возрастная: Нозологическая форма: Код по МКБ-10: Фаза: Стадия: Осложнение: Условие оказания:

Стандарт 1.1. Лечение из расчета … дней А. Стандартизированный объем обследования пациента Б. Стандартизированный объем немеди- каментозного лечения В. Стандартизированный объем сестрин- ской помощи Г. Стандартизированный объем медикаментозного лечения

Стандартизированный объем медикаментозного лечения Фармакотерапевтическая группа МНН Частота назначения ОДД - ориентировочная дневная доза ЭКД - эквивалентная курсовая доза Стоимость курсовая (руб) Проблема выбора ЛС в рамках финансового обеспечения ЛПУ В идеале – соответствие формуляру

ПРОТОКОЛ Область применения Нормативные ссылки (например, постановления Правительства РФ..) Общие положения (решение определенных задач, в том числе, определение алгоритмов диагностики и фармакотерапии конкретного заболевания) План обследования больного Принципы рационального ведения больных Принципы медикаментозной терапии

впервые синтезированное, прошедшее полный цикл доклинических и клинических исследований лекарственное средство, защищённое патентом на срок до 20 лет Только по истечении срока действия патента возможно воспроизведение ЛС любой компанией: создаётся генерик Оригинальный препарат -

Evidence-based medicine «медицина, основанная на доказательствах» Согласно этой концепции наиболее ценным источником информации являются крупномасштабные рандомизированные слепые контролируемые исследования (РКИ) Результаты РКИ определенного лекарственного препарата нельзя переносить на «аналоговые» препараты

Генерик: ЛС, обладающего доказанной терапевти-ческой взаимозаменяемостью с оригинальным ЛС аналогичного состава, выпускаемый иным, нежели разработчик оригинального, производителем без лицензии разработчика. Допускается в обращение после истечения срока патентной защиты оригинального ЛС на основании регистрационного досье сокращенного объема.
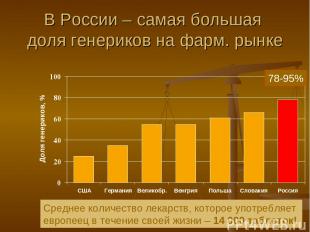
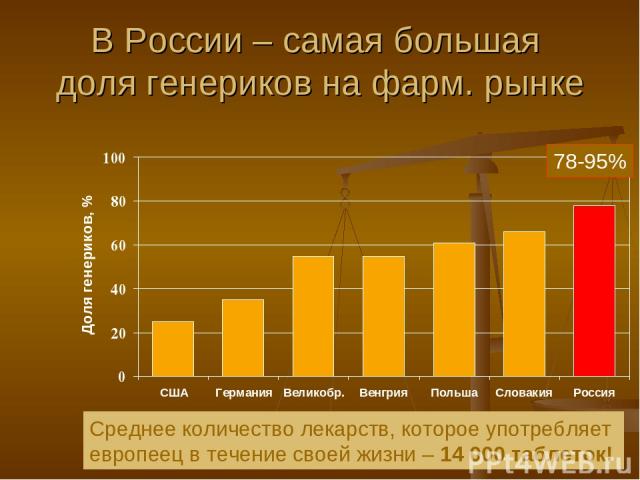
В России – самая большая доля генериков на фарм. рынке 78-95% Среднее количество лекарств, которое употребляет европеец в течение своей жизни – 14 000 таблеток!

Эналаприл: оригинал и 33 копии* Оригинал Генерики Багоприл Берлиприл Вазопрен Веро-Эналаприл Инворил Кальпирен Миниприл Миоприл Нормапресс Рениприл Эднит Эназил Эналакор Эналаприл Эналаприл-ICN Эналаприл- Аджио Эналаприл-АКОС Эналаприл-Акри Эналаприл-Гексал Эналаприл-Н.С Эналаприл-Рос Эналаприл-ФПО Эналаприла малеат Энам Энан-ЛМ Энап Энаприл Энаренал Энафарм Энвас Энвиприл Энприл Энрил * - Справочник синонимов лекарственных средств. М., 2005, с. 308-309

“Критерии для ЛП (для торговых наименований)”: 1. является ли ЛП оригинальным лекарством; 2. является ли ЛП супердженериком, то есть ЛП имеющем лицензию на производство от разработчика оригинального ЛП; 3. является ли ЛП дженериком, которое на международном рынке ЛП более 3 лет; 4. обладает ли генерик данными по биоэквивалентности; 5. обладает ли генерик данными по терапевтической эквивалентности; 6. производятся ли генерик по требованиям GMP; 7. обладает ли ЛП “стационарными” формами выпуска (наибольшее количество таблеток, капсул, ампул, флаконов и тд); 8. является ли торговая марка ЛП наиболее широко используемой в ЛПУ города (более 70% ЛПУ заказывают именно эту торговую форм). ФАРМАКОЭПИДЕМИОЛОГИЧЕСКИЕ ПОКАЗАТЕЛИ

Преимущества качественных (добросовестных) генериков Сравнительно небольшая стоимость при высоком качестве и хорошем терапевтическом эффекте Прошли исследования на эквивалентность С 1 января 2007 года в года в РФ обязательная сертификация ЛС заменена декларированием соответствия

Виды эквивалентности Фармацевтическая эквивалентность -равное количество (отличия не более чем на 5%) действующего начала и соответствуют стандартам производства. Максимальная ФЭ при использовании GMP Биоэквивалентность (фармакокинетическая) – идентичность оригинального и воспроизведенного ЛС по основным фармакокинетическим параметрам. Изучается in vivo. Терапевтическая эквивалентность ( позиционируется при биоэквивалентности, НО НЕ ИЗУЧАЕТСЯ)

Какие-либо исследования чрезвычайно редки Активные лекарственные субстанции, нередко закупаются в странах, мало доступных для действенного контроля (Китай, Индия, Вьетнам и т.д.) Качество этих субстанций в силу несовершенных методов синтеза невысокое (примеси, продукты деградации и т.д.). Производство вспомогательных веществ (наполнителей) также может производиться с определенными нарушениями ФАРМАЦЕВТИЧЕСКАЯ ЭКВИВАЛЕНТНОСТЬ Белоусов Ю.Б. Дженерики - мифы и реалии Remedium. www.pliva.ru/content/files/library/170.doc 26.07.2004.

Качество наполнителей имеет значение! Любое изменение в составе вспомогательных веществ или оболочки могут существенно изменить качество препарата, его биодоступность, привести к токсическим или аллергическим явлениям

Оценка состава генерика затруднена! Фармакопейные статьи не отражают тонкостей в изменении синтеза Химико-аналитическая экспертиза субстанции, необходимая для выявления технологических примесей, при регистрации генериков в РФ не проводится

Биоэквивалентность: Реальность РФ Если генерик разрешен к применению в других странах, он регистрируется в РФ по упрощенной схеме (без определения биоэквивалентности) Только генерики новых производителей исследуются на биоэквивалентность Из 1256 зарегистрированных в 2001 г. зарубежных препаратов только 22 прошли экспертизу на биоэквивалентность при регистрации в РФ

КАК ОПРЕДЕЛЯЕТСЯ БИОЭКВИВАЛЕНТНОСТЬ Проводится на небольших гомогенных группах здоровых некурящих испытуемых, мужского пола в возрасте 18 - 55 лет, не получающих каких-либо медикаментозных средств, обладающих нормальным ростом и весом, придерживающихся стабильной диеты Генерик и оригинальный препарат назначается в течение одного дня в одной и той же суточной дозе Если концентрация генерика укладывается в пределы от -20%, до +25% брендового препарата, то считается, что биоэквивалентность подтверждена Meyer MC. Generic drug product equivalence: Current status. Am J Manag Care. 1998;4:1183-1189.
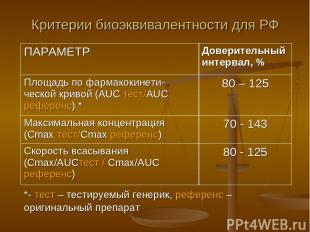
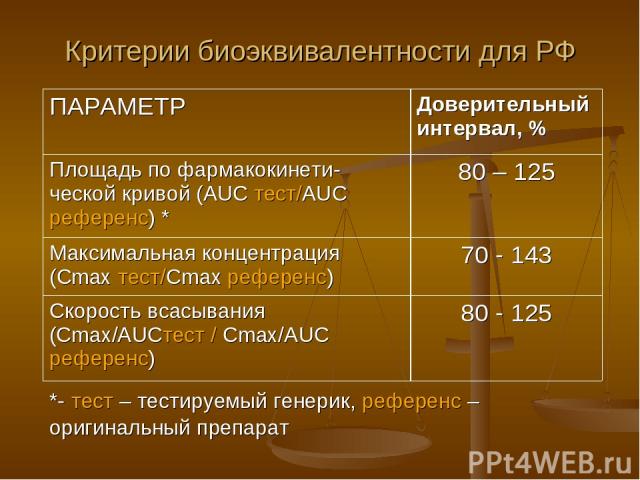
Критерии биоэквивалентности для РФ ПАРАМЕТР Доверительный интервал, % Площадь по фармакокинети-ческой кривой (AUС тест/AUС референс) * 80 – 125 Максимальная концентрация (Сmax тест/Cmax референс) 70 - 143 Скорость всасывания (Cmax/AUСтест / Сmax/AUС референс) 80 - 125 *- тест – тестируемый генерик, референс – оригинальный препарат
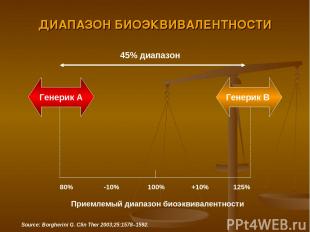
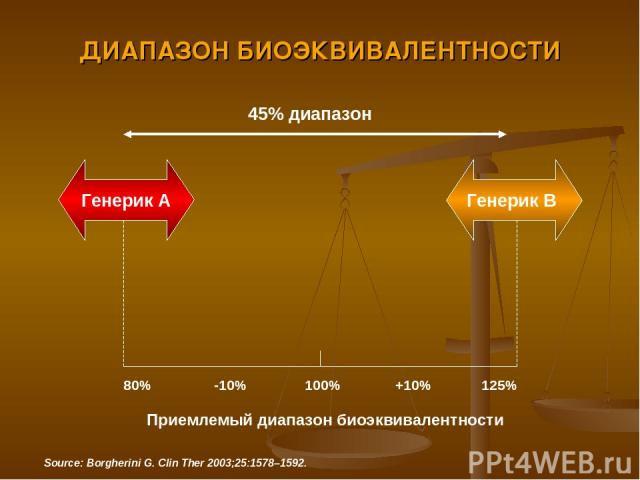
ДИАПАЗОН БИОЭКВИВАЛЕНТНОСТИ 45% диапазон Генерик А Генерик В 80% -10% 100% +10% 125% Приемлемый диапазон биоэквивалентности Source: Borgherini G. Clin Ther 2003;25:1578–1592.

Проведенный в Великобритании в 1995-1996 анализ 2427 воспроизведенных ЛС обнаружил 228 существенных отличий. Причем в 84 случаях пришлось провести качественное улучшение препаратов. Ведущее ведомство США, контролирующее качество пищевых продуктов и лекарственных препаратов (Food and Drug Administration) в конце 80-х признало, что до 20% имеющихся там брендовых и дженериковых препаратов не являются биоэквивалентными, и соответственно не могут подменять друг друга КАК ЧАСТО НАРУШАЕТСЯ БИОЭКВИВАЛЕНТНОСТЬ? Generic medicines—can quality be assured? Drug Ther Bull. 1997; 35:9-11 Nightingale SL, Morrison JC, Generic drugs and the prescribing physician JAMA. 1987;258:1200-1204..

Как решается проблема генериков в развитых странах ? Отрицательное отношение к биоэквивалентности как к единственному способу оценки равнозначности лекарств Обязательность клинических испытаний по правилам GCP Классификация генериков: коды "А" и "В"

Как решается проблема генериков в развитых странах ? В США присваивается код «А» генерикам, прошедшим клинические испытания на терапевтическую эквивалентность и имеющий отличия фармакокинетики от оригинального препарата на 3-4% На генерики с кодом «А» можно экстраполировать данные исследований оригинального препарата Генерики с кодом «А» могут являться заменой оригинальному препарату по финансовым соображениям

Как решается проблема генериков в развитых странах ? В США присваивается код «В» генерикам, не прошедшим клинические испытания на терапевтическую эквивалентность Генерик с кодом «В» не может быть автоматической заменой оригинальному препарату или другому генерику с кодом «А»

Результаты отсутствия исследований терапевтической эквивалентности Биоэквивалентные Ренитеку генерики значительно отличаются от него по терапевтической эффективности Ю.Б. Белоусов; Ремедиум, июль-август, 2003 Препарат Ср. доза для достижения Целевого АД Ренитек 12 мг Энап 15 мг Эднит 15,6 мг Инворил 20,6 мг Энам 36,6 мг

Требования к сравнительным исследованиям: независимое многоцентровое рандомизированное контролируемое длительное (ср. продолжительность приема) с жесткими конечными точками Выполнены только для единичных генериков, применяемых в РФ

Паксил Рексетин СХОДСТВО ПАКСИЛА И РЕКСЕТИНА (фармакологическое действие) генерализованное тревожное расстройство (эффективность препарата сохраняется при длительном лечении этого расстройства) - www.vidal.ru

Паксил Рексетин СХОДСТВО ПАКСИЛА И РЕКСЕТИНА (побочные действия) Эпилептиформные припадки Повышение внутричерепного давления Судороги в структуре серотонинового синдрома - www.vidal.ru

Что делать ? Создавать информационную базу для закупок КАЧЕСТВЕННЫХ препаратов: оригиналов и генериков! Доказательная медицинская база (РКИ) Фармакоэкономическая и фармакоэпидемиологическая экспертиза Контроль качества по международным стандартам (доступный для экспертной оценки)