Презентация на тему: Наследственная патология. Моногенные синдромы

Наследственная патология Моногенные синдромы

Классификация моногенных синдромов Так как проявление моногенных болезней зависит от природы мутантного гена, существует их классификация в зависимости от типа наследования. Выделяют аутосомно-доминантные, аутосомно-рецессивные, а также Х-сцепленные моногенные синдромы.

Аутосомно-доминантный тип наследования характеризуется следующими признаками: больные имеются в каждом поколении; больной ребенок у больных родителей; болеют в равной степени мужчины и женщины; проявление признака (болезни) наблюдается по вертикали и по горизонтали; вероятность наследования 100% (если хотя бы один родитель гомозиготен), 75% (если оба родителя гетерозиготны) и 50% (если один родитель гетерозиготен).
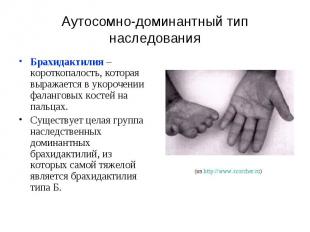
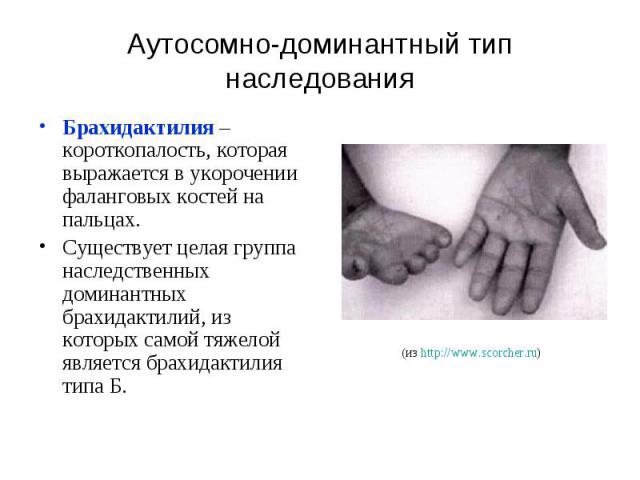
Аутосомно-доминантный тип наследования Брахидактилия – короткопалость, которая выражается в укорочении фаланговых костей на пальцах. Существует целая группа наследственных доминантных брахидактилий, из которых самой тяжелой является брахидактилия типа Б.

Брахидактилия Причиной заболевания являются гетерозиготные мутации в гене тирозин-киназного рецептора ROR2. Установлено, что этот ген экспрессируется в остеобластах и хондроцитах, принимая участие в их размножении, созревании и дифференцировке. Ген ROR2 локализован в хромосоме 9, в районе 9q22, состоит из 9 экзонов.
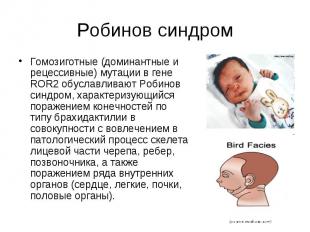
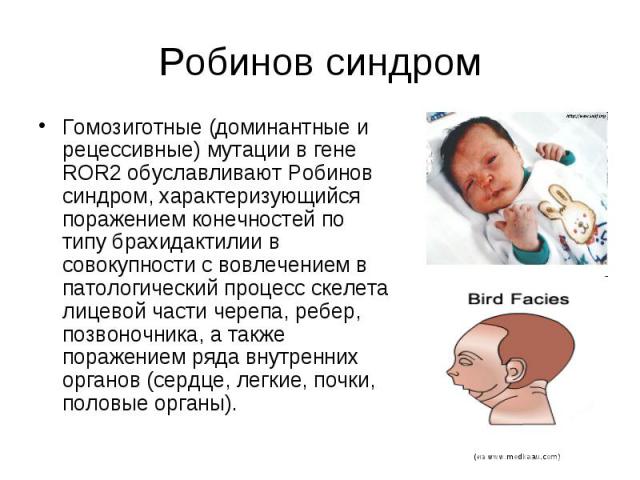
Робинов синдром Гомозиготные (доминантные и рецессивные) мутации в гене ROR2 обуславливают Робинов синдром, характеризующийся поражением конечностей по типу брахидактилии в совокупности с вовлечением в патологический процесс скелета лицевой части черепа, ребер, позвоночника, а также поражением ряда внутренних органов (сердце, легкие, почки, половые органы).
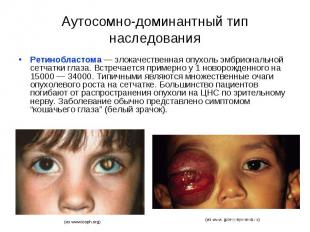
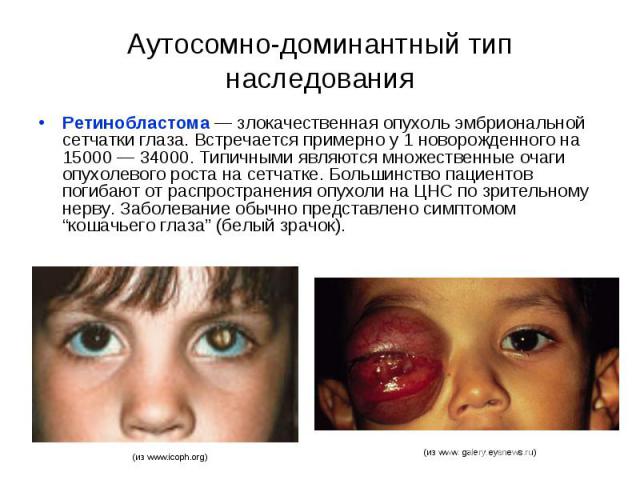
Аутосомно-доминантный тип наследования Ретинобластома — злокачественная опухоль эмбриональной сетчатки глаза. Встречается примерно у 1 новорожденного на 15000 — 34000. Типичными являются множественные очаги опухолевого роста на сетчатке. Большинство пациентов погибают от распространения опухоли на ЦНС по зрительному нерву. Заболевание обычно представлено симптомом “кошачьего глаза” (белый зрачок).

Ретинобластома если ребёнок наследует мутантный аллель гена Rb, то вторая мутация, происходящая уже в ретинобласте, ведёт к образованию опухоли. Локус RB1 расположен на хромосоме 13q и занимает около 200000 п.н. Цитогенетические методы показали, что многие случаи наследственных и спорадических форм ретинобластмы сопровождаются делецией в участке 13q14
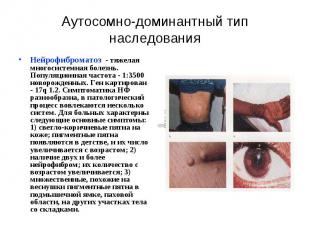
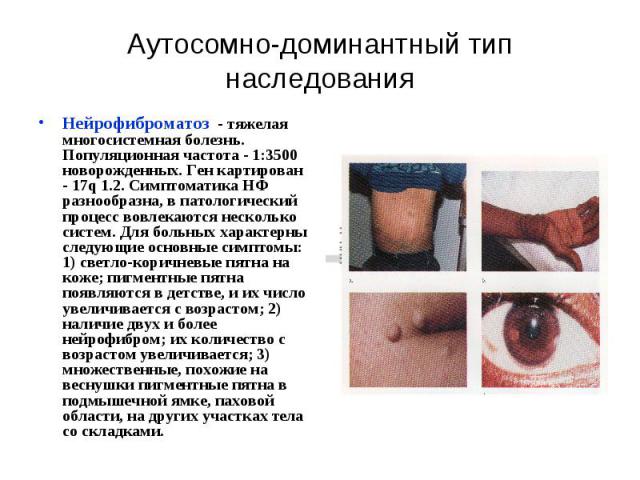
Аутосомно-доминантный тип наследования Нейрофиброматоз - тяжелая многосистемная болезнь. Популяционная частота - 1:3500 новорожденных. Ген картирован - 17q 1.2. Симптоматика НФ разнообразна, в патологический процесс вовлекаются несколько систем. Для больных характерны следующие основные симптомы: 1) светло-коричневые пятна на коже; пигментные пятна появляются в детстве, и их число увеличивается с возрастом; 2) наличие двух и более нейрофибром; их количество с возрастом увеличивается; 3) множественные, похожие на веснушки пигментные пятна в подмышечной ямке, паховой области, на других участках тела со складками.

Нейрофиброматоз Чаще наблюдается нейрофиброматоз I типа (болезнь Реклингаузена). В этом случае имеются доминантные мутации в гене NF1 (17q11.2), кодирующем белок нейрофибромин. Этот белок контролирует активность белков Ras, которые в свою очередь регулируют различные аспекты клеточной пролиферации, дифференцировки и морфологии. Ras являются протоонкогенами и их постоянная активация ведет к злокачественному перерождению клеток .
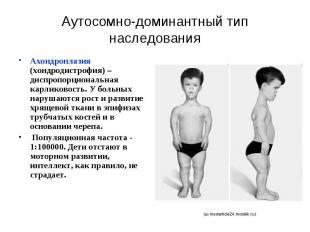
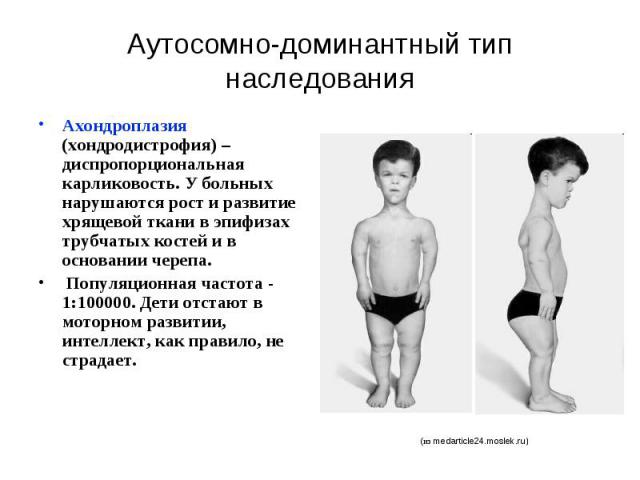
Аутосомно-доминантный тип наследования Ахондроплазия (хондродистрофия) – диспропорциональная карликовость. У больных нарушаются рост и развитие хрящевой ткани в эпифизах трубчатых костей и в основании черепа. Популяционная частота - 1:100000. Дети отстают в моторном развитии, интеллект, как правило, не страдает.

Ахондроплазия ахондроплазия вызывается мутацией в гене, кодирующем белок FGFR3 (рецептор 3 к фактору роста фибробластов). При этой точечной мутации происходит замена: вместо глицина в 380 положении у белка FGFR3 находится аргинин. В норме белок FGFR3 участвует в процессе остеогенеза.
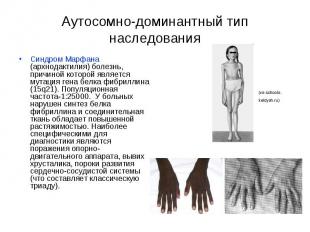
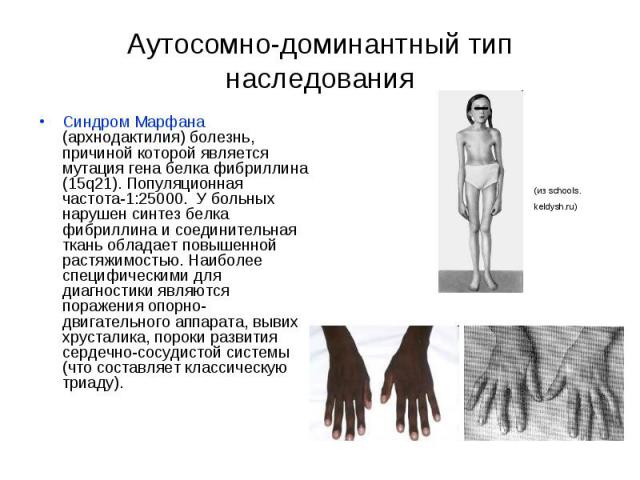
Аутосомно-доминантный тип наследования Синдром Марфана (архнодактилия) болезнь, причиной которой является мутация гена белка фибриллина (15q21). Популяционная частота-1:25000. У больных нарушен синтез белка фибриллина и соединительная ткань обладает повышенной растяжимостью. Наиболее специфическими для диагностики являются поражения опорно-двигательного аппарата, вывих хрусталика, пороки развития сердечно-сосудистой системы (что составляет классическую триаду).

Синдром Марфана ?

Аутосомно-рецессивный тип наследования характеризуется следующими признаками: больные не в каждом поколении; больной ребенок (гомозигота) рождается у здоровых родителей (гетерозигот); болеют в равной степени мужчины и женщины; проявление признака (болезни) наблюдается по горизонтали; вероятность наследования 25% (если оба родителя гетерозиготны), 50% (если один родитель гетерозиготен, а второй гомозиготен по рецессивному признаку) и 100% (если оба родителя рецессивные гомозиготы).

Альбинизм врожденное отсутствие пигмента кожи, волос, радужной и пигментной оболочек глаза встречается в разных популяциях с разной частотой - от 1:5000 до 1:25000. Основными клиническими проявлениями альбинизма в любом возрасте являются отсутствие меланина в клетках кожи (молочно-белый ее цвет), очень светлые волосы, светло-серая или светло-голубая радужная оболочка глаз, красный зрачок, повышенная чувствительность к УФ-облучению

Альбинизм у представителей разных рас

Типы альбинизма Глазокожный альбинизм 1 А - самая тяжелая форма альбинизма. Он появляется в результате миссенс, нонсенс мутаций, мутаций ошибки рамки считывания в гене тирозиназы на хромосоме 11 (11q24). Глазокожный альбинизм 2 (тирозин-позитивный) - наиболее распространенный тип альбинизма во всех расах. Это заболевание также аутосомно-рецессивное, но локализуется на 15 хромосоме, в отличие от ГКА 1 (15q11-13). В этом случае поражается ген, кодирующий P-протеин, а синтез тирозиназы остается нормальным.
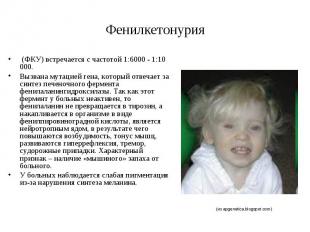
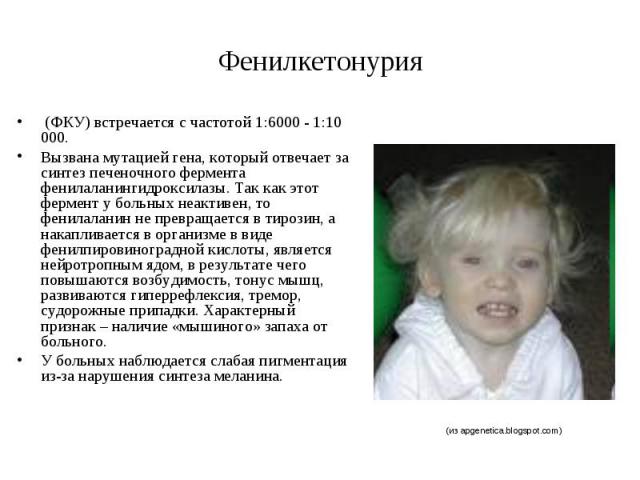
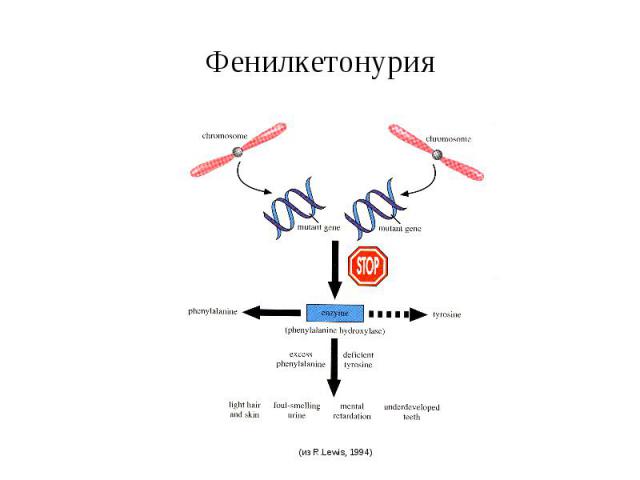
Фенилкетонурия (ФКУ) встречается с частотой 1:6000 - 1:10 000. Вызвана мутацией гена, который отвечает за синтез печеночного фермента фенилаланингидроксилазы. Так как этот фермент у больных неактивен, то фенилаланин не превращается в тирозин, а накапливается в организме в виде фенилпировиноградной кислоты, является нейротропным ядом, в результате чего повышаются возбудимость, тонус мышц, развиваются гиперрефлексия, тремор, судорожные припадки. Характерный признак – наличие «мышиного» запаха от больного. У больных наблюдается слабая пигментация из-за нарушения синтеза меланина.

Фенилкетонурия Кроме того, образуются также почти полностью отсутствующие в норме фенилэтиламин и ортофенилацетат, избыток которых вызывает нарушение метаболизма липидов в головном мозге. Предположительно, это и ведёт к прогрессирующему снижению интеллекта у таких больных вплоть до идиотии. Окончательно механизм развития нарушений функций мозга при фенилкетонурии остается неясным. Ген фенилкетонурии (PKU) локализован в длином плече 12 хромосомы (12q24.1).
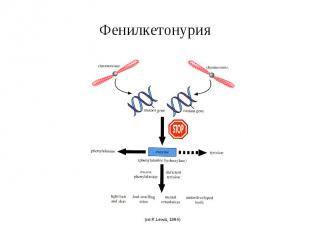
Фенилкетонурия

Алкаптонурия метаболическое заболевание, обусловленное мутацией гена АР (3q25-26), кодирующего синтез оксидазы гомогентизиновой кислоты. этот дефект приводит к нарушению катаболизма аминокислоты тирозина, сопровождается повышенным накоплением гомогентизиновой кислоты в организме и выделением ее с мочой. Вследствие этого со временем происходят изменения в разных тканях, прежде всего в соединительной.
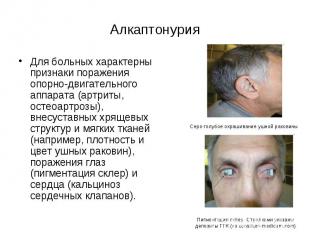
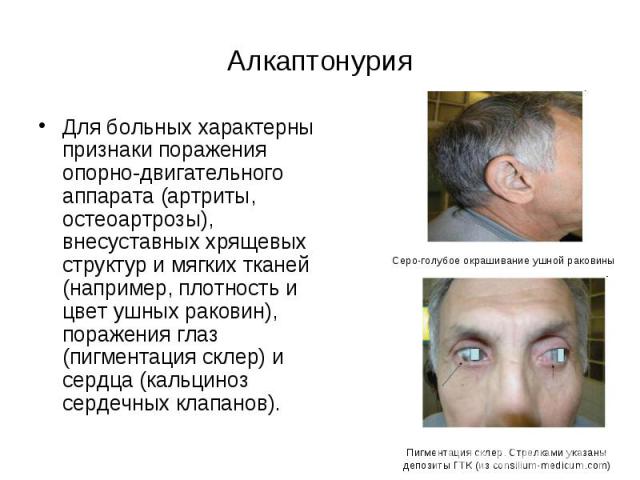
Алкаптонурия Для больных характерны признаки поражения опорно-двигательного аппарата (артриты, остеоартрозы), внесуставных хрящевых структур и мягких тканей (например, плотность и цвет ушных раковин), поражения глаз (пигментация склер) и сердца (кальциноз сердечных клапанов).

Тирозинемия заболевание, связанное с дефицитом активности фумарилацетоацетатгидроксилазы. Ген локализован на 15-й хромосоме (15q23-q25). Мутации приводят к нарушению метаболизма тирозина с повреждением печени, почек, периферических нервов. Первым пораженным органом является печень, в течение первых месяцев жизни отмечаются начальные проявления печеночной дисфункции с отдаленным исходом в цирроз и печеночную карциному. У некоторых пациентов развивается нефрокальциноз и почечная недостаточность. Возрастание уровня тирозина и метионина в сыворотке вызывают появление «капустного» запаха от больных.
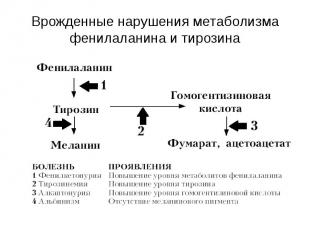
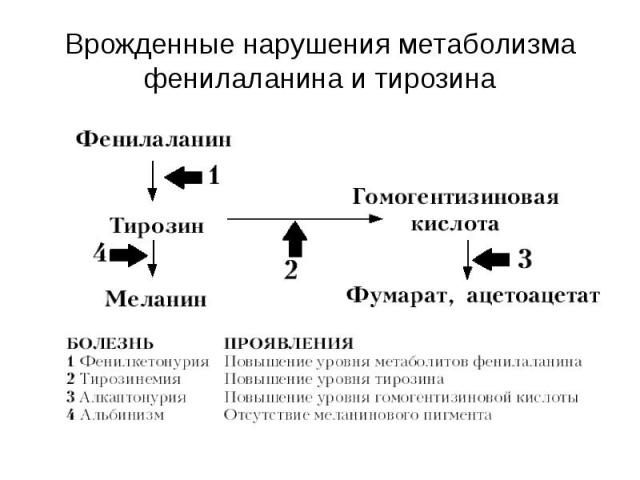
Врожденные нарушения метаболизма фенилаланина и тирозина
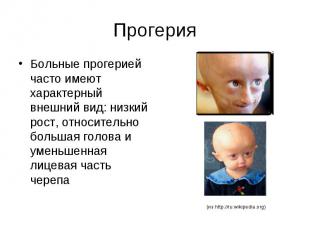
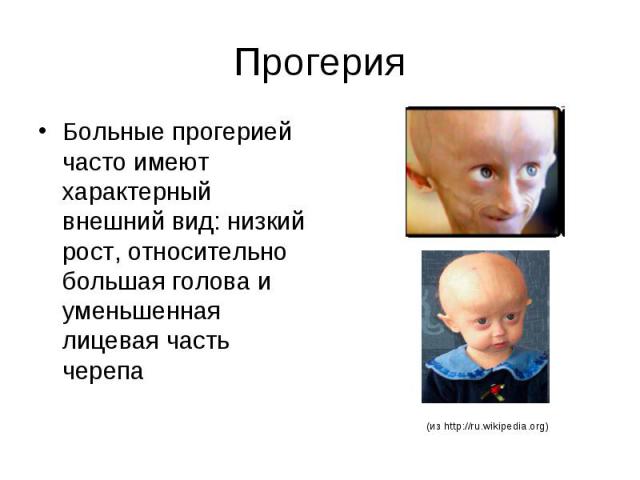
Прогерия Больные прогерией часто имеют характерный внешний вид: низкий рост, относительно большая голова и уменьшенная лицевая часть черепа

Прогерия характеризуется комплексом изменений кожи и внутренних органов, обусловленных преждевременным старением организма. Основными формами является детская прогерия (синдром Гетчинсона - Гилфорда) и прогерия взрослых (синдром Вернера).

Детская прогерия Причина детской прогерии — мутации гена LMNA, кодирующего ламин А (1q22). Вероятный тип наследования: аутосомно-рецессивный. Популяционная частота: менее 1:250000. Ядерные ламины - фибриллярные белки, обеспечивающие структурную функцию и регуляцию транскрипции в ядре клеток. Белки ядерной ламины участвуют в разнообразных функциях, включая механическую стабильность ядра, регуляцию клеточного цикла, репликацию ДНК, транскрипцию РНК, апоптоз и старение.

Детская прогерия клинические признаки проявляются обычно на 2—3-м году жизни. Резко замедляется рост ребенка, отмечаются атрофические изменения дермы, подкожной клетчатки, особенно на лице, конечностях. Кожа истончается, становится сухой, морщинистой, на туловище могут быть склеродермоподобные очаги, участки гиперпигментации. Сквозь истонченную кожу просвечивают вены. Внешний вид больного: большая голова, лобные бугры выступают над маленьким заостренным («птичьим») лицом с клювовидным носом, нижняя челюсть недоразвита.

Детская прогерия Средняя продолжительность жизни при детской прогерии — 13 лет. Большинство источников указывают возраст смерти от 7 до 27 лет, при этом случаи достижения совершеннолетия очень редки.
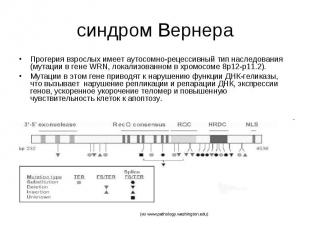
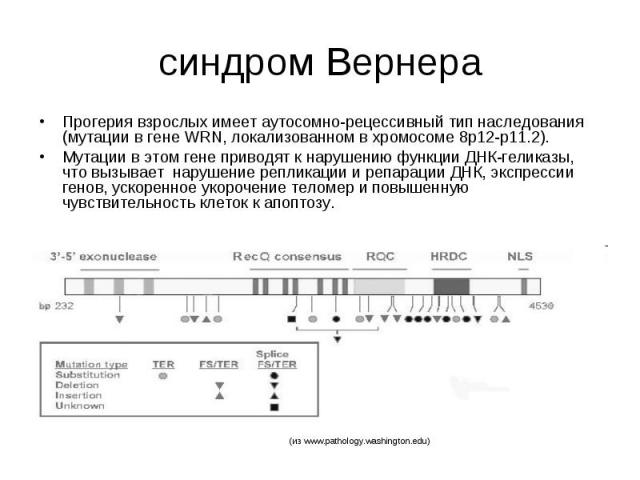
синдром Вернера Прогерия взрослых имеет аутосомно-рецессивный тип наследования (мутации в гене WRN, локализованном в хромосоме 8p12-p11.2). Мутации в этом гене приводят к нарушению функции ДНК-геликазы, что вызывает нарушение репликации и репарации ДНК, экспрессии генов, ускоренное укорочение теломер и повышенную чувствительность клеток к апоптозу.
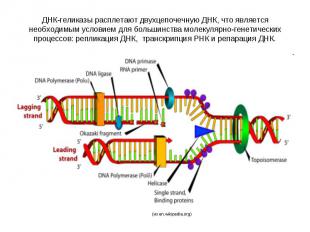
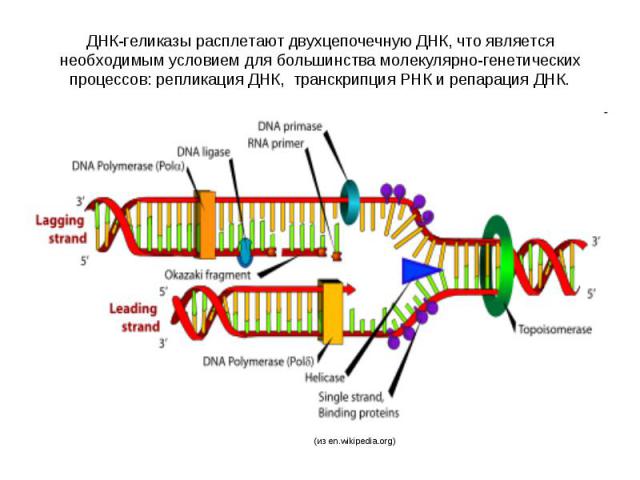
ДНК-геликазы расплетают двухцепочечную ДНК, что является необходимым условием для большинства молекулярно-генетических процессов: репликация ДНК, транскрипция РНК и репарация ДНК.

синдром Вернера Клинически заболевание проявляется в период полового созревания. Отмечаются замедленный рост, гипогонадизм. Обычно на третьем десятилетии жизни у больного седеют и выпадают волосы, развивается катаракта, постепенно истончается кожа и атрофируется подкожная клетчатка на лице и конечностях, вследствие чего руки и особенно ноги становятся тонкими. Больные преждевременно погибают либо от рака, либо от сердечно-сосудистой патологии. Средняя продолжительность жизни при данном заболевании – 40-50 лет.

Синдром Блума Обусловлен мутациями в гене BLM, принадлежащем к генам ДНК-геликаз. Тип наследования – аутосомно-рецессивный (19q13.3). У больных отмечается гиперчувствительность к ультрафиолету, иммунодефицит, малорослость, остеосаркомы (являющиеся причиной смерти до 30 лет). синдром характеризуется нестабильностью генома и повышенным риском канцерогенеза.
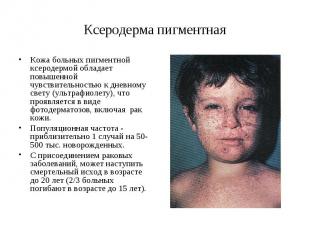
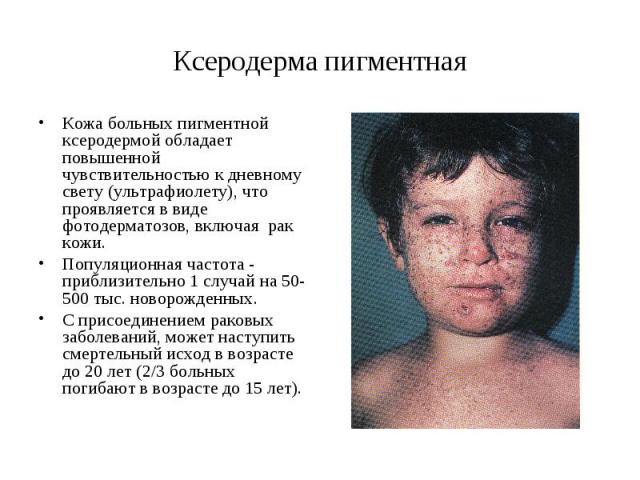
Ксеродерма пигментная Кожа больных пигментной ксеродермой обладает повышенной чувствительностью к дневному свету (ультрафиолету), что проявляется в виде фотодерматозов, включая рак кожи. Популяционная частота - приблизительно 1 случай на 50-500 тыс. новорожденных. С присоединением раковых заболеваний, может наступить смертельный исход в возрасте до 20 лет (2/3 больных погибают в возрасте до 15 лет).

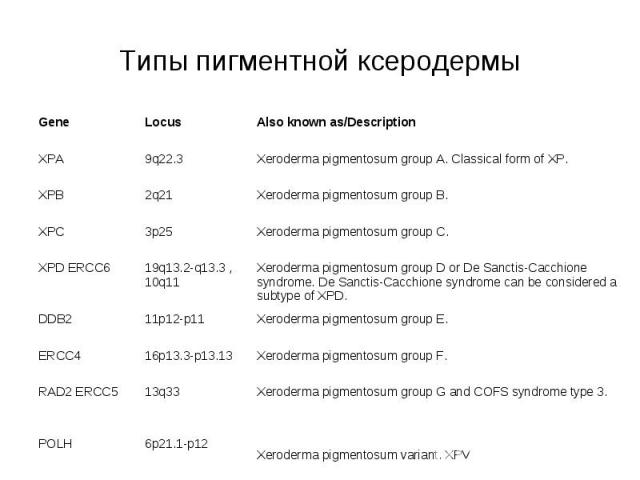
Ксеродерма пигментная заболевание вызывается генетическими дефектами раннего этапа эксцизионной репарации нуклеотидов. Существует семь комплементарных групп генов пигментной ксеродермы (от XPA до XPG), локализованных в разных хромосомах.

Типы пигментной ксеродермы
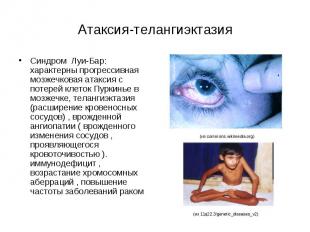
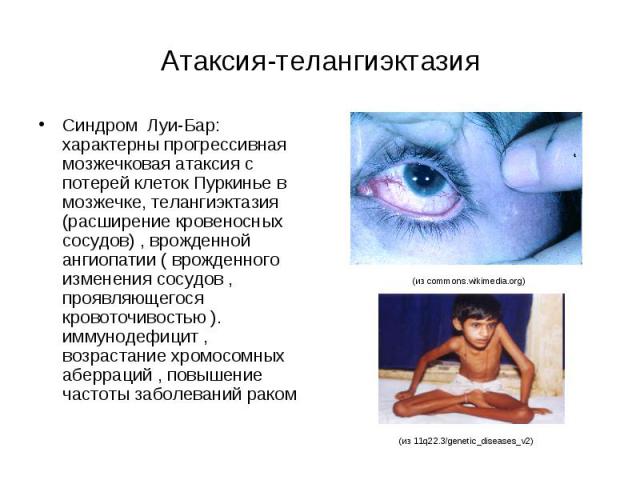
Атаксия-телангиэктазия Синдром Луи-Бар: характерны прогрессивная мозжечковая атаксия с потерей клеток Пуркинье в мозжечке, телангиэктазия (расширение кровеносных сосудов) , врожденной ангиопатии ( врожденного изменения сосудов , проявляющегося кровоточивостью ). иммунодефицит , возрастание хромосомных аберраций , повышение частоты заболеваний раком
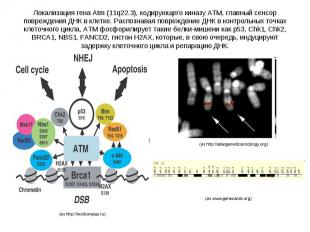
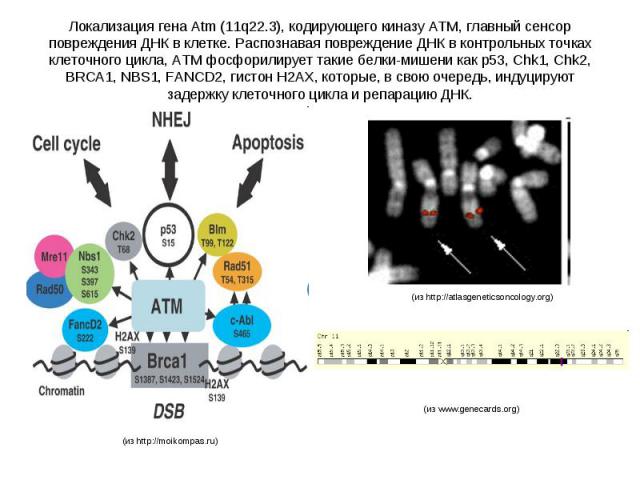
Локализация гена Atm (11q22.3), кодирующего киназу ATM, главный сенсор повреждения ДНК в клетке. Распознавая повреждение ДНК в контрольных точках клеточного цикла, ATM фосфорилирует такие белки-мишени как р53, Chk1, Chk2, BRCA1, NBS1, FANCD2, гистон H2AX, которые, в свою очередь, индуцируют задержку клеточного цикла и репарацию ДНК.
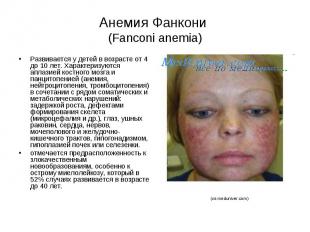
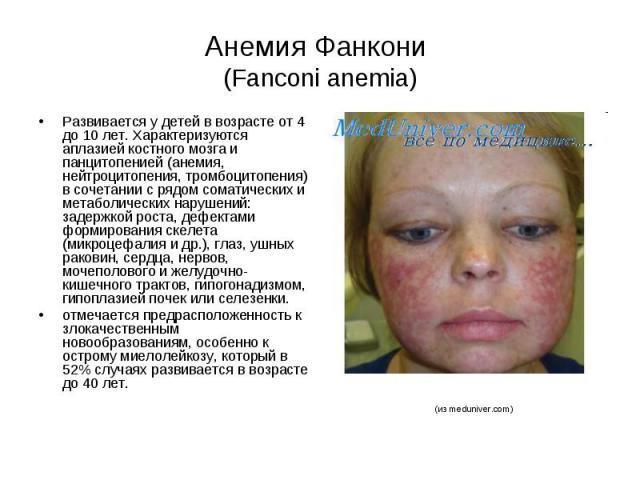
Анемия Фанкони (Fanconi anemia) Развивается у детей в возрасте от 4 до 10 лет. Характеризуются аплазией костного мозга и панцитопенией (анемия, нейтроцитопения, тромбоцитопения) в сочетании с рядом соматических и метаболических нарушений: задержкой роста, дефектами формирования скелета (микроцефалия и др.), глаз, ушных раковин, сердца, нервов, мочеполового и желудочно-кишечного трактов, гипогонадизмом, гипоплазией почек или селезенки. отмечается предрасположенность к злокачественным новообразованиям, особенно к острому миелолейкозу, который в 52% случаях развивается в возрасте до 40 лет.
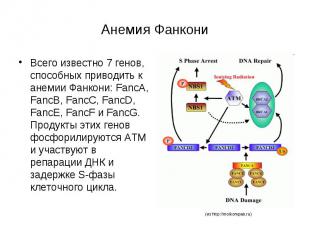
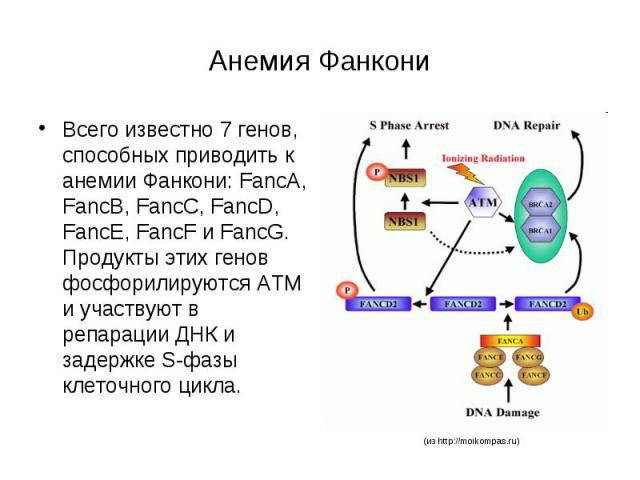
Анемия Фанкони Всего известно 7 генов, способных приводить к анемии Фанкони: FancA, FancB, FancC, FancD, FancE, FancF и FancG. Продукты этих генов фосфорилируются ATM и участвуют в репарации ДНК и задержке S-фазы клеточного цикла.
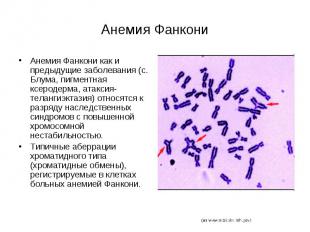
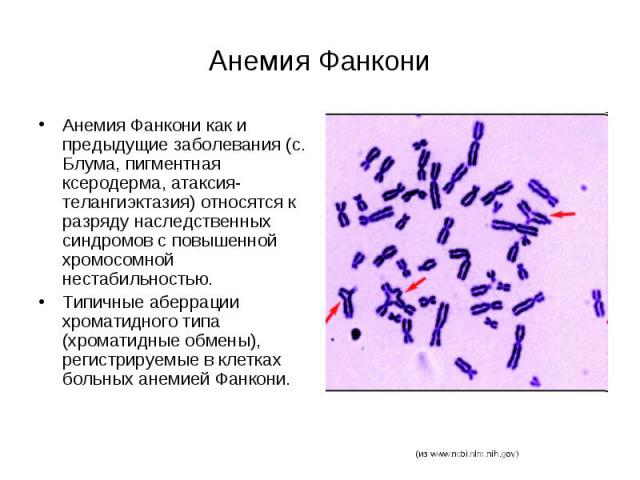
Анемия Фанкони Анемия Фанкони как и предыдущие заболевания (с. Блума, пигментная ксеродерма, атаксия-телангиэктазия) относятся к разряду наследственных синдромов с повышенной хромосомной нестабильностью. Типичные аберрации хроматидного типа (хроматидные обмены), регистрируемые в клетках больных анемией Фанкони.
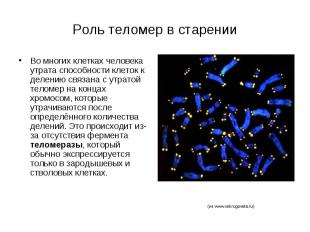
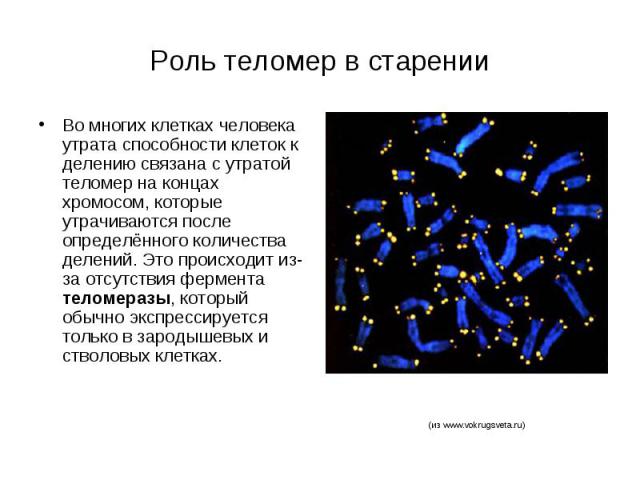
Роль теломер в старении Во многих клетках человека утрата способности клеток к делению связана с утратой теломер на концах хромосом, которые утрачиваются после определённого количества делений. Это происходит из-за отсутствия фермента теломеразы, который обычно экспрессируется только в зародышевых и стволовых клетках.

Общие причины синдромов преждевременного старения Нарушение свойств теломер, хроматина и клеточного ядра Нарушение репарации и репликации ДНК, генетическая нестабильность Нарушение экспрессии генов Репликативное старение Повышенная чувствительность клеток к апоптозу. Вполне вероятно, что те же самые механизмы задействованы в "нормальном" старении.

Х-сцепленный рецессивный тип наследования характеризуется следующими признаками: больные появляются не в каждом поколении; больной ребенок рождается у здоровых родителей; болеют преимущественно мужчины; проявление болезни наблюдается преимущественно по горизонтали; вероятность наследования - у 25% всех детей, в том числе у 50% мальчиков; здоровые мужчины не передают болезни.

Дальтонизм - частичная цветовая слепота, один из видов нарушения цветового зрения. Д. впервые описан в 1794 Дж. Дальтоном, который сам страдал этим недостатком. Д. встречается у 8% мужчин и у 0,5% женщин. Предполагается, что в сетчатой оболочке глаза существуют три элемента, каждый из которых воспринимает только один из трёх основных цветов (красный, зелёный, фиолетовый), смешением которых получаются все воспринимаемые нормальным глазом оттенки. Это - нормальное, т. н. трихроматическое цветоощущение. При выпадении одного из этих элементов наступает частичная цветовая слепота — дихромазия.


Гемофилия А - тяжелое заболевание, обусловленное дефектом фактора VIII свертывания крови. Встречается с частотой 1:2500 новорожденных мальчиков. Ген расположен в длинном плече Х-хромосомы (Xq28), структура его установлена. Заболевание распознается обычно на 2-3-м году жизни. Для него характерны множественные гематомы. Преобладают кровоизлияния в крупные суставы конечностей, подкожные, внутри- и межмышечные гематомы, кровотечения при травмах и хирургических вмешательствах, наличие крови в моче. Кровоизлияния в полость суставов приводят к развитию стойкой их тугоподвижности из-за остеоартрозов (развитие соединительной ткани в суставах).

Синдром Леша-Нихана (Lesch-Nyhan) обусловлен недостаточностью фермента гипоксантинфосфорибозилтрансферазы (ГФРТ), который катализирует присоединение свободных пуриновых оснований (гуанина и гипоксантина) к нуклеотидам. При недостаточности фермента ГФРТ конечным продуктом превращения пуриновых оснований является мочевая кислота. В первые месяцы жизни отмечаются задержка развития двигательных навыков. Болезнь сопровождается олигофренией, склонностью ребенка к самоповреждениям (кусание пальцев, губ, внутренней поверхности щёк). Высокое содержание мочевой кислоты и ее солей, несмотря на усиленное выделение их с мочой, приводит к формированию камней в мочевыводящих путях, отложению солей мочевой кислоты в суставах, подагре.

Синдром Леша-Нихана Ген, кодирующий фермент гипоксантинфосфо-рибозилтрансферазу локализован в длином плече Х-хромосомы (Xq26-q27.2) Синдром встречается редко (1:300000 рождений).
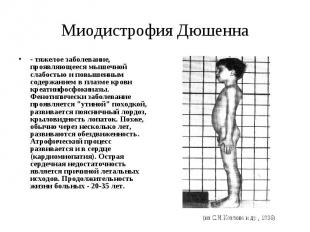
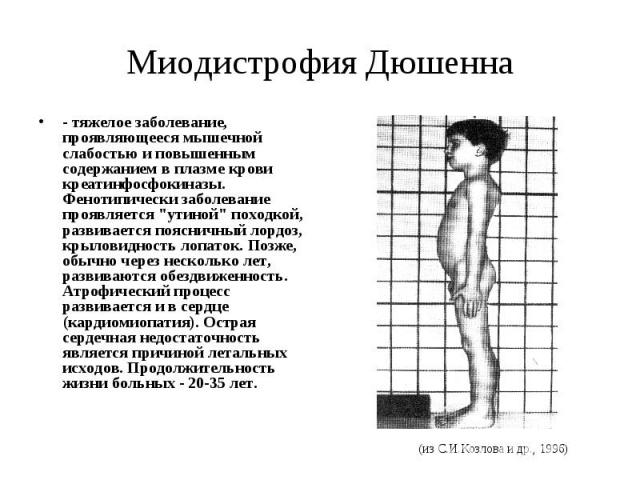
Миодистрофия Дюшенна - тяжелое заболевание, проявляющееся мышечной слабостью и повышенным содержанием в плазме крови креатинфосфокиназы. Фенотипически заболевание проявляется "утиной" походкой, развивается поясничный лордоз, крыловидность лопаток. Позже, обычно через несколько лет, развиваются обездвиженность. Атрофический процесс развивается и в сердце (кардиомиопатия). Острая сердечная недостаточность является причиной летальных исходов. Продолжительность жизни больных - 20-35 лет.

Х-сцепленный доминантный тип наследования сходен с аутосомно-доминантным, за исключением того, что мужчина передает этот признак только дочерям (т.к. сыновья получают от отца Y-хромосому). Примерами таких заболеваний являются: Гипоплазия эмали - резкое истончение эмали, сопровождающееся изменением цвета зубов. Пятна и дефекты различной формы появляются на зубах симметрично.
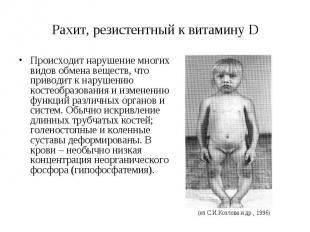
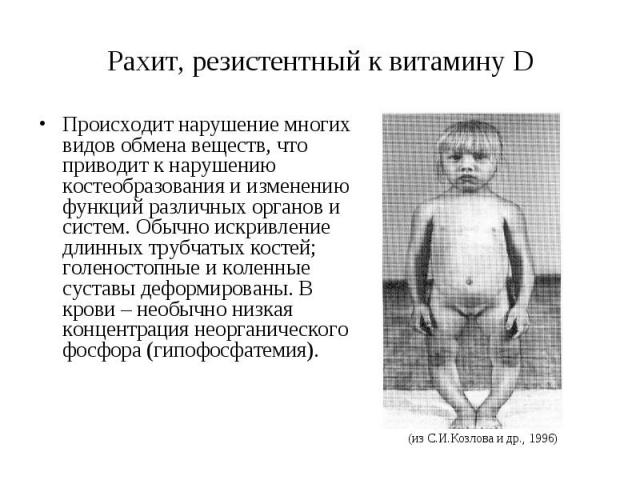
Рахит, резистентный к витамину D Происходит нарушение многих видов обмена веществ, что приводит к нарушению костеобразования и изменению функций различных органов и систем. Обычно искривление длинных трубчатых костей; голеностопные и коленные суставы деформированы. В крови – необычно низкая концентрация неорганического фосфора (гипофосфатемия).