Презентация на тему: ФАРМАКОТЕРАПИЯ АНТИКОАГУЛЯНТАМИ

Фармакотерапия антитромбоцитарными, антикоагулянтными и фибринолитическими препаратами в клинике внутренних болезней Кафедра госпитальной терапии Доцент С.А. Матвеева 2008 г.

Введение

Введение

Введение

Антитромбоцитарные средства В современных руководствах указано, что прием антитромбоцитарных средств является обязательным компонентом лечения сердечно-сосудистых заболеваний. Основными антитромбоцитарными препаратами современного врача являются аспирин, тиклопидин, клопидогрель.


Ацетилсалициловая кислота (аспирин) В основе антитромбоцитарного действия аспирина лежит ингибирование циклооксигеназы и синтеза тромбоцитарного тромбоксана А2. При назначении аспирина пациентам со стабильной стенокардией напряжения в среднем на 33% снижается риск неблагоприятных сердечно-сосудистых исходов – инфаркта миокарда, внезапной смерти.

Ацетилсалициловая кислота (аспирин) Ацетилсалициловая кислота (аспирин) При острых формах ИБС (нестабильная стенокардия, инфаркт миокарда) и инвазивных вмешательствах на коронарных артериях (ангиопластика, стентирование, атерэктомия), когда требуется быстрый антиагрегантный эффект, необходимо применение более высоких доз аспирина (>325 мг/сут) - с последующим снижением для уменьшения риска геморрагических осложнений. Для вторичной профилактики сосудистых осложнений пациентам следует назначать малые дозы аспирина (75-150 мг/сут).
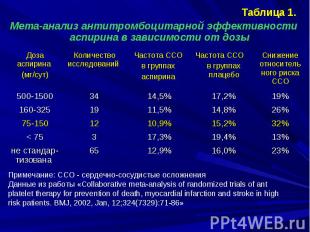
Таблица 1. Таблица 1. Мета-анализ антитромбоцитарной эффективности аспирина в зависимости от дозы

Ацетилсалициловая кислота (аспирин) Данные, обобщенные в ходе мета-анализа, свидетельствуют, что на фоне приема малых доз аспирина (75-150 мг/сут) вся циклооксигеназа тромбоцитов практически полностью блокирована через несколько суток, что обеспечивает антитромботический эффект препарата. Ацетилсалициловая кислота (аспирин) Данные, обобщенные в ходе мета-анализа, свидетельствуют, что на фоне приема малых доз аспирина (75-150 мг/сут) вся циклооксигеназа тромбоцитов практически полностью блокирована через несколько суток, что обеспечивает антитромботический эффект препарата. Учитывая повсеместное назначение аспирина для продолжительного приема при различных сердечно-сосудистых заболеваниях (в т.ч. пожилым людям), вопросы безопасности терапии этим препаратом становятся актуальными.

Ацетилсалициловая кислота (аспирин) Ацетилсалициловая кислота (аспирин) Прием средних (160-325 мг/сут) и высоких (500-1500 мг/сут) доз аспирина не усиливает его антитромботическую активность и не повышает профилактическую целесообразность приема. Однако средние и высокие дозы аспирина вызывают достоверно более частые осложнения (как правило, желудочно-кишечные кровотечения, в т.ч. опасные для жизни).

обострение язвенной болезни, обострение язвенной болезни, геморрагические диатезы повышенная чувствительность к салицилатам.

Антитромбоцитарные средства В случаях непереносимости аспирина рекомендуется применение препаратов из группы тиенопиридинов (тиклопидин, клопидогрель). Основным недостатком тиенопиридинов является медленное развитие антиагрегационного эффекта.

Тиклопидин Тиклопидин Тиклопидин ингибирует агрегацию тромбоцитов, вызванную АДФ, тромбином, коллагеном, тромбоксаном А2 и фактором агрегации тромбоцитов. При стабильной стенокардии напряжения тиклопидин снижает вязкость крови, уменьшая концентрацию фибриногена плазмы. Длительное применение препарата ограничено из-за побочных эффектов, наиболее опасными из которых являются нейтропения и тромбоцитопеническая пурпура.

Клопидогрель Клопидогрель Клопидогрель, подобно тиклопидину, является производным тиенопиридина, но превосходит тиклопидин по антитромботическому эффекту. В сравнительных исследованиях клопидогрель превосходил аспирин в снижении комбинированного риска инфаркта миокарда, сосудистой смерти и инсульта среди пациентов с постинфарктным кардиосклерозом, инсультом и периферическим атеросклерозом.

Перспективной считается концепция комбинированной антиагрегантной терапии, т.е. одновременного блокирующего воздействия на различные пути активации тромбоцитов. Перспективной считается концепция комбинированной антиагрегантной терапии, т.е. одновременного блокирующего воздействия на различные пути активации тромбоцитов. Рандомизированное исследование CURE, включавшее более 12500 больных: клопидогрель (300 мг/сут), клопидогрель в дозе 75 мг/сут в сочетании с аспирином (75-325 мг/сут) - доказана эффективность в предотвращении (в среднем на 20%) вероятности инфаркта миокарда, инсульта и смерти от сердечно-сосудистых осложнений у больных с нестабильной стенокардией и другими проявлениями ОКС.

В исследовании CURE показано, что лечение больных, перенесших ОКС без подъема сегмента ST, комбинацией аспирина и клопидогреля по сравнению с терапией только аспирином приводит к достоверно более выраженному снижению риска развития сердечно-сосудистых событий при отсутствии разницы по количеству жизнеугрожающих кровотечений.

Необходимо помнить, клопидогрель реже, чем аспирин, вызывает опасные желудочно-кишечные кровотечения, но прием клопидогреля на 30% чаще сопровождается появлением диареи и кожных высыпаний. Необходимо помнить, клопидогрель реже, чем аспирин, вызывает опасные желудочно-кишечные кровотечения, но прием клопидогреля на 30% чаще сопровождается появлением диареи и кожных высыпаний.

Профилактика повторного инфаркта миокарда Аспирин 100 мг 1 раз/сут, длительно в течение многих лет при наличии противопоказаний. При выраженном периферическом атеросклерозе: тиклопидин 250 мг 2 раза (у пожилых пациентов 1 раз/сут) или клопидогрель 75 мг 1 раз/сут.

Профилактика коронарного тромбоза после транслюминальной ангиоластики аспирин 100-300 мг 1 раз/сут комбинация с тиклопидином по 250 мг 2 раза/сут в течение первого месяца после операции

Антитромбоцитарные средства Антитромбоцитарные средства Антагонисты рецепторов llb/llla тромбоцитов Абциксимаб, эптифибатид, тирофибан, ламифибан способны блокировать агрегацию тромбоцитов, вызываемую любым физиологическим индуктором. По данным исследований (EPILOG, EPISTENT, EPIC, CAPTURE, PRISM-PLUS, PURSUIT, PARAGON и др.), внутривенное введение этих препаратов больным с ОКС без подъема сегмента ST в дополнение к аспирину и НФГ улучшает результаты коронарной баллонной ангиопластики как в сочетании, так и без сочетания с установкой стента.

Рекомендуемые дозы антагонистов Рекомендуемые дозы антагонистов гликопротеиновых рецепторов llb/llla Абциксимаб - внутривенно болюс 0,25 мг/кг с последующей инфузией 0,125 мкг/кг/мин в течение 12-24 ч; Эптифибатид - внутривенно болюс 180 мг/кг с последующей инфузией 2,0 мкг/кг/мин в течение 72-96 ч; Тирофибан - внутривенная инфузия 0,4 мкг/кг/мин в течение 0,5 ч, затем 0,1 мкг/кг/мин в течение 48-96 ч.

Абциксимаб эффективен только у больных, которым проводилась реваскуляризация миокарда, Абциксимаб эффективен только у больных, которым проводилась реваскуляризация миокарда, Тирофибан и эптифибатид как при проведении реваскуляризации, так и при медикаментозном лечении. Дополнительное снижение числа неблагоприятных исходов было особенно выраженным при добавлении антагонистов гликопротеиновых рецепторов llb/llla к стандартному антитромботическому лечению у больных с повышенным уровнем сердечных тропонинов.

Антагонисты гликопротеиновых рецепторов llb/llla тромбоцитов не продемонстрировали эффективности в клинических исследованиях у пациентов со стабильной стенокардией. Антагонисты гликопротеиновых рецепторов llb/llla тромбоцитов не продемонстрировали эффективности в клинических исследованиях у пациентов со стабильной стенокардией. Основным показанием к применению антагонистов гликопротеиновых рецепторов llb/llla у больных с ОКС является: отсутствие стойкого подъема сегмента ST в сочетании с высоким непосредственным риском смерти, развития инфаркта миокарда при запланированном проведении процедуры реваскуляризации миокарда в ближайшие 24 ч.

Длительное применение антагонистов гликопротеиновых рецепторов llb/llla тромбоцитов внутрь, по данным исследований OPUS-TIMI и SYMPHONY, не оказывало положительного влияния на результаты лечения больных с ОКС.

Антикоагулянты Антикоагулянты прямого действия - препараты, которые оказывают непосредственное влияние на активность циркулирующих в крови факторов свертывания. Общим свойством антикоагулянтов прямого действия является их способность тормозить ферментативную активность тромбина (или фактора IIа), который играет ключевую роль в тромбообразовании. Антикоагулянты непрямого действия – препараты, тормозящие синтез протромбина и других факторов свертывания в печени.

Различают две основные группы антикоагулянтов прямого действия: зависимые от АТ-III (непрямые ингибиторы тромбина), независимые от АТ-III (прямые ингибиторы тромбина).

Непрямые ингибиторы тромбина Непрямые ингибиторы тромбина В группу непрямых ингибиторов тромбина входят гепарин, его производные, которые способны тормозить активность тромбина в присутствии плазменных кофакторов и АТ- III.

Прямые ингибиторы тромбина Эту группу прямых антикоагулянтов называют независимыми от АТ-III ингибиторами тромбина, или прямыми (селективными, специфическими) ингибиторами тромбина.

Антикоагулянты для парентерального введения ГЕПАРИН СТАНДАРТНЫЙ (нефракционированный) - антикоагулянт животного происхождения, синтезируется тучными клетками (мастоцитами), в виде неоднородной смеси мукополисахаридных цепей различной длины: от 2-5 тыс. (низкомолекулярные цепи) до 10-50 тыс. (высокомолекулярные цепи) дальтон.

Существуют различные соли гепарина (натриевая, кальциевая, калиевая, магниевая, бариевая). Существуют различные соли гепарина (натриевая, кальциевая, калиевая, магниевая, бариевая). Наиболее широко используются натриевая и кальциевая соли гепарина. Клиническая эффективность этих двух солей гепарина практически одинакова.

Препараты стандартного (нефракционированного) гепарина Препараты стандартного (нефракционированного) гепарина А. Препараты натриевой соли гепарина (внутривенное и подкожное введение) Гепарин - раствор 5 мл (25 тыс. ЕД) во флаконах. Б. Кальциевая соль гепарина (только для подкожного применения) Кальципарин 1 ампула - раствор 0,5 мл (12,5 тыс. ЕД) 1 заполненный шприц - раствор 0,2 мл (5 тыс. ЕД)

В результате угнетения тромбина развивается выраженное противо-свертывающее, противотромботическое и прогеморрагическое действие. В результате угнетения тромбина развивается выраженное противо-свертывающее, противотромботическое и прогеморрагическое действие. Гепаринотерапия, за исключением подкожного применения малых доз препарата, должна проводиться в стационарных условиях под адекватным лабораторным контролем.

Способ применения и дозы для лечения артериального, венозного и внутрисердечного тромбоза гепарин вводится внутривенно: первично болюсно 5-10 тыс. ЕД с последующей инфузией со скоростью 1-2 тыс. ЕД/ч; или подкожно в переднюю область брюшной стенки по 12,5 тыс. ЕД 2 раза в сутки. у больных с низким весом, детей внутривенно инфузия гепарина производится со скоростью 15-25 ЕД/кг/ч или 250 ЕД/кг каждые 12 ч. для профилактики венозных тромбозов и ТЭЛА гепарин вводится подкожно по 5 тыс. ЕД 3-4 раза в сутки.

Гепаринотерапия проводится под контролем АЧТВ или времени свертывания крови. Гепаринотерапия проводится под контролем АЧТВ или времени свертывания крови. АЧТВ - до увеличения показателей в 1,2-1,5 раза при профилактике венозного тромбоза и в 2-3 раза при лечении артериального тромбоза. При невозможности регулярного определения АЧТВ внутривенную гепаринотерапию проводят под контролем времени свертывания крови, которое должно быть увеличено в 2-2,5 раза по сравнению с нормой (11-14 сек).

При назначении терапевтических ("высоких") доз гепарина следует отдавать предпочтение внутривенному непрерывному способу его введения, который позволяет поддерживать оптимальные значения АЧТВ на протяжении суток. При назначении терапевтических ("высоких") доз гепарина следует отдавать предпочтение внутривенному непрерывному способу его введения, который позволяет поддерживать оптимальные значения АЧТВ на протяжении суток.

В начале 5000 ЕД гепарина вводят внутривенно в виде болюса, затем начинают непрерывную инфузию со средней скоростью 1000 ЕМ/ч. В начале 5000 ЕД гепарина вводят внутривенно в виде болюса, затем начинают непрерывную инфузию со средней скоростью 1000 ЕМ/ч. Скорость инфузии изменяют в зависимости от значений АЧТВ, которое определяют до введения гепарина, а в дальнейшем через 6 и 12 ч после болюсного введения в 1-е сутки, затем не менее 1 раза в день. Предложены схемы дозирования гепарина при внутривенной непрерывной его инфузии под контролем АЧТВ.

Внутривенный прерывистый способ назначения гепарина ведет к высокому риску возникновения кровотечений по сравнению с непрерывной инфузией и не обеспечивает необходимого антитромботического лечебного эффекта.

Показания Показания нестабильная стенокардия, инфаркт миокарда, острая окклюзия периферических артерий, тромбоз глубоких вен, тромбоэмболия легочной артерии, синдром диссеминированного внутрисосудистого свертывания крови, протезирование клапанов сердца, экстракорпоральное кровообращение.

Противопоказания Противопоказания гемофилия, тромбоцитопения и другие геморрагические диатезы, язвы желудка и кишечника, геморрагический инсульт, тяжелая артериальная гипертензия, черепно-мозговая травма, хирургические операции на ЦНС, артериальная и люмбальная пункции, бактериальный эндокардит, тяжелая печеночная, почечная недостаточность, аллергические реакции.

В случаях ОКС со стойким подъемом сегмента ST при отсутствии противопоказаний гепарин показан всем больным, не получавшим ТЛТ, а также больным, у которых планируется проведение реваскуляризации миокарда. В случаях ОКС со стойким подъемом сегмента ST при отсутствии противопоказаний гепарин показан всем больным, не получавшим ТЛТ, а также больным, у которых планируется проведение реваскуляризации миокарда. НФГ рекомендуется вводить подкожно по 7,5 тыс.-12,5 тыс. ЕД 2 раза в день или внутривенно.

Внутривенный путь введения НФГ применяется у больных с повышенным риском тромбоэмболических осложнений: Внутривенный путь введения НФГ применяется у больных с повышенным риском тромбоэмболических осложнений: обширный ИМ, передняя локализация ИМ, фибрилляция предсердий, тромбоэмболии в анамнезе, документированный тромб в левом желудочке).

НФГ вводится не только больным со стойкой элевацией сегмента ST, но и пациентам с другими вариантами ОКС. НФГ вводится не только больным со стойкой элевацией сегмента ST, но и пациентам с другими вариантами ОКС. Основными противопоказаниями к гепаринотерапии являются активное кровотечение и заболевания, сопровождающиеся высоким риском его возникновения.

Взаимодействие Взаимодействие Действие гепарина уменьшается при одновременном применении с АКТГ, тироксином, тетрациклином. Эффект гепарина усиливается непрямыми антикоагулянтами, антиагрегантами, фибринолитическими и нестероидными противовоспали-тельными средствами.

Клинически значимая иммунная тромбоцитопения при гепаринотерапии развивается после 6-10 дней лечения через 5 дней лечения рекомендуется проводить подсчет тромбоцитов в крови. Клинически значимая иммунная тромбоцитопения при гепаринотерапии развивается после 6-10 дней лечения через 5 дней лечения рекомендуется проводить подсчет тромбоцитов в крови. При развитии тромбоцитопении необходимо исключить возможность потребления тромбоцитов вследствие ДВС-синдром, прекратить применение гепарина и перейти на применение низкомолекулярного гепарина (НМГ) или непрямого антикоагулянта.

Передозировка При передозировке гепарина и/или развитии геморрагических осложнений немедленно прекращается введение гепарина и начинает проводиться в/в инфузия протамина сульфата из расчета 1 мг препарата на 100 ЕД введенного гепарина.

В случае снижения АТ-III в результате врожденной недостаточности или чрезмерного потребления при массивном тромбозе перед введением гепарина следует восстановить содержание АТ-III с помощью переливания свежецитратной плазмы или введения препарата АТ-III. В случае снижения АТ-III в результате врожденной недостаточности или чрезмерного потребления при массивном тромбозе перед введением гепарина следует восстановить содержание АТ-III с помощью переливания свежецитратной плазмы или введения препарата АТ-III.

Переход на непрямые антикоагулянты В случае перевода больного с гепаринотерапии на непрямые антикоагулянты последние назначаются за один день до отмены гепарина.

НИЗКОМОЛЕКУЛЯРНЫЙ ГЕПАРИН (фракционированный) НМГ состоит из низкомолекулярных фрагментов (в среднем 4-5 тыс. дальтон) гепарина. В отличие от стандартного гепарина НМГ ингибирует активированный Х (Ха) фактор свертывания крови и в значительно меньшей степени тромбин (фактор IIA).

В связи с низкой антитромбиновой активностью НМГ не вызывает развитие выраженной гипокоагуляции крови, что снижает риск геморрагических осложнений. В связи с низкой антитромбиновой активностью НМГ не вызывает развитие выраженной гипокоагуляции крови, что снижает риск геморрагических осложнений. Уменьшение активности Х (Ха) фактора свертывания крови, активация фибринолиза и положительное влияние НМГ на реологические свойства крови приводит к выраженному противотромботическому действию препарата.

Высокая биодоступность (> 95%) НМГ определяет преимущественно подкожно введение 1-2 раза/сут (период полувыведения препарата составляет 3-4 ч при подкожном введении). Высокая биодоступность (> 95%) НМГ определяет преимущественно подкожно введение 1-2 раза/сут (период полувыведения препарата составляет 3-4 ч при подкожном введении). В связи с отсутствием значительного противосвертывающего эффекта при применении НМГ существенно не изменяются время свертывания крови и АЧТВ.

Лабораторный контроль за лечением НМГ проводится: Лабораторный контроль за лечением НМГ проводится: у больных с повышенным риском геморрагических осложнений, при введении больших доз препарата. Стандартный профилактический режим применения НМГ не требует контроля.

Показания к НМГ Показания к НМГ профилактика и лечение тромбозов глубоких вен; профилактика и лечение тромбоэмболии лёгочной артерии у больных терапевтического профиля; нестабильная стенокардия; инфаркт миокарда без зубца Q; проведение гемодиализа.

Препараты НМГ Препараты НМГ Надропарин(Фраксипарин) - шприцы по (0,3 мл /2850 ME); ( 0,6 мл /5700 МЕ); (1,0 мл /9500 МЕ) по 2 или 10 шт в упаковке. Эноксапарин (Клексан), (Ловенокс) - шприцы по (0,2 мл/2000МЕ/20 мг); (0,4мл /4000МЕ/ 40 мг); (0,6мл /6000 МЕ/ 60 мг); (0,8мл /8000 МЕ /80 мг); (1,0мл /10000МЕ / 100 мг) Дальтепарин (Фрагмин ) - шприцы по 0,2 /2500 МЕ и 0,4 мл/ 5000 МЕ или ампулы по 1000 МЕ. Дозирование НМГ зависит от выбора препарата и цели его введения: профилактики или лечения тромбоза.

НМГ обладают рядом преимуществ по сравнению с НФГ: имеют большую продолжительность действия, более предсказуемый антикоагулянтный эффект, вводятся подкожно в фиксированной дозе, не требуется применения инфузионного насоса, не требуется лабораторный контроль.

Для профилактики тромбоза глубоких вен и тромбоэмболии легочной артерии в зависимости от веса больного (50-100 кг) и степени риска тромбоза вводится 0,2-0,4 мл (30-60 ЕД/кг) НМГ 1 раз в сутки на протяжении 7-10 дней и более. В случае оперативного лечения выбранная доза вводится больному за 2-4 ч перед операцией и в последующем ежедневно 1 раз в сутки.

Для активного лечения ТГВ, ТЭЛА профилактическая доза и кратность введения удваиваются (0,4 - 1,0 мл и более 2 раза в сутки). Для активного лечения ТГВ, ТЭЛА профилактическая доза и кратность введения удваиваются (0,4 - 1,0 мл и более 2 раза в сутки). Контроль за лечением осуществляется с помощью определения АЧТВ.

Противопоказания гемофилия, тромбоцитопения и другие геморрагические диатезы, язвы желудка и кишечника, геморрагический инсульт, тяжелая артериальная гипертензия, черепно-мозговая травма, хирургические операции на ЦНС, артериальная и люмбальная пункции, бактериальный эндокардит, тяжелая печеночная, почечная недостаточность, аллергические реакции.

Побочные действия геморрагические осложнения (геморрагии в местах иньекций, гематурия, геморрагический инсульт, кровотечения); некроз кожи в месте иньекции; иммунная тромбоцитопения; остеопороз при длительном применении; аллергические реакции.

Меры предосторожности Меры предосторожности Требуется осторожное применение гепарина при почечной и печеночной недостаточности и у лиц пожилого возраста, а также при комбинированном применении гепарина с фибринолитическими средствами, антиагрегантами и нестероидными противовоспалительными препаратами. На фоне активной гепаринотерапии желательно избегать назначения внутримышечных иньекций.

Передозировка Для нейтрализации НМГ требуется введение большего количества протамина сульфата (0,6 мл протамина сульфата нейтрализует около 0,1 мл НМГ).

Взаимодействие Взаимодействие Эффект гепарина уменьшается при одновременном применении с АКТГ, тироксином, тетрациклином. Действие гепарина усиливается непрямыми антикоагулянтами, антиагрегантами, фибринолитическими и нестероидными противовоспали-тельными средствами .

Длительность лечения больных ОКС НМГ в среднем составляет 5-7 суток. Длительность лечения больных ОКС НМГ в среднем составляет 5-7 суток. Исследования FRIC, FRAXIS и TIMI11В показали, что более продолжительное их применение не приводит к дополнительному снижению частоты «коронарных событий», но увеличивает риск кровотечений.

Результаты исследований FRIC, FRAXIS, TIMI 11В показали, что НМГ обладают не меньшей, но и не большей, чем НФГ, способностью снижать риск развития инфаркта миокарда и смерти у больных с нестабильной стенокардией напряжения и инфарктом миокарда без зубца Q. Результаты исследований FRIC, FRAXIS, TIMI 11В показали, что НМГ обладают не меньшей, но и не большей, чем НФГ, способностью снижать риск развития инфаркта миокарда и смерти у больных с нестабильной стенокардией напряжения и инфарктом миокарда без зубца Q.

Непрямые антикоагулянты ( антагонисты витамина К) Непрямые антикоагулянты являются антагонистами витамина К, нарушают синтез в печени протромбина и других (VII, IX, Х) витамин К-зависимых факторов свертывания крови. Для развития полного антикоагулянтного эффекта необходимо 48-72 ч. При необходимости достижения быстрого антикоагулянтного эффекта дополнительно применяется гепарин, В случае прекращения ранее проводившейся гепаринотерапии непрямые антикоагулянты назначаются за 1 сутки до отмены гепарина.

Способ применения и дозы Способ применения и дозы Для стандартизации результатов определения протромбинового времени, получаемых в разными лабораториях и с применением различных видов тромбопластина, ВОЗ (1983 г.) рекомендовала использовать международный нормализационный индекс (INR; International Normalized Ratio), который учитывает влияние используемого тромбопластина на величину протромбинового времени, определяемого в данной лаборатории.

Дозирование непрямых антикоагулянтов (OAK) производится индивидуально. Дозирование непрямых антикоагулянтов (OAK) производится индивидуально. Варфарин принимается 1 раз в день в фиксированное время после еды. Контроль MHO проводится через 8-10 ч после приема препарата. На протяжении первой недели определение MHO рекомендуется проводить ежедневно, затем 1 раз в неделю.

Использование общепринятых ранее стартовых ударных («насыщающих») доз OAK не рекомендуется по причине реальной угрозы тромбообразования (вследствие более быстрого снижения уровня антикоагулянтного протеина С в сравнении с фактором II).

Терапию OAK рекомендуется начинать с поддерживающих доз: 2,5-5 мг варфарина, 0,75-3 мг фенпрокумона, 1-4 мг аценокумарола.

Более низкие стартовые дозы показаны: лицам старше 60 лет, пациентам с нарушением функции почек и печени, АГ, ХСН, при сопутствующей терапии препаратами, усиливающими антикоагулянтный эффект OAK.

Если пациенту показан прием варфарина с целью достижения среднего уровня гипокоагуляции MHO = 2,5 (2,0-3,0), следует придерживаться алгоритма. Если пациенту показан прием варфарина с целью достижения среднего уровня гипокоагуляции MHO = 2,5 (2,0-3,0), следует придерживаться алгоритма. При достижении необходимого уровня MHO алгоритм дальнейшего наблюдения должен быть следующим: первое определение MHO - через 5-10 дней, второе - через 2 недели, третье - через 3 недели, четвертое и все последующие - через 4 недели.

Кровотечение является наиболее значимым и опасным осложнением терапии OAK. Ежегодная частота всех кровотечений составляет от 0,9 до 2,7%, фатальных - 0,07-0,7%. Внутричерепные кровотечения составляют 2% от всех геморрагий. Среди причин, приводящих к кровотечениям, основное значение имеют интенсивность и продолжительность лечения.

Факторы, повышающие риск кровотечений: Факторы, повышающие риск кровотечений: анемия, почечная недостаточность, нарушение функции печени, сопутствующая терапия нестероидными противовоспалительными препаратами и кортикостероидами, нарушение питания, злокачественные опухоли, возраст старше 80 лет.

Первые месяцы лечения OAK обычно сопряжены с большим риском кровотечений (до 3%), вследствие неустойчивого уровня коагуляции при подборе дозы препарата. Первые месяцы лечения OAK обычно сопряжены с большим риском кровотечений (до 3%), вследствие неустойчивого уровня коагуляции при подборе дозы препарата. Если во время терапии OAK возникло кровотечение, необходимо оценить: степень его тяжести, значение MHO, уточнить режим приема OAK и других лекарств.

При высоком показателе MHO без кровотечения (5<МНО<9) следует пропустить 1-2 приема препарата, осуществлять контроль MHO и возобновить лечение при терапевтических значениях MHO или пропустить 1 прием OAK, назначить витамин K в дозе 1-2,5 мг. Если необходима срочная коррекция, доза витамина K должна составлять 2-4 мг. Если при этом MHO сохраняет высокие значения на протяжении суток, необходимо еще раз назначить витамин K в дозе 1-2,5 мг.

При еще более высоком MHO (выше 9) следует пропустить 1 прием OAK, принять витамин K в дозе 5 мг. Если MHO сохраняет высокие значения на протяжении 24-48 ч, принимать витамин K в дозе 1-2,5 мг. Возобновить лечение OAK при достижении терапевтических значений MHO.

При небольшом кровотечении (гематурия, носовое кровотечение) следует прекратить прием OAK на 1-2 дня и назначить витамин K в дозе 0,5 мг внутривенно или 5-10 мг внутрь. Внутривенное введение витамина K должно проводиться со скоростью не более 1 мг/мин вследствие угрозы развития анафилаксии.

Если возникло угрожающее жизни кровотечение (внутричерепное или желудочно-кишечное), необходимо: Если возникло угрожающее жизни кровотечение (внутричерепное или желудочно-кишечное), необходимо: прекратить прием препарата, назначить внутривенное введение витамина K 5-10 мг (при необходимости его повторить) вводить внутривенно концентраты факторов II, IX, X или свежезамороженную плазму (15 мл/кг).

Побочные эффекты На фоне приема OAK могут возникнуть тошнота, рвота, диарея, повышение температуры, лейкопения, выпадение волос, желтуха, стоматит, некроз кожи, боли в пальцах ног. Кожные некрозы чаще развиваются в первые недели терапии, преимущественно у женщин, и возникают на бедрах, передней брюшной стенке, молочных железах. Проявляясь первоначально в виде экхимозов, они быстро прогрессируют в геморрагические буллы.

Взаимодействие Действие непрямых антикоагулянты усиливают: другие антитромботические средства, азатиоприн, аллопуринол, амиодарон, анаболики, наркотические анальгетики, андрогены, антибиотики, трициклические антидепрессанты, глюкокортикостероиды, диазоксид, дизопирамид, налидиксовая кислота, фибраты, метронидазол, парацетамол,резерпин, сульфаниламиды, циметидин, хинидин, гормоны щитовидной железы, токоферол, тетурам.

Взаимодействие Действие непрямых антикоагулянтов ослабляют: анаприлин, антациды, барибитураты, диуретики, карбамазепин, рифампицин, витамины К и С, оральные контрацептивы, холестирамин.

Фибринолитические препараты Фибринолитические (тромболитические) препараты - активаторы плазминогена переводят циркулирующий в крови неактивный белок плазминоген в активный фермент плазмин, вызывающий лизис свернувшегося фибрина и разрушение тромба (тромболиз). Кроме этого, плазмин вызывает разрушение фибриногена (фибриногенолиз) и других белковых факторов свертывания крови, что ведет к риску развития геморрагических осложнений.

Механизм действия тромболитических средств заключается в растворении фибринового тромба. Механизм действия тромболитических средств заключается в растворении фибринового тромба. Этот тромб может как образоваться в пораженной атеросклерозом артерии, так и явиться результатом эмболии. Локализация и происхождение тромба и общее состояние больного, имеют важное значение при решении вопроса о целесообразности тромболитической терапии в каждом конкретном случае, учитывая высокую стоимость тромболитических препаратов и связанный с их применением риск развития серьезных геморрагических осложнений.

Тромболитическая терапия показана: в остром периоде инфаркта миокарда, при массивной или субмассивной тромбоэмболии, тромбозе крупных артерий (бедренных, подколенных, подключичных и др.), возможно, в первые часы после возникновения инсульта тромбоэмболического происхождения.

Не рекомендуется применение тромболитических препаратов для лечения тромбоза глубоких вен нижних конечностей, так как частичный лизис венозного тромба может повысить риск развития тромбоэмболии легочной артерии.

Венозные тромбы, как правило, легче лизируются, чем артериальные, поэтому при лечении ТЭЛА требуются гораздо меньшие дозы тромболитических препаратов, чем при лечении острого инфаркта миокарда. Венозные тромбы, как правило, легче лизируются, чем артериальные, поэтому при лечении ТЭЛА требуются гораздо меньшие дозы тромболитических препаратов, чем при лечении острого инфаркта миокарда. В первом случае причиной заболевания служит венозный по происхождению тромб, Во втором - фибриновый тромб образуется в месте пораженной атеросклерозом коронарной артерии.

Тромболитическая терапия направлена на то, чтобы по возможности быстро растворить фибриновый тромб и восстановить антероградный кровоток в соответствующем органе или части его. Тромболитическая терапия направлена на то, чтобы по возможности быстро растворить фибриновый тромб и восстановить антероградный кровоток в соответствующем органе или части его. Для этого необходимо повысить фибринолитическую активность крови больного. Это достигается двумя путями: введением активированного in vitro плазмина, увеличивая тем самым его содержание в крови; введением активаторов плазминогена, которые усиливают образование плазмина из эндогенного плазминогена.

Фибринолитические средства можно разделить на 3 основные группы: Фибринолитические средства можно разделить на 3 основные группы: препараты первого поколения, которые активируют и связанный с фибрином, и циркулирующий в крови плазминоген и имеют короткие Т ½ (стрепто- и урокиназа); препараты второго поколения, обладающие относительной специфичностью к связанному с фибрином плазминогену и более продолжительными Т ½ (рекомбинантная проурокиназа, АПСАК — анизоилированный плазминоген-стрептокиназный активаторный комплекс), рекомбинантный тканевый активатор плазминогена — ТАП); препараты третьего поколения, обладающие более высокой тромболитической активностью (негликозилированный рекомбинантный ТАП, химерные молекулы, содержащие различные участки ТАП и урокиназы, и др.).

Стрептокиназа - непрямой активатор плазминогена, неферментный белок, образующий комплекс с плазмином, Стрептокиназа - непрямой активатор плазминогена, неферментный белок, образующий комплекс с плазмином, Комплекс стрептокиназа-плазминоген играет роль фермента в превращении эндогенного плазминогена в плазмин, Т½ стрептокиназы 15- 25 минут.

С учетом динамики антистрептокиназных антител, обычно не рекомендуют повторное введение стрептокиназы после проведенного лечения, а также сразу после перенесенной стрептококковой инфекции. С учетом динамики антистрептокиназных антител, обычно не рекомендуют повторное введение стрептокиназы после проведенного лечения, а также сразу после перенесенной стрептококковой инфекции. Установлено, что в течение 72 ч после лечения стрептокиназой повторное ее введение (при необходимости) может быть эффективным и безопасным у большинства больных.

Показания Показания инфаркт миокарда, ТЭЛА, тромбоз периферических артерий, острая артериальная тромбоэмболия, тромбоз глазных сосудов.

Фибринолитические препараты Показанием к ТЛТ является ангинозная боль длительностью более 30 мин, сохраняющаяся несмотря на прием нитроглицерина, в сочетании с элевацией на 1 мм и более сегмента ST не менее чем в 2-х смежных отведениях ЭКГ или появлением полной блокады левой ножки пучка Гиса.

Противопоказания существующее или недавно перенесенное кровотечение, все формы пониженной свертываемости крови и другие геморрагические диатезы, перенесенная травма или хирургическое вмешательство перенесенный геморрагический инсульт, опухоль головного мозга, язвенные поражения ЖКТ, расслаивание аорты, кома, тяжелая АГ, деструктивные заболевания легких, острый панкреатит, тяжелые заболевания печени, гиперчувствительность к препарату, диабетическая микроангиопатия, фибрилляция предсердий, бактериальный эндокардит.

Абсолютными противопоказаниями к ТЛТ являются: Абсолютными противопоказаниями к ТЛТ являются: геморрагический инсульт в анамнезе, ишемический инсульт или динамическое нарушение мозгового кровообращения в течение последнего года, внутричерепная опухоль, активное внутреннее кровотечение, расслаивающая аневризма аорты.

Побочные действия Побочные действия лихорадка, озноб и другие аллергические реакции, кровотечения, геморрагический инсульт, тошнота, рвота, боли в спине, реперфузионная аритмия, гипотензия, отек легких.

Фибринолитические препараты Для профилактики аллергических реакций (включая анафилактический шок) рекомендуют перед введением стрептокиназы внутривенно ввести глюкокортикостероиды (до 180-240 мг преднизолона) и/или антигистаминные препараты. Предостережения особой осторожности требует применение стрептокиназы при инвазивных исследованиях, после артериальной пункции, при наличии аневризмы аорты и пристеночных тромбов, а также в сочетании с антикоагулянтной терапией.

Взаимодействия: при сочетанном применении с антиагрегантами и антикоагулянтами увеличивается риск кровотечения и других геморрагических осложнений. Взаимодействия: при сочетанном применении с антиагрегантами и антикоагулянтами увеличивается риск кровотечения и других геморрагических осложнений. Способ применения и дозы: при и ТЭЛА - внутривенная инфузия 250000 МЕ за 30 минут, затем по 100000 МЕ/ч до 24 ч и более в зависимости от достигнутого тромболитического эффекта и уровня дефибриногенизации крови (фибриноген в плазме крови - не мене 1 г/л, или увеличение тромбинового времени в 2-4 раза).

При инфаркте миокарда 1500000 МЕ в течение 60 минут. В случае дополнительного применения гепаринотерапии контроль за лечением осуществляется по величине АЧТВ (увеличение показателя в 2-3 раза). Стрептокиназа выпускается во многих странах мира под различными коммерческими названиями: "стрептаза", "кабикиназа", «авелизин», «целиаза» и др.

ТКАНЕВОЙ АКТИВАТОР ПЛАЗМИНОГЕНА (ТАП) представляет собой сериновую протеазу с молекулярной массой 72000 Д, которая синтезируется преимущественно эндотелиальными клетками сосудов. ТКАНЕВОЙ АКТИВАТОР ПЛАЗМИНОГЕНА (ТАП) представляет собой сериновую протеазу с молекулярной массой 72000 Д, которая синтезируется преимущественно эндотелиальными клетками сосудов. В кровяное русло ТАП секретируется в виде одноцепочечной молекулы (молекулярная масса 700000 Д), которая превращается в двухцепочечную под действием плазмина, трипсина, калликреина или фактора Ха свертывающей системы крови. Свойством ТАП является его очень высокая избирательность в отношении связанного с фибрином плазминогена, что обеспечивает преимущественную активацию на поверхности фибринового тромба.

ТАП не обладает антигенными свойствами и не оказывает существенного влияния на гемодинамику; пирогенные и аллергические реакции в ответ на введение ТАП встречаются редко. ТАП не обладает антигенными свойствами и не оказывает существенного влияния на гемодинамику; пирогенные и аллергические реакции в ответ на введение ТАП встречаются редко. ТАП выделяют из ткани матки человека и культуры клеток человеческой меланомы. В последние годы для клинического применения ТАП получают ДНК-рекомбинантным методом. Препарат одноцепочечного ТАП, полученного рекомбинантным методом, получил название "альтеплаза" (alteplase), а двухцепочный ТАП -"дутеплаза" (duteplase). Альтеплаза выпускается под патентованными названиями: "активаза" (activase) и "актилизе" (actilyse).

В клинической практике используется одноцепочечный рекомбинантный ТАП или альтеплаза. Т½ ТАП составляет 4-8 минут. В клинической практике используется одноцепочечный рекомбинантный ТАП или альтеплаза. Т½ ТАП составляет 4-8 минут. Для лечения острого инфаркта миокарда альтеплазу назначают в общей дозе 100-150 мг в течение 3 ч, причем первые 6-10 мг препарата вводят в виде болюса в течение 2 минут. В связи с тем, что альтеплаза в общей дозе 150 мг часто вызывает геморрагические осложнения, а 3-х-часовая инфузия слишком поздно приводит к реканализации инфаркт-связанной коронарной артерии, предложены две схемы введения рекомбинантного ТАП.

Исследование GUSTO доказало, что ускоренный режим введения альтеплазы является наилучшей стратегией тромболитической терапии в настоящий момент для пациентов с инфарктом миокарда. Исследование GUSTO доказало, что ускоренный режим введения альтеплазы является наилучшей стратегией тромболитической терапии в настоящий момент для пациентов с инфарктом миокарда.

Схема ускоренного введения альтеплазы (100 мг) при инфаркте миокарда в течение 6 ч от начала развития симптомов при массе тела более 65 кг следующая: Схема ускоренного введения альтеплазы (100 мг) при инфаркте миокарда в течение 6 ч от начала развития симптомов при массе тела более 65 кг следующая: 15 мг альтеплазы болюсно в течение 1-2 минут, затем инфузионно внутривенно 50 мг в течение 30 минут, затем 35 мг в течение 60 минут.

До начала внутривенное введение гепарина 5000 ME + внутривенная инфузия гепарина 1000 МЕ/ч в последующие двое суток. До начала внутривенное введение гепарина 5000 ME + внутривенная инфузия гепарина 1000 МЕ/ч в последующие двое суток. При ТЭЛА - внутривенная иньекция 10 мг альтеплазы в течение 1-2 минут, затем внутривенная инфузия 90 мг альтеплазы в течение 2-х ч.

Лабораторный контроль при проведении тромболитической терапии включает определение концентрации фибриногена в плазме крови. Лабораторный контроль при проведении тромболитической терапии включает определение концентрации фибриногена в плазме крови. После окончания тромболитической терапии назначают гепарин по указанной выше схеме. Эффект тромболитической терапии оценивается по: клиническим (уменьшение одышки, тахикардии, цианоза), электрокардиографическим (регресс признаков перегрузки правых отделов сердца) признакам, результатам повторной сцинтиграфии и др.

По сравнению с гепарином тромболитические препараты способствуют более быстрому растворению тромбоэмбола, что ведет: к увеличению легочной перфузии, снижению давления в легочной артерии, улучшению функции правого желудочка, повышению выживаемости больных при тромбоэмболии крупных ветвей.

Заключение Заключение Следовательно, прием аспирина в малых и средних дозах столь же эффективен, как и прием антикоагулянтов, однако риск осложнений антиагрегантной терапии гораздо меньше. Продолжительное (от 3 месяцев до 4 лет) применение варфарина (в дополнение к ацетилсалициловой кислоте) способствует снижению частоты реокклюзий инфаркт-зависимой коронарной артерии у больных ИМ после успешной ТЛТ, уменьшению риска развития ИМ, мозгового инсульта и смерти без достоверного увеличения частоты геморрагических осложнений. Широкое применение варфарина во вторичной профилактике ИБС ограничивается необходимостью регулярного контроля антикоагуляционного эффекта по величине МНО.

Заключение Заключение ТЛТ, выполненная позже 12 ч от момента развития ИМ, позитивного влияния на смертность не оказывает. При отсутствии стойкой элевации сегмента ST, которая рассматривается как признак закупорки коронарной артерии фибринсодержащим тромбом, применение ТЛТ также нецелесообразно. Целесообразность применения НФГ в сочетании с ТЛТ оспариваеся. Согласно современным представлениям, если тромболизис проводится неспецифичными фибринолитическими препаратами (стрептокиназа, анистреплаза, урокиназа) на фоне применения ацетилсалициловой кислоты в полной дозе, введение гепарина необязательно. При применении альтеплазы внутривенное введение гепарина считается оправданным. .