Презентация на тему: ЖЕСТКОСТЬ ВОДЫ

Цели занятия: Цели занятия: Развить умения: выделять существенные признаки и свойства объектов Классифицировать факты, делать выводы Формировать практические навыки работы с веществами и химическим оборудованием Развивать познавательные интересы, коммуникативные качества, уверенность в своих силах, настойчивость, умение действовать самостоятельно Воспитывать культуру умственного труда

«Ни одна наука не нуждается в эксперименте в такой степени, как химия. Её основные законы, теории и выводы опираются на факты. Поэтому постоянный контроль опытом необходим». «Ни одна наука не нуждается в эксперименте в такой степени, как химия. Её основные законы, теории и выводы опираются на факты. Поэтому постоянный контроль опытом необходим». М. Фарадей

«Свои способности, человек может узнать только попытавшись приложить их.» «Свои способности, человек может узнать только попытавшись приложить их.» Сенека Младший

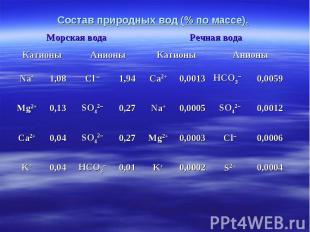
Аристотель считал воду одним из «элементов» мироздания. Аристотель считал воду одним из «элементов» мироздания. Российский геохимик, академик Александр Евгеньевич Ферсман назвал воду самым важным «минералом» на Земле. Гимном этому веществу стали слова писателя Антуана Сент-Экзюпери: «Вода – у тебя нет цвета, ни вкуса, ни запаха, тебя невозможно описать, тобою наслаждаются, не ведая, что ты такое. Нельзя сказать, что ты необходима для жизни. Ты сама – жизнь». На Земле имеется громадное количество воды, человек непосредственно может использовать не более 0,05% общего количества воды. Воды морей и океанов содержат в среднем 3,5% растворённых веществ. Это соли – хлориды и сульфаты магния, которые находятся в морской воде в виде ионов. Морская вода содержит 35г соли на 1 литр. Морская вода содержит растворённые газы и органические соединения. Речные воды содержат ионы, нейтральные молекулы, взвешенные частицы, солей в них гораздо меньше.
ЖЁСТКАЯ МЯГКАЯ

Для питания паровых котлов Для питания паровых котлов Для применения в химической технологии В производстве керамике, бетонных смесей, затворение глин Приводит к нарушению работ теплосетей
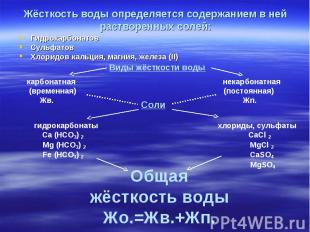
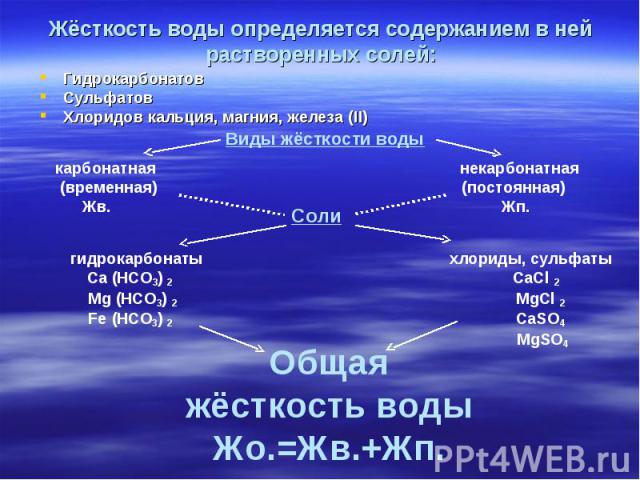
Гидрокарбонатов Гидрокарбонатов Сульфатов Хлоридов кальция, магния, железа (II)
![Карбонатная жёсткость (временная) [Жв.] – Карбонатная жёсткость (временная) [Жв. Карбонатная жёсткость (временная) [Жв.] – Карбонатная жёсткость (временная) [Жв.](https://fs1.ppt4web.ru/images/95274/148950/310/img8.jpg)
Карбонатная жёсткость (временная) [Жв.] – Карбонатная жёсткость (временная) [Жв.] – метод кислотно-основного титрования Общая жёсткость [Жо.] – метод комплексонометрии Некарбонатная (постоянная) [Жп.] – определяют по разности между Ж общая - Ж временная Жв. (постоянная) = Ж общая - Ж временная


Экспертные группы Экспертные группы Химический анализ I гр. Водопроводная вода II гр. Родниковая вода III гр. Снеговая (талая) вода IV гр. Прудовая вода (водоём «Копань», район ОАО «Биосинтез») V гр. Морская вода VI гр. Вода и моющие средства VII гр. Общая жёсткость воды

№1 Определение жесткости водопроводной воды №1 Определение жесткости водопроводной воды №2 Определение жесткости родниковой воды №3 Определение жесткости снеговой (талой) воды №4 Определение жесткости воды водоёма (Копань район ОАО «Биосинтез») №5 Определение жесткости морской (искусственной) воды №6 Вода и МС (мыло, стиральный порошок) №7 Общая жёсткость воды (водопроводная, морская)
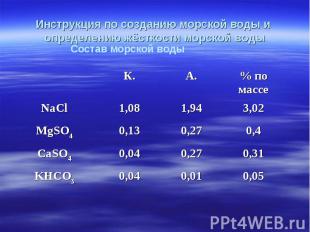

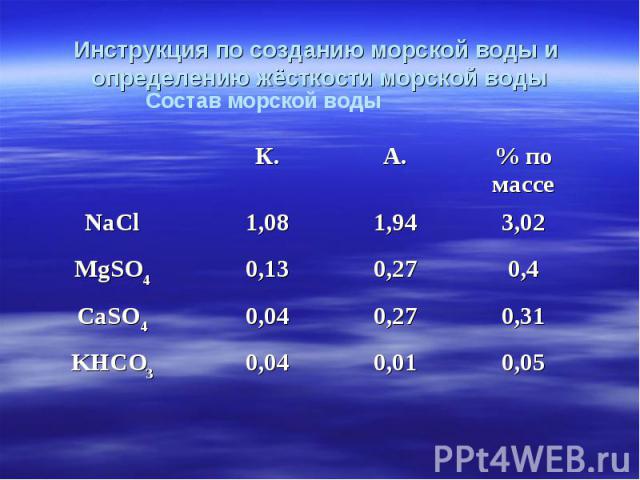
Рассчитать весовые части солей морской воды Рассчитать весовые части солей морской воды 3,02: 0,4: 0,31: 0,05 60,4: 8 : 6,2 : 1 весовые части: MgSO 4 – 8г CaSO4 – 6г NaCl – 60г KHCO3 – 1г Отмерить (взвесить) на весах соли: NaCl MgSO4 CaSO4 KHCO3 Отмерить воду дист. объёмом 100 см3 Растворить соли в воде дист., тщательно перемешать Добавить в морскую воду 3 капли индикатора метилоранж Оттитровать стандартным раствором соляной кислоты (С=0,1 моль/л) до изменения окраски индикатора Определить объём израсходованной кислоты. Анализ проводим 3 раза! Оформить отчёт в таблицу «Определение жёсткости воды»


Карбонатная жёсткость: Карбонатная жёсткость: Жк. =C(HCl)*V(HCl)*1000 V (H2O) V (H2O) – объём воды, взятый на титрование 1000 – 1л воды, в котором по ГОСТУ определяют жёсткость воды. Жёсткость воды Мягкая ≤4 Средне жёсткая 4─8 Жёсткая 8─12 Очень жёсткая ≥12

Цель: выяснить действия различной воды на моющие средства Цель: выяснить действия различной воды на моющие средства А) мыло Б) стиральный порошок проанализировать информацию о жёсткости воды

Жёсткость воды влияет на пенообразование МС (мыла, стирального порошка). Жёсткость воды влияет на пенообразование МС (мыла, стирального порошка). Оценить это качество воды можно по количеству пены, появляющиеся при встряхивании образцов воды с добавкой раствора моющего средства (мыла. стирального порошка).

Оборудование: Оборудование: Штатив с одинаковыми пробирками, стеклянные палочки, ложки, линейка, резинки аптечные, часы песочные 1мин. Реактивы: мыло, стиральный порошок вода: водопроводная родниковая снеговая прудовая морская

Пронумерованные пробирки заполните на 1/5 их объёма исследуемой водой. Пронумерованные пробирки заполните на 1/5 их объёма исследуемой водой. Добавьте в каждую пробирку: а) кусочек мыла размером с горошину б) 1 ложечку стирального порошка Тщательно перемешайте стеклянными палочками и закройте пробками. Соединив пробирки вместе аптечной резинкой, одновременно встряхивайте в течение 1 минуты. Измерьте линейкой высоту пены в каждой пробирке и оформите отчёт в таблицу.


Примечание: чтобы мыло было удобно резать на равные части, его следует размягчить: Примечание: чтобы мыло было удобно резать на равные части, его следует размягчить: кусочек мыла следует обернуть мокрой салфеткой, поместить на сутки в по лиэтиленовый пакет. Нарезать кусочки одинакового размера.

Установлено: Установлено: Iгр. Водопроводная вода Жводы = IIгр. Родниковая вода Жводы = IIIгр. Снеговая (талая) вода Жводы = IVгр. Прудовая вода Жводы = Vгр. Морская вода Жводы =

Определяется Жо. воды – методом комплексонометрии - титриметрический метод, основан на реакциях взаимодействия определяемых ионов с некоторыми органическими реагентами. Ионы металлов практически мгновенно взаимодействуют с комплексонами с образованием растворимых малодиссоциированных соединений постоянного состава. Определяется Жо. воды – методом комплексонометрии - титриметрический метод, основан на реакциях взаимодействия определяемых ионов с некоторыми органическими реагентами. Ионы металлов практически мгновенно взаимодействуют с комплексонами с образованием растворимых малодиссоциированных соединений постоянного состава. Комплексон (III) (трилон Б) со многими катионами образует прочные растворимые в воде внутрикомплексные соли: Трилон Б определяют ионы: Ca 2+, Mg 2+, Br 2+, Cu 2+ , Zn 2+, Ni 2+, Al 3+, Cr 3+, Co 3+. Грамм – эквивалент металла, независимо от степени окисления связывает один грамм – эквивалент комплексона.

Исследуемую воду объём 10 мл поместить в колбу. Исследуемую воду объём 10 мл поместить в колбу. Анализируемую воду подщелочить до pH=10, прибавляя аммонийную буферную смесь. Добавить индикатор хромоген чёрный. Титровать трилоном Б (титр установлен ранее). Появление синей окраски раствора указывает на окончание реакции. Определить Жо. Воды по формуле. Ж=Cn (Na [H2Tr])*V (Na2 [H2Tr])*1000/V(H2O) Где Cn (Na [H2Tr]) – нормальность трилона Б V (H2O) – объём анализируемой воды V (Na2 [H2Tr]) – объём трилона Б, пошедший на титрование C (трилон Б)= 0,1 моль/л

(Метод комплексонометрии) – титриметрический метод, основан на реакциях взаимодействия определяемых ионов с некоторыми органическими реагентами. (Метод комплексонометрии) – титриметрический метод, основан на реакциях взаимодействия определяемых ионов с некоторыми органическими реагентами. Ионы металлов практически мгновенно взаимодействуют с комплексонами с образованием растворимых мало диссоциированных соединений постоянного состава. Комплексон III (трилон Б) со многими катионами образует прочные растворимые в воде внутрикомплексные соли. Трилон Б – определяют ионы Ca 2+, Mg 2+, Co 3+, Cu 2+, Zn 2+, Ni 2+, Al 3+, Cr 3+, PO43-. Грамм – эквивалент металла, независимо от степени окисления, связывает один грамм – эквивалент комплексона. Общая жёсткость воды показывает содержание мили/моль гидрокарбонатов, сульфатов и хлоридов кальция и магния в 1л воды.

Цель: определить Жо. воды водопроводной Цель: определить Жо. воды водопроводной Оборудование: бюретка, колба, химический стакан Реактивы: вода водопроводная, аммонийная буферная смесь (100мл 20% раствора NH4Cl и 100мл 20% раствора NH3), индикатор хромоген чёрный, трилон Б (0,1н) Отмерить объём исследуемой воды (водопроводной) 100см3 или 100мл Добавить 5см3 аммонийной буферной смеси 5-7 капель спиртового индикатора хромогена чёрного Титровать трилоном Б (комплексон III) (по каплям встряхивать) Появление синей окраски раствора указывает на окончание реакции.

![Жо=Cn (Na [H2Tr])*V (Na2[H2Tr])*1000/V(H2O) Жо=Cn (Na [H2Tr])*V (Na2[H2Tr])*1000 Жо=Cn (Na [H2Tr])*V (Na2[H2Tr])*1000/V(H2O) Жо=Cn (Na [H2Tr])*V (Na2[H2Tr])*1000](https://fs1.ppt4web.ru/images/95274/148950/310/img28.jpg)
Жо=Cn (Na [H2Tr])*V (Na2[H2Tr])*1000/V(H2O) Жо=Cn (Na [H2Tr])*V (Na2[H2Tr])*1000/V(H2O) Где Cn (Na [H2Tr]) – нормальность трилона Б V (H2O) – объём анализируемой воды V (Na2[H2Tr]) – объём трилона Б, пошедший на титрирование или Жо = С(1/2 Na2H2Tr)*V(Na2H2Tr)*1000 100 Жо – [ммоль/л] Расход трилона больше 5см3 на 100см3 Суммарное содержание кальция, магния c (1/2 Ca 2+, Mg 2+) больше 0,5 ммоль/л. титрование повторить, взяв меньший объём воды. Нечёткое уменьшение окраски раствора в точке эквивалентности указывает на присутствие в воде катионов Cu 2+, Zn 2+, Mn 2+.

«Опыт - единственная верный путь спрашивать природу и слышать ответ в её лаборатории» «Опыт - единственная верный путь спрашивать природу и слышать ответ в её лаборатории» Д. И. Менделеев







![Карбонатная жёсткость (временная) [Жв.] – Карбонатная жёсткость (временная) [Жв.] – метод кислотно-основного титрования Общая жёсткость [Жо.] – метод комплексонометрии Некарбонатная (постоянная) [Жп.] – определяют по разности между Ж общая - Ж време… Карбонатная жёсткость (временная) [Жв.] – Карбонатная жёсткость (временная) [Жв.] – метод кислотно-основного титрования Общая жёсткость [Жо.] – метод комплексонометрии Некарбонатная (постоянная) [Жп.] – определяют по разности между Ж общая - Ж време…](https://fs1.ppt4web.ru/images/95274/148950/640/img8.jpg)


















![Жо=Cn (Na [H2Tr])*V (Na2[H2Tr])*1000/V(H2O) Жо=Cn (Na [H2Tr])*V (Na2[H2Tr])*1000/V(H2O) Где Cn (Na [H2Tr]) – нормальность трилона Б V (H2O) – объём анализируемой воды V (Na2[H2Tr]) – объём трилона Б, пошедший на титрирование или Жо = С(1/2 Na2H2Tr)*… Жо=Cn (Na [H2Tr])*V (Na2[H2Tr])*1000/V(H2O) Жо=Cn (Na [H2Tr])*V (Na2[H2Tr])*1000/V(H2O) Где Cn (Na [H2Tr]) – нормальность трилона Б V (H2O) – объём анализируемой воды V (Na2[H2Tr]) – объём трилона Б, пошедший на титрирование или Жо = С(1/2 Na2H2Tr)*…](https://fs1.ppt4web.ru/images/95274/148950/640/img28.jpg)